Genes & Devel:为什么干细胞可以维持多潜能性?
2015-10-15 佚名 生物谷
图片来源:medicalxpress.com为什么干细胞研究这么火热,因为其具有多向性,可以转变成机体中任何类型的细胞,而这种潜能常常被研究者们用来移除机体损伤或病变的组织细胞,但控制干细胞具有多向潜能的机制目前还并不清楚。近日,发表在国际杂志Genes & Development上的一项研究论文中,来自基础科学研究院的研究人员利用小鼠的胚胎干细胞(mESCs)进行研究揭示了控制诱导多能干
为什么干细胞研究这么火热,因为其具有多向性,可以转变成机体中任何类型的细胞,而这种潜能常常被研究者们用来移除机体损伤或病变的组织细胞,但控制干细胞具有多向潜能的机制目前还并不清楚。
近日,发表在国际杂志Genes & Development上的一项研究论文中,来自基础科学研究院的研究人员利用小鼠的胚胎干细胞(mESCs)进行研究揭示了控制诱导多能干细胞(iPSCs)的分子机制,研究者发现,16个RNA的结合蛋白(RBPs),这些结合蛋白的剔除可以引发干细胞多能性的缺失,同时还发现了6个无包被的RBPs(Krr1, Ddx47, Ddx52, Nol6, Pdcd11, 和Rrp7a)其可以组成关键的蛋白复合体—小亚基加工体,对于核糖体的制造非常关键。
首先研究人员利用RNAi技术对小鼠的胚胎干细胞进行筛选,来确定哪一种RBPs对于RNA介导的基因调节非常关键,研究者进行了两轮的RNAi筛选目的在于寻找干细胞的多潜能性,最终发现了16个阳性指示,随后他们发现,组成小亚基加工体的6个RBPs可以调节18S rRNA的生成从而帮助制造多能细胞的重要调节子,此外研究者还检测了另外27个涉及核糖体生成的基因来确定是否小亚基加工体(SSUP)需要ESC来维持,剔除小亚基加工体蛋白(Imp4, Mpp10/Mphosph10, Wdr36, Wdr46, and Wdr75)将会导致Nanog表达的降低,而其中一种组分(Cirh1a)的缺失都会引发细胞死亡。
在ESCs中,SSUP的亚单位处于上调状态来增强其翻译的效率,并且可以支持控制干细胞多能性的互联调节网络;包括Krr1在内的SSUP基因在多育的细胞中都处于高度表达的状态,而多育的细胞则包括干细胞、祖细胞,尤其是ESC细胞系,这些可以增强广泛的转录效率,对于维持多能性因子的蛋白水平非常关键。
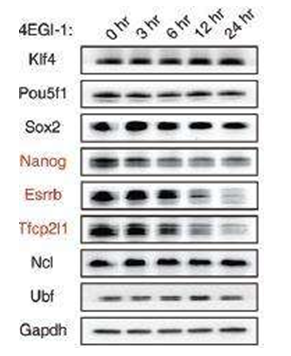
为了检测翻译如何影响ESCs,研究小组利用名为4EGI-1的翻译抑制子来处理mESCs,4EGI-1可以引发多能性因子Nanog, Esrrb, 和Tfcp2l1的水平快速下降来对翻译抑制产生反应,进一步研究发现,增强翻译的活性对于ESC维持功能非常重要,研究者还发现,SSUP蛋白对于诱导多能干细胞进行有效的重编程非常重要,当进行重编程实验时,研究者发现,相比对照细胞而言,内源性的Nanog和Esrrb因子的诱导大大减缓了,而且同时也抑制了Krr-1剔除的细胞的表达。
研究者表示,当主要转录因子长久维持在合适水平下时,ESCs就会处于多潜能状态,但当主要转录因子不再可以获得时,细胞就会进入分化状态,这就表明,翻译效率的精确调节可以精密地影响干细胞最终的决定。我们都知道核糖体的生成是细胞循环的关键组分,其会帮助调节细胞尺寸及生长,而如今研究者发现SSUP在维持诱导多能干细胞的完整性上扮演着重要的角色。
下一步研究人员计划进行更为深入的研究,来基于当前的研究数据再获得更多有价值的线索,最终帮助开发治疗多种疾病的新型疗法,尤其是癌症和神经变性疾病的新型疗法等。
原文出处:
Kwon Tae You1,,Joha Park1, and V. Narry Kim1,Role of the small subunit processome in the maintenance of pluripotent stem cells.Genes & Devel.2015
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Dev#
74
#Gene#
45
#多潜能性#
57