Science重磅:长出头发和皮肤修复,都离不开这种常见的维生素!
2024-03-25 Swagpp MedSci原创 发表于上海
Science:维生素A是调节谱系可塑性的关键调节因子。即通过控制维生素A的浓度能够协调毛囊干细胞的谱系可塑性,从而引导干细胞实现伤口愈合或毛发生长,对再生医学、伤口修复和癌症治疗具有重要意义。
众所周知,维生素是人体所需的六大营养素之一,也是维持人体正常生活及健康所必需的微量有机化合物。就绝大多数维生素而言,人体不能直接合成或合成量非常少,无法满足机体的需要。因此,必需由食物供给或直接补充以维持正常的生命活动和生理功能。
维生素A是一种易氧化的脂溶性维生素,通常代表视黄醇及其活性物质。与上述提及的那样,人体不能直接合成维生素A,因此需要从新鲜的食物或者补充剂获取。先前,梅斯医学开展的调研显示,受调查者中有8.57%坚持摄入维生素A补充剂;其中,有超一半的人表示吃维生素补剂的原因为,“身体出现某些症状,自我感觉需要补充”。
可别小看了维生素A,它与人体健康密切相关,在维持正常视力、生长发育、免疫功能、生殖和基因表达等方面均起到重要作用。相反,缺乏维生素A则会出现眼部症状、皮肤损害、食欲降低、免疫功能低下、血红蛋白合成代谢障碍等等情况。
而Science上最新发表的重磅研究,揭示了维生素A的又一大“全新”作用——调控干细胞的谱系选择。
具体来说,维生素A是调节谱系可塑性的关键调节因子。即通过控制维生素A的浓度能够协调毛囊干细胞的谱系可塑性,从而引导干细胞实现伤口愈合或毛发生长,对再生医学、伤口修复和癌症治疗具有重要意义。

DOI: 10.1126/science.adi7342
研究开始前要厘清一个概念「干细胞的谱系可塑性」。
在整个生命过程中,成体干细胞都发挥着“促进组织再生”的作用,严格调节组织再生的类型和时间。当机体受伤时,干细胞会被调动到“最需要”的区域,以扩大再生范围来加速修复。而在该过程中,成体干细胞需要从一个谱系过渡到另一个,因此会进入一种“谱系可塑性(lineage plasticity)”的状态。
谱系可塑性是指新旧谱系的细胞特性转录因子的双重表达,即在这种状态下原有细胞和新细胞的命运均会共同表达。这是一种典型的创伤诱导应激通路,赋予干细胞命运灵活性,有助于组织恢复健康。
举个简单的例子,生活中人们难免受伤,当一个孩子从自行车上摔下来并擦伤膝盖时,皮肤干细胞会冲向伤口并施展“救援”,长出新的表皮来覆盖伤口。但在大规模的“救援军”中,除了部分本身就发挥“皮肤再生”作用的干细胞外,还有一部分是从毛囊干细胞(HFSCs)变形来的。
通常情况下,毛囊干细胞的主要作用是促进头发生长。但当身体受到损伤时(比如膝盖擦伤),为了应对当下更为迫切的需求,毛囊干细胞便会转变形态为表皮干细胞,汇入“修复大军”中帮助伤口的恢复。为此,毛囊干细胞要进入“谱系可塑性”的状态,需暂时表达毛发和表皮两种干细胞的转录因子。

毛囊干细胞的动员和扩张
但正如本研究的参与者之一Matthew T. Tierney博士所述,谱系可塑性是一把“双刃剑”。在出现损伤时,毛囊干细胞能够及时转入谱系可塑性状态,实现伤口的修复;但如果不受控并一直保持在修复模式中,则会导致慢性伤口状态或癌症发生。
为了找到调控谱系可塑性的关键因素,研究者选择了哺乳动物的皮肤上皮作为研究对象,原因有二:在应对环境损伤时,这种屏障组织能够实现快速愈合;与此同时,哺乳动物的皮肤上皮包含了多个离散的干细胞群,而这些干细胞群源自一个共同的胚胎祖细胞,这其中就包括了毛囊干细胞。
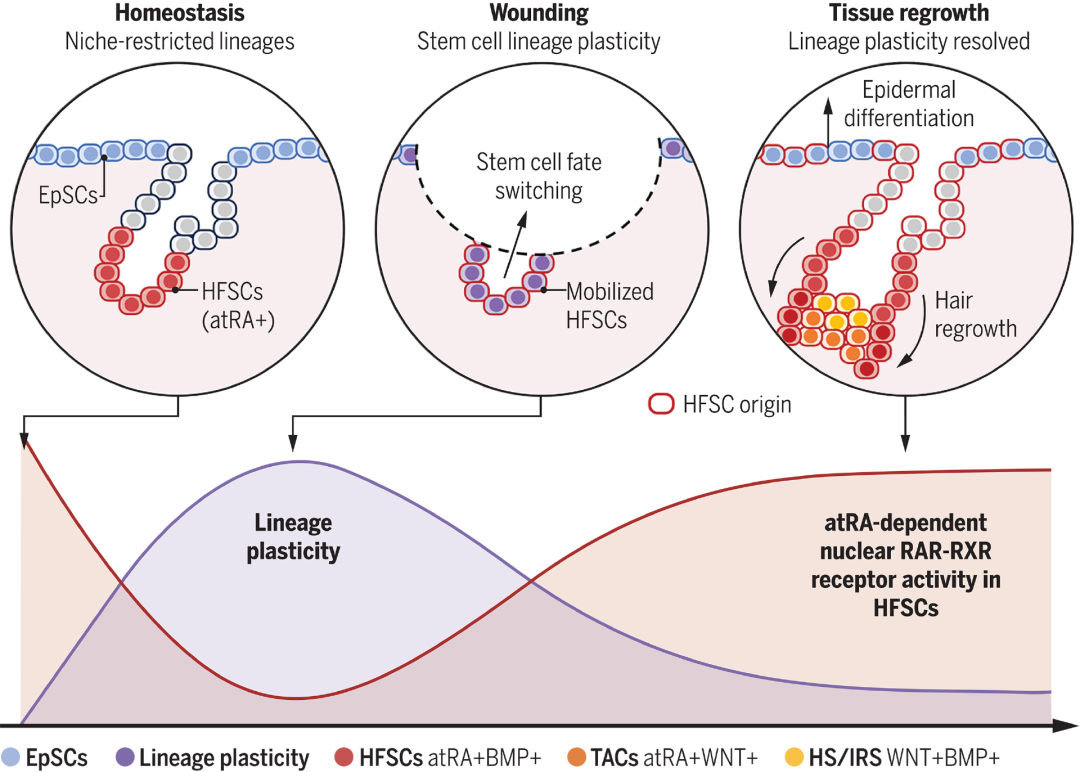
在伤口愈合期间干细胞的谱系可塑性
在筛选小分子库之后,研究者惊讶地发现,视黄酸(一种具有生物活性的维生素A)是干细胞脱离谱系可塑性状态并在体外诱导分化为头发或表皮细胞的必要条件。而这算是维生素A的一种未知的全新功能。
体内和体外实验显示,视黄酸水平必须要保持在合理范围内,毛囊干细胞才能参与伤口修复的过程——如果视黄酸的水平过高,干细胞无法进入谱系可塑性状态,因此无法修复伤口;但如果视黄酸的水平过低,干细胞则会重点发挥伤口修复的作用,而阻碍了毛发的再生。
换言之,通过遗传、饮食和局部干预的小鼠实验后,研究者发现了维生素A的“天平”作用,即影响毛囊干细胞在皮肤损伤和毛发再生之间的平衡。一旦平衡被打破,就会发生皮肤和头发不可兼得的情况。
当然,视黄酸并不是单独发挥作用的,准确来说需要与BMP和WNT等蛋白信号分子相互作用,有效地编排形成毛囊所需的不同谱系,共同影响干细胞的平衡状态。
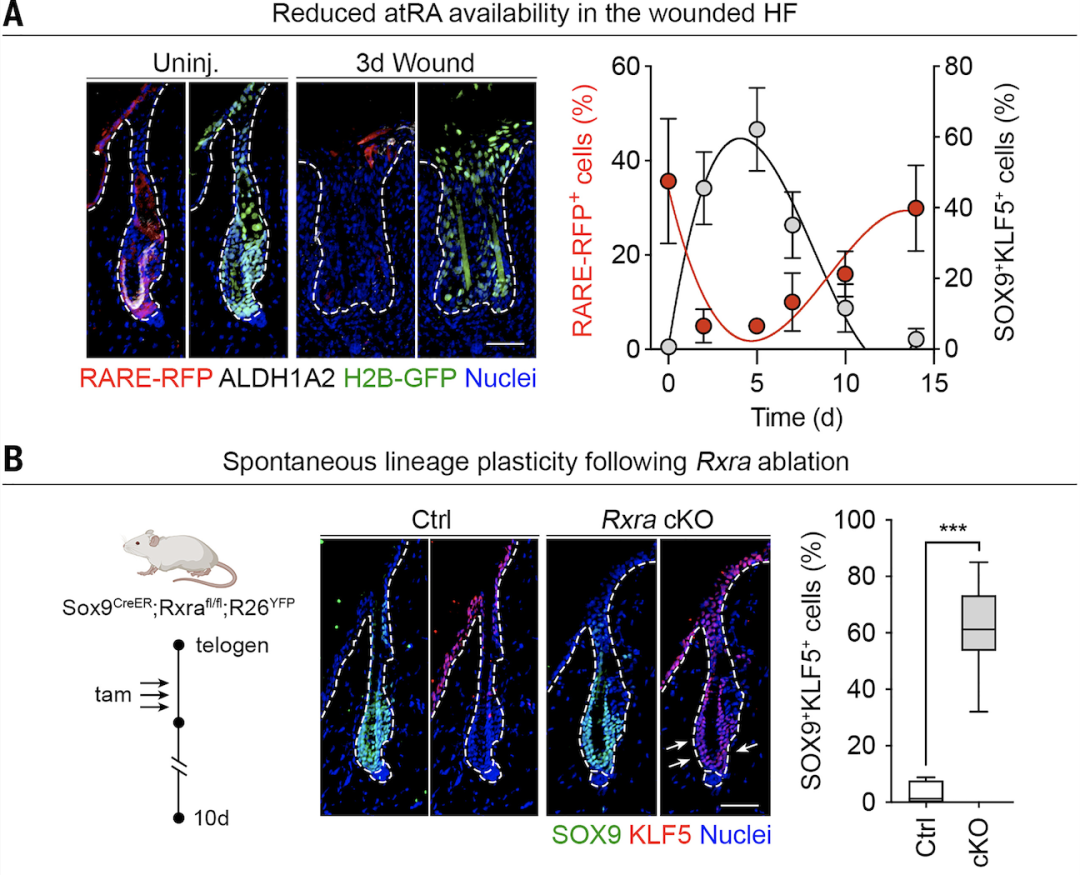
维生素A在谱系可塑性中发挥着重要作用
一直以来,人们观察到这样一个“矛盾相反”的现象:外用维生素A能够刺激伤口处的毛发生长;但过量的维生素A又会抑制毛发生长,甚至导致脱发的发生。而本研究则很好地解释了这一现象。
当然,除了再生医学和伤口修复之外,维生素A在癌症治疗领域可能存在的作用也引起了研究团队的兴趣,特别是鳞状细胞癌和基底细胞癌的谱系可塑性。事实上,癌症干细胞的特点是“不走寻常路”,当癌症干细胞的谱系可塑性不受控时,或成为致癌的关键因素。
既然调控和抑制谱系可塑性是控制肿瘤生长和改善预后的关键,那么维生素A或将成为癌症治疗的潜在有效药物。研究者兴奋地表示,抑制干细胞的谱系可塑性将成为改善癌症预后的重点研究方向,而这也将成为新前沿。
综上所述,该研究首次发现了维生素A在调节干细胞的谱系可塑性过程中的重要作用,即维持干细胞在皮肤修复和头发生长之间的平衡,或成为再生医学和肿瘤治疗领域的重点研究方向。
对于普通人来说,保证维生素A摄入的平衡,既不缺少也不过量,才是重中之重。按照膳食指南推荐摄入量,我国成人维生素A的RNI,男性为每天800μg RAE(视黄醇活性当量),女性为700μg RAE。
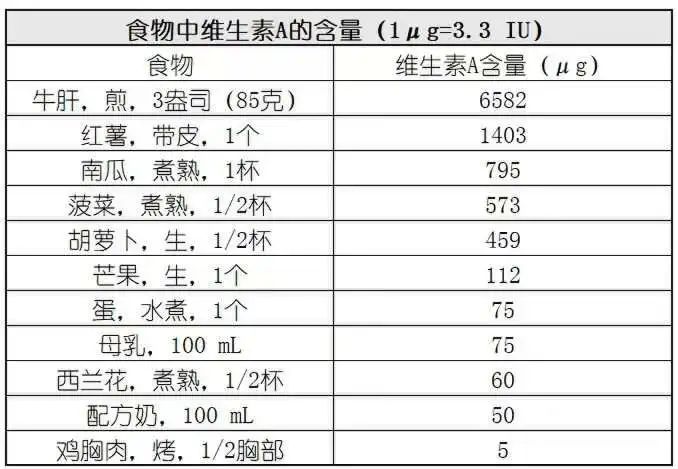
图源:微信公众号
参考资料:
[1]https://www.eurekalert.org/news-releases/1036957
[2]Matthew T. Tierney et al.,Vitamin A resolves lineage plasticity to orchestrate stem cell lineage choices.Science383,eadi7342(2024).DOI:10.1126/science.adi7342
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















谢谢分享
57
谢谢分享
59
谢谢分享
61
谢谢分享
57
#维生素A# #干细胞# #谱系选择# #毛发生长#
95