不明原因的反复发热,原因竟是…..
2022-05-10 “检验医学”公众号 “检验医学”公众号
对于发热,首先要明确病因,方能有效治疗。对于一直不明原因的反复发热,临床医生可能需要考虑的更多。
前 言
生活中,说起发热,大家并不陌生。发热分为感染性发热,非感染性发热及功能性发热三种。感染性发热,顾名思义,是由病原体侵入人体感染引起。非感染性发热主要见于肿瘤,结缔组织病,血液系统疾病及内分泌疾病等。功能性发热主要包括生理性发热及神经性发热。
对于发热,首先要明确病因,方能有效治疗。对于一直不明原因的反复发热,临床医生可能需要考虑的更多。对检验人员而言,我们则需要更多的细心与责任,在工作中发现蛛丝马迹,尽量避免漏诊和误诊,为每一位患者保驾护航。
案例经过
患者,女,62岁,农民,2022-02-21新冠核酸检测结果:阴性,患者1月前受凉后出现畏寒发热,间断发热1月,最高体温38.9℃,伴乏力,双下肢疼痛,头晕,纳差,以为感冒,遂至当地中医院就诊。
完善检查,诊断为“肺部感染、泌尿道感染、EB病毒感染、高血压病、双膝关节骨性关节炎”并先后行舒普深、阿米卡星、亚安培南抗感染治疗,期间体温有所下降,但又复升高,发热时间以晚上发热为主。
患者无头痛、恶心呕吐,无尿频、尿急、排尿困难,无咳嗽、咳痰、心慌、胸闷、气喘,无腹痛、腹胀、腹泻等不适,今为求进一步诊治,特来我院就诊,门诊以“发热待查”收入我科。起病以来,患者精神、食欲、睡眠欠佳,大便正常,小便尿量明显减少,体力、体重均有所下降。
入院后外周血检查结果显示白细胞升高,CRP升高,肝功能受损,凝血功能障碍,因患者反复发热,中度贫血,病因不明,建议完善骨髓穿刺,血培养等相关检查后以便明确诊断。
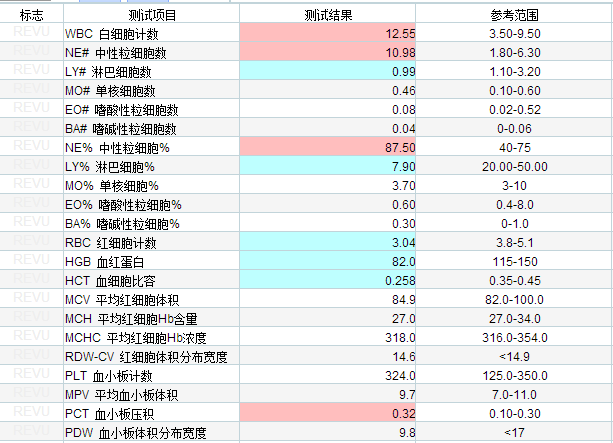

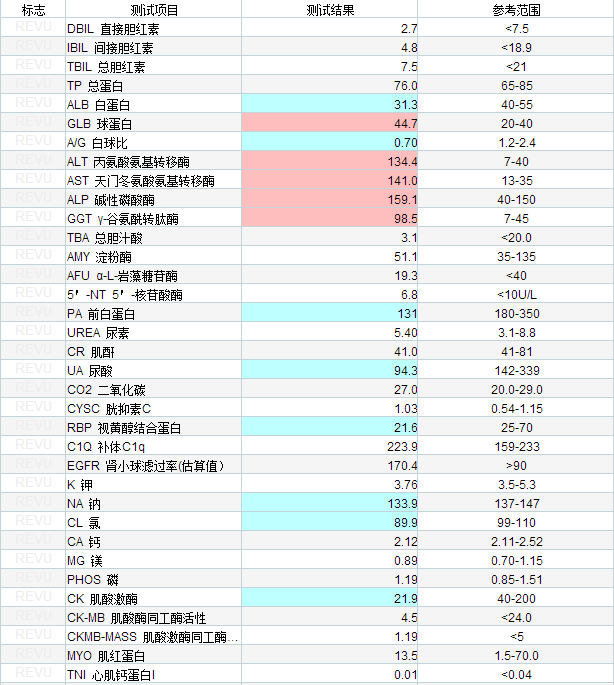
2月23日临床送检了患者的骨髓涂片,镜下结果出乎意料,又似乎意料之中。骨髓细胞学检查显示骨髓增生明显活跃,分类200个有核细胞,粒红两系各阶段细胞比例大致正常,形态未见明显异常,巨核细胞较常见,血小板簇状分布。
浏览全片时,偶尔能找到吞噬细胞的身影。认真浏览两张骨髓片后,终于找到比较典型的吞噬细胞吞噬血细胞现象。如下图所示,油镜视野下可见吞噬细胞吞噬红细胞,中性粒细胞及血小板。
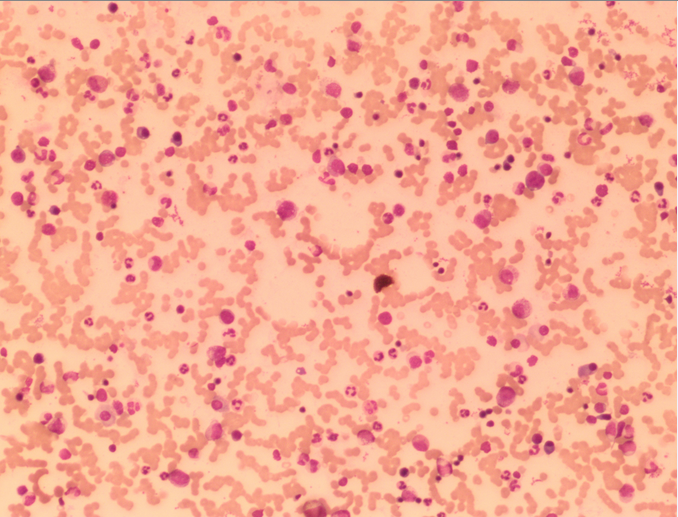
骨髓细胞学涂片 瑞姬氏 ×360
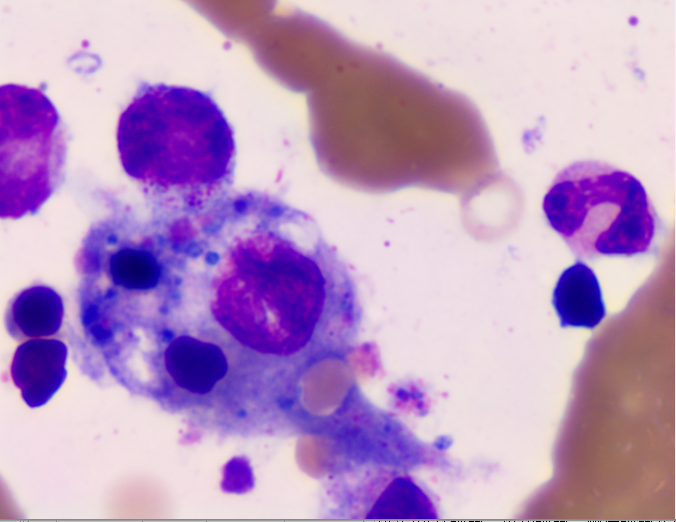
吞噬细胞吞噬成熟红细胞及血小板 瑞姬氏 ×1800
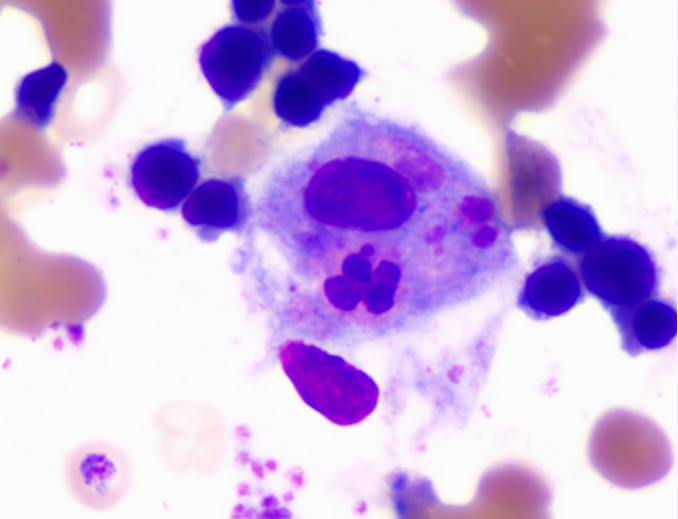
吞噬细胞吞噬中性粒细胞及血小板 瑞姬氏 ×1800
该患者1月余前无明显诱因出现间断性发热,伴畏寒寒颤,肝酶轻度异常,炎症指标升高,于外院抗感染治疗后,效果欠佳。入院4天后复查血常规及纤溶指标,血常规较入院第一天变化不大,但纤维蛋白原由4.95g/L下降为2.2g/L。铁蛋白高达1576ng/mL,EB病毒及CMV检测阴性。目前骨髓形态学结果提示不能除外HPS,应积极完善其他指标协助诊断。
报告回传给临床后,医生采取了甲强龙及丙种球蛋白的规律治疗。并且动态监测血常规、纤溶指标、炎症指标、生化及电解质等相关指标。经治疗一周后病情逐渐好转,患者体温恢复正常,血象逐渐正常,肝功能好转。出院后嘱咐患者继续口服醋酸泼尼松,1月内逐渐减停。
案例分析
噬血细胞综合征(HPS)又称噬血细胞性淋巴组织细胞增多征(hemophagocyticlymphohistiocytosis,HLH),是一种免疫介导的危及生命的疾病,是由于巨噬细胞过度活化、增殖,同时伴自然杀伤细胞和细胞毒性T淋巴细胞活性降低,颗粒酶依赖的细胞毒功能缺陷,进而继发免疫功能紊乱而导致的一系列临床综合征。
HPS分为原发性与继发性。原发性HPS多发生于儿童和青少年时期,少见于成人。继发性HPS多因感染、肿瘤及免疫性疾病所致。临床表现主要包括持续性高热、肝脾大及凝血功能障碍等。
近年来研究证实HPS患者存在多种基因突变,包括穿孔素1(PRF1)、Unc13同族体D(UNC3D)突触融合蛋白11(STX11)RAS致癌基因家族成员(RAB27A)溶酶体转运调节蛋白(LYST)以及最新发现的NLR家族CARD域容纳4(NLRC4)等其中以PRF1基因突变最为常见[1]。
生理情况下,机体主要通过释放穿孔素和颗粒酶对各种感染或肿瘤细胞进行杀伤。通常情况下,CD8+CTL和NK细胞识别异常靶细胞,诱导靶细胞凋亡,该过程不会产生大量的抗原刺激物。但当机体存在上述基因突变时,CTL和NK细胞功能受损,导致抗原刺激物不能及时被清除,免疫反应持续存在。活化的免疫细胞释放细胞因子继而激活巨噬细胞,最终导致单核巨噬细胞吞噬血细胞现象、炎症因子风暴、组织损伤等其他炎性反应[2]。
HPS的诊断标准:1.检测到相关的分子遗传学异常即可诊断。2.满足以下8条中的5条可以诊断:a.发热超过1周,体温>38.5℃;b.脾大;c.两系或三系降低;d.甘油三酯>3mmol/L或/和纤维蛋白原下降<1.5g/L;e.血清铁蛋白>500ug/L;f.血浆可溶性CD25>2400U/ml;g.NK细胞活性下降;h.骨髓穿刺发现噬血现象。其中以可溶性CD25及NK细胞活性最有意义,血清铁蛋白>10000ug/L时诊断的敏感性及特异性明显升高,可达90%以上[3]。
HPS一般较凶险,病情进展迅速。目前HPS的治疗主要以化疗和造血干细胞移植为主。近年来,一些靶向治疗药物逐渐进入临床并取得较好的疗效。继发性HPS的早发现,早诊断对于预后至关重要。
总 结
该病例患者以不明原因发热就诊,需要寻找不明原因发热的病因,根据一系列的检查结果排除感染性发热,风湿免疫相关疾病及明显实体肿瘤可能。基于其有前驱感染病史,中度贫血建议完善骨穿检查。
该患者目前检查结果符合HPS的诊断标准。HPS是一种多器官、多系统受累,并进行性加重伴免疫功能紊乱的巨噬细胞增生性疾病,病情进展迅速、病情凶险,应及时采取针对措施挽救患者生命。作为检验的医务人员,尤其是从事形态学的人员更需善于发现的眼睛,见微知着,善于分析与总结。
参考文献
[1]管玉洁,刘炜,宋丽丽,等.EB病毒相关性嗜血细胞综合征患儿EB病毒潜伏膜蛋白1及Th1细胞因子的表达及其意义[J].临床与病理杂志,2019(09).
[2]王昭,王天有.嗜血细胞综合征诊治中国专家共识[J].中华医学杂志,2018(02).
[3]王昭,王旖旎,冯翠翠,等.继发性嗜血细胞性淋巴组织细胞增多症57例患者的早期诊断和临床分析[J].中国内科杂志,2019(04).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言