Lancet:帕博利珠单抗联合吉西他滨和顺铂显著改善晚期胆道癌患者的总生存期
2023-07-27 daikun MedSci原创 发表于上海
该研究旨在评估帕博利珠单抗联合吉西他滨和顺铂与吉西他滨和顺铂单独治疗晚期胆道癌症患者的疗效和安全性,研究结果显示与吉西他滨和顺铂相比,帕博利珠单抗联合吉西他滨和顺铂在总生存期方面取得了显著改善。
胆道癌起源于肝内或肝外胆管和胆囊,通常预后不良,并且在全球范围内发病率不断上升。 晚期胆道癌的标准治疗方法是吉西他滨和顺铂化疗。由于大多数胆道癌具有免疫抑制的微环境,因此免疫检查点抑制剂单一疗法的客观缓解率较低。该研究的目的是评估在晚期胆道癌患者中,与单独使用吉西他滨和顺铂相比,在吉西他滨和顺铂中添加免疫检查点抑制剂的疗效和安全性。

方法:KEYNOTE-966 是一项在全球 175 个医疗中心进行的随机、双盲、安慰剂对照 3 期试验。纳入患者年龄为 18 岁或以上;既往患有未经治疗、不可切除、局部晚期或转移性胆道癌;根据实体瘤疗效评价标准RECIST 1.1 版,患有可测量的疾病;东部肿瘤合作组表现状态为 0 或 1。 符合条件的参与者被随机分配 (1:1) 接受帕博利珠单抗 200 mg 或安慰剂,两者均每 3 周静脉注射一次(最多 35 个周期),并与吉西他滨(1000 mg/m 2)联合用药每 3 周在第 1 天和第 8 天静脉注射; 无最长持续时间)和顺铂(25 mg/m 2每三周在第 1 天和第 8 天静脉注射; 最多 8 个周期)。主要终点是在意向治疗人群中评估的总体生存期。次要终点为在接受治疗的人群中评估的安全性。
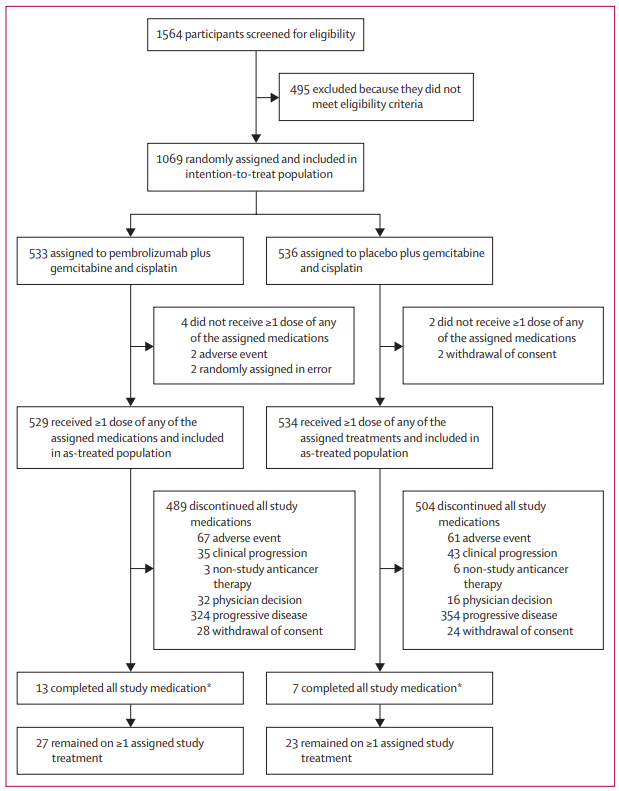
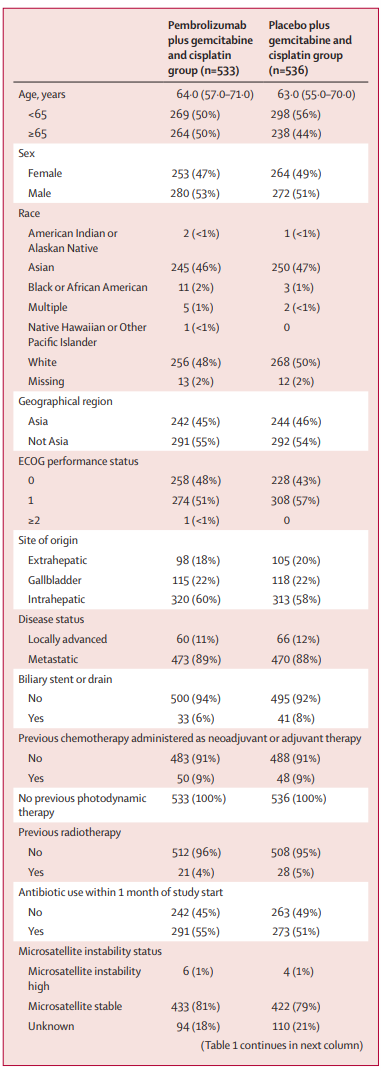
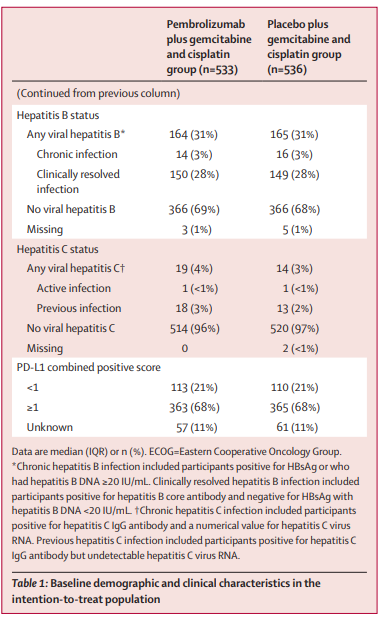
研究结果:在2019年10月4日至2021年6月8日期间,1564名患者接受了资格筛选,其中1069人被随机分配到帕博利珠单抗组加吉西他滨和顺铂组(帕博利珠单抗组;n=533)或安慰剂加吉西他滨和顺铂(安慰剂组;n=536)。最终分析的中位研究随访时间为25.6个月(IQR 21.7-30.4)。帕博利珠单抗组的中位总生存期为12.7个月(95%CI 11.5-13.6),而安慰剂组为10.9个月(9.9-11.6)(危险比0.83[95%CI 0.72-0.95];单侧p=0.034[显著性阈值,p=0.0200])。
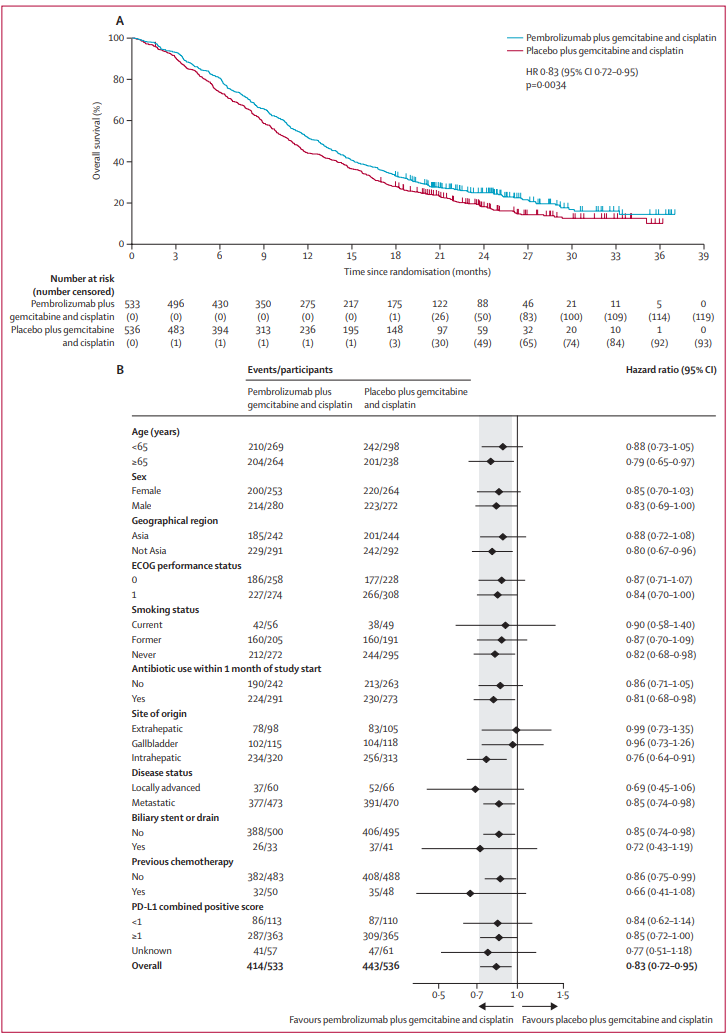
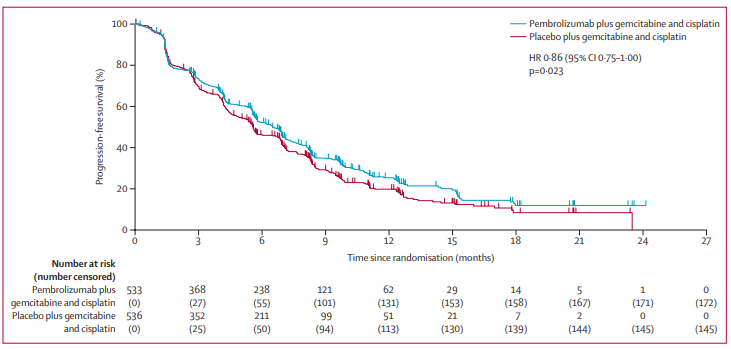
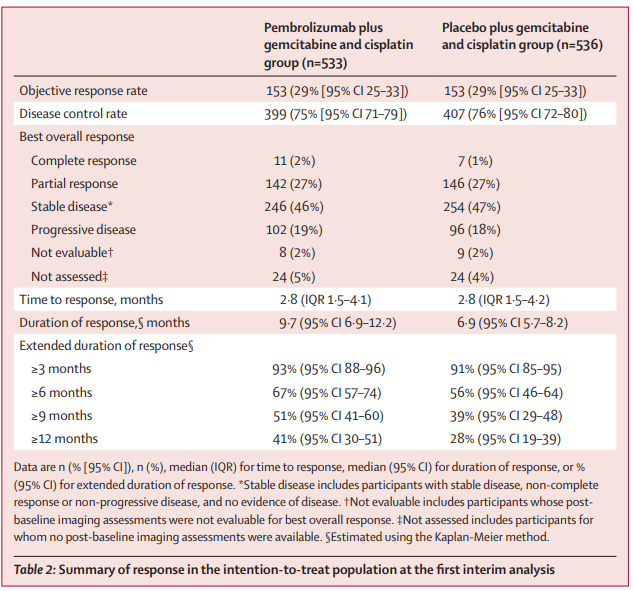
安全性分析:在接受治疗的人群中,帕博利珠单抗组529名参与者中的420人(79%)和安慰剂组534人中的400人(75%)的最大不良事件等级为3-4级;帕博利珠单抗组的369名(70%)参与者和安慰剂组的367名(69%)参与者出现了最高级别为3至4级的治疗相关不良事件。帕博利珠单抗组31名(6%)参与者和安慰剂组49名(9%)参与者死于不良事件,其中帕博利珠单抗组8名(2%)和安慰剂组3名(1%)参与者死于治疗相关不良事件。
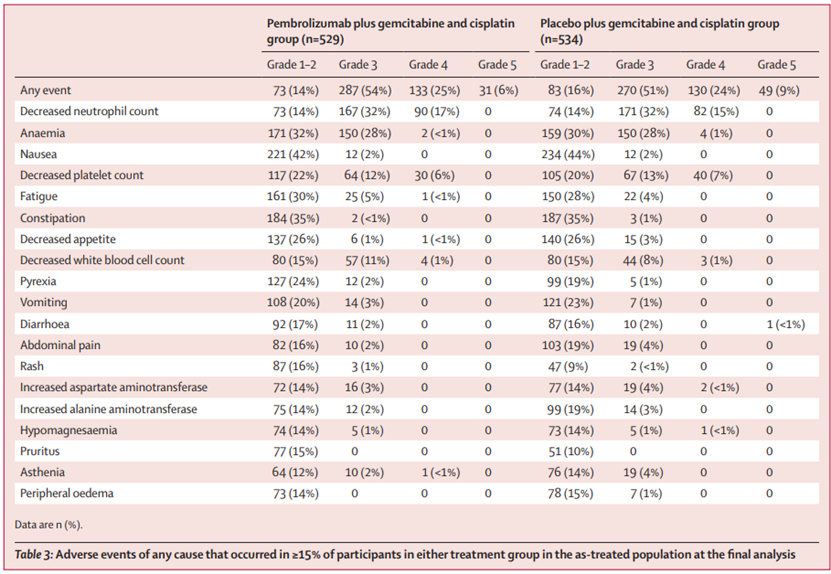
结论:与吉西他滨和顺铂相比,在没有任何新的安全信号的情况下,帕博利珠单抗联合吉西他滨和顺铂在总生存期方面取得了统计学上显着的、有临床意义的改善,因此可能成为先前未经治疗的转移性或不可切除的胆道癌患者的新治疗选择。
原始出处:
Kelley RK, et al. 2023. Pembrolizumab in combination with gemcitabine and cisplatin compared with gemcitabine and cisplatin alone for patients with advanced biliary tract cancer (KEYNOTE-966): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 401:1853-1865.DOI: 10.1016/s0140-6736(23)00727-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言