AACR 2020:豪森药业阿美替尼用于EGFR突变耐药的NSCLC患者结果公布
2020-04-28 MedSci MedSci原创
3月底,国家药监局通过优先审评审批程序附条件批准1类创新药甲磺酸阿美替尼片(商品名:阿美乐)上市,用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测
3月底,国家药监局通过优先审评审批程序附条件批准1类创新药甲磺酸阿美替尼片(商品名:阿美乐)上市,用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌成人患者。
在4月27日举行的“II期临床试验专场(Phase II Clinical Trials)”上,豪森药业公布了自主研发1类创新药阿美乐®(甲磺酸阿美替尼片)最新临床研究结果。
此次AACR年会上,陆舜教授公布了阿美替尼II期临床试验随访至2019年8月1日的疗效和安全性数据,并首次公布了脑转移患者的疗效数据。数据显示,中位随访时间11.4个月时,阿美替尼二线治疗经治EGFR T790M突变阳性NSCLC患者疗效确切。经独立评审委员会评估,阿美替尼在脑转移患者中,疗效与总人群相仿。随着随访时间的延长,阿美替尼的长期安全性得到了进一步的验证,其不良事件发生率低,无间质性肺炎的发生,安全性良好。
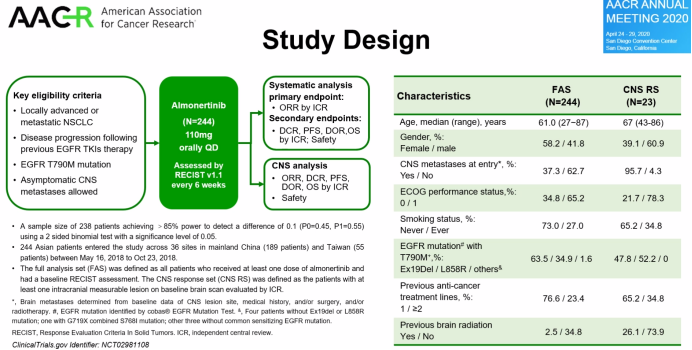
阿美替尼II期研究(APOLLO)共入组244例经一、二代EGFR-TKI治疗后出现疾病进展,并且经检验确认存在EGFR T790M突变阳性的NSCLC患者。此前结果显示,总人群的ORR为68.9%,DCR为93.4%,中位PFS为12.3个月,中位DOR为12.4个月。脑转移疗效评估,ORR为60.9%,DCR为91.3%,中位PFS为10.8个月,中位DOR为11.3个月。从瀑布图来看,总人群及脑转移亚群的疗效相似。
基线数据显示,本研究共纳入37.3%(91例)的无症状脑转移患者,其中23例脑转移患者经研究者判断基线有颅内靶病灶,组成CNS分析组。
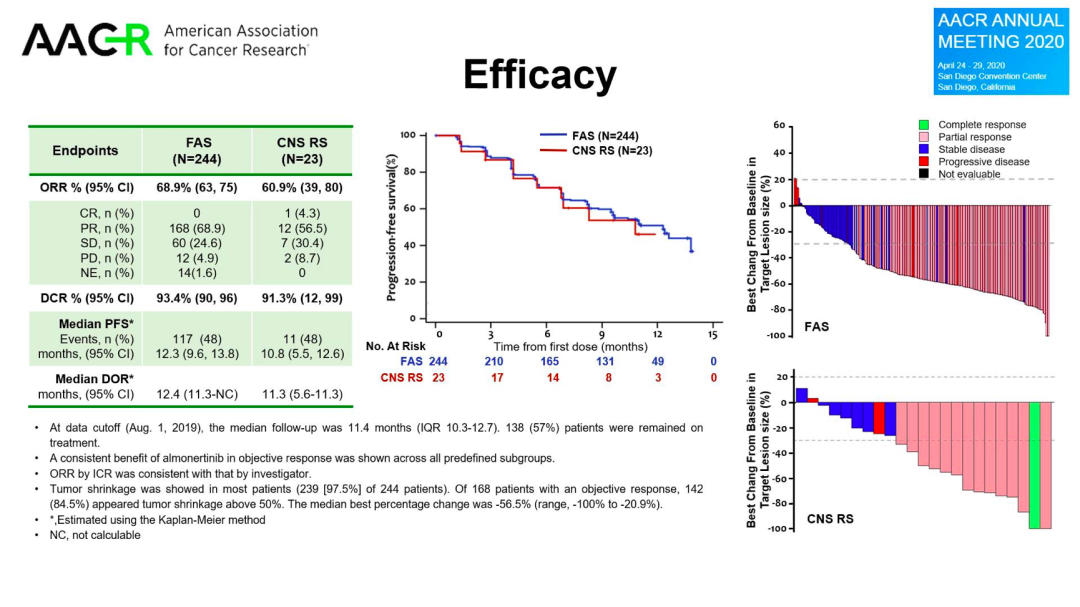
数据显示,中位随访时间11.4个月时,阿美替尼二线治疗经治EGFR T790M突变阳性NSCLC患者疗效确切。经独立评审委员会评估,阿美替尼在脑转移患者中,疗效与总人群相仿。随着随访时间的延长,阿美替尼的长期安全性得到了进一步的验证,其不良事件发生率低,无间质性肺炎的发生,安全性良好。
阿美替尼作为首个上市的国产第三代EGFR-TKI,展现了不错的入脑能力,后续可期。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#结果公布#
74
#AACR 2020#
68
#SCLC患者#
65
#豪森药业#
67
#ACR#
66
#NSCLC患者#
57
#GFR#
76
#AACR#
66
NSCLC下一步突破在于新靶点了,靶向治疗和免疫治疗基本见顶了,再有新的就需要新机制了
68