EMA开始审查MorphoSys的CD19单抗tafasitamab,治疗淋巴瘤
2020-05-22 MedSci原创 MedSci原创
如果获得批准,tafasitamab可能会对诺华和吉利德的CAR-T疗法带来挑战。
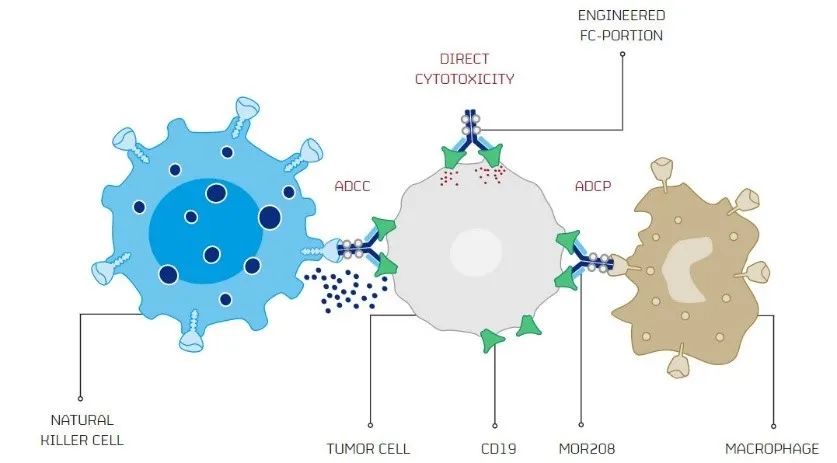
欧洲药品管理局(EMA)开始对MorphoSys靶向CD19的单抗tafasitamab(MOR208)进行审查,如果获得批准,可能会对诺华和吉利德的CAR-T疗法带来挑战。
美国监管机构接受了MorphoSus及其合作伙伴Incyte的tafasitamab的市场营销申请,用于治疗不适合干细胞移植的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)成年患者。
2期L-MIND研究结果表明,将tafasitamab与Celgene的Revlimid(来那度胺)联合治疗后患者的总体缓解率为60%,包括43%的完全缓解率。
诺华的Kymriah(tisagenlecleucel)和Gilead的Yescarta(axicabtagene ciloleucel)CAR-T疗法治疗前,需要服用大剂量化疗药物,很多患者(尤其是老年人)的体力不足以耐受该疗法。
DLBCL是全世界成年人中最常见的非霍奇金淋巴瘤(NHL),占所有病例的40%,并且是一种非常具有侵略性的疾病--大约30-40%的患者对初始治疗或复发无反应,这意味着对新疗法的迫切需求。
原始出处:
http://www.pmlive.com/pharma_news/ema_starts_review_of_morphosys_tafasitamab_for_lymphoma_1340717
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#tafasitamab#
78
#SIT#
88
#FAS#
81
#ASIT#
70
#mAb#
61
#EMA#
70
#CD19#
110
#CD19单抗tafasitamab#
71