【衡道丨病例】病理诊断——胃ESD标本内翻性息肉
2024-04-09 衡道病理 衡道病理 发表于上海
本次就由广州医科大学附属番禺中心医院病理科陈芳老师为大家带来一例罕见病例——胃ESD标本发现内翻性息肉的病例分享。
胃息肉是内镜诊断经常遇到的疾病,它是一组异质性的上皮和上皮下病变(SELs),分为肿瘤性的和非肿瘤性的,每种都有独特的组织学形态、恶变潜能和处理方式。而胃内翻性息肉是一种罕见的胃息肉,它的独特特征是上皮性的黏膜成分呈内生方式向黏膜下生长,形成黏膜下息肉。
本次就由广州医科大学附属番禺中心医院病理科陈芳老师为大家带来一例罕见病例——胃ESD标本发现内翻性息肉的病例分享。
病例资料
女,38岁,体检发现胃体隆起肿物性质待查1周余入院,胃镜下胃体见一直径8mm的半球形息肉样隆起,顶端似一个针样开口,放大内镜结合窄带成像(magnifying endoscopy-Narrow Band Imaging,ME-NBI)下边界明显,表面不规则,隐窝边缘上皮(Marginal crypt epithelium,MCE)弧形、延长,微血管大小不等、增宽。
无痛超声胃镜显示椭圆形高回声灶,起源于黏膜层,局部层次较清楚。
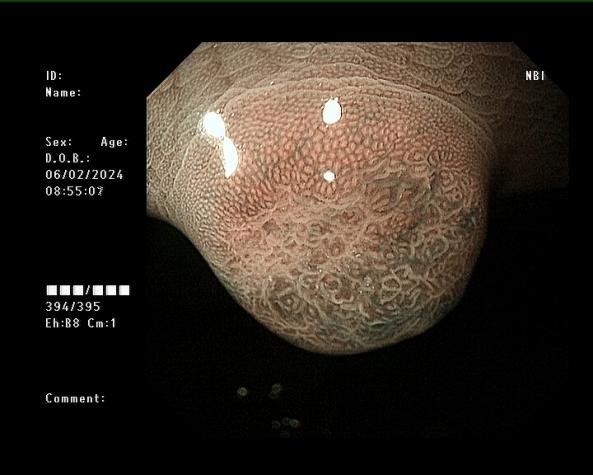
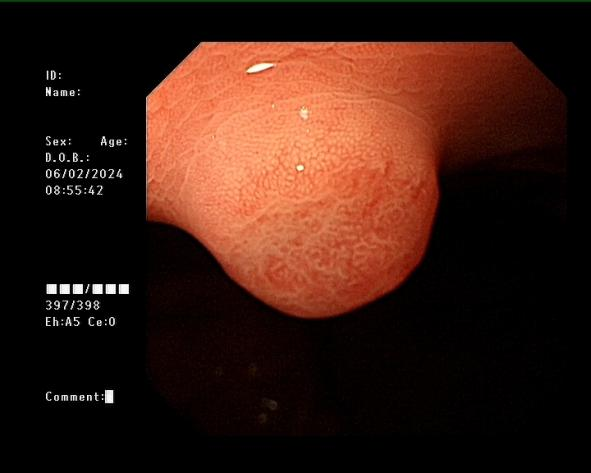
图1、图2 内镜下胃黏膜病变所见。
患者行内镜下胃黏膜下剥离术[ESD]。
病理大体所见:
(胃体)ESD胃黏膜组织一块, 2.0x1.5x0.1CM,表面见一0.5x0.5x0.2CM突起,切面灰白、实性、质中。由口侧至肛侧依次切开全取。
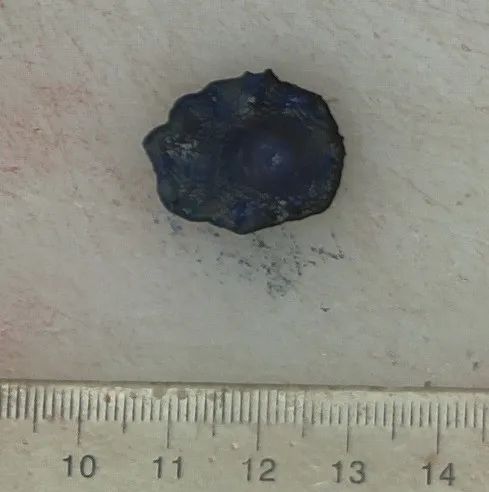
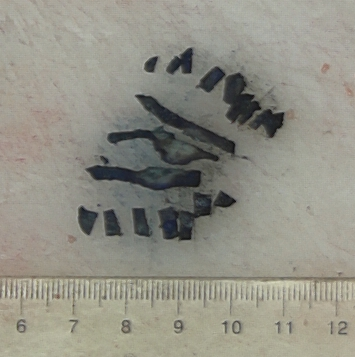
图3、图4 胃黏膜病变病理大体所见。
病理形态镜下表现:
镜下所见:
送检组织病变界限清晰,可见黏膜突向黏膜下层生长,中央开口,似烧瓶样结构,黏膜保存正常胃黏膜结构,中央胃小凹上皮增生,胃底腺在外周,薄平滑肌束在最外层,部分胃底腺增生、扩张。
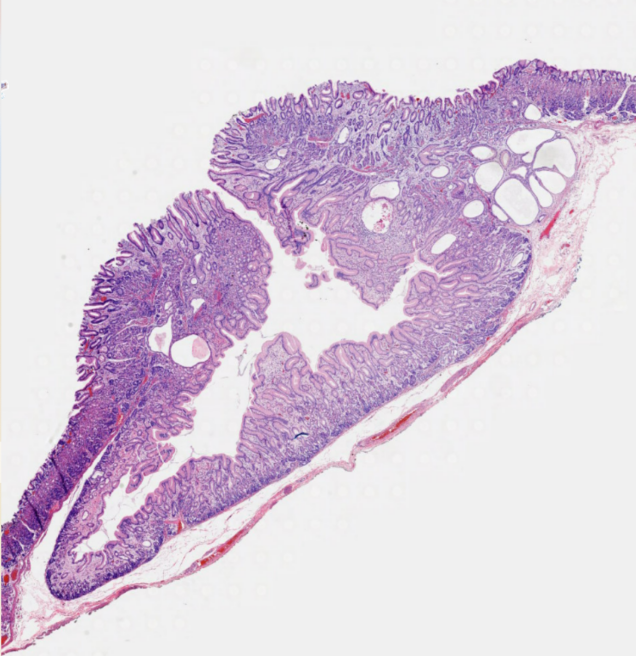
图5 胃黏膜病变HE镜下形态。

图6 胃黏膜病变HE镜下形态。
免疫组化

图7 胃黏膜病变免疫组化MUC5AC
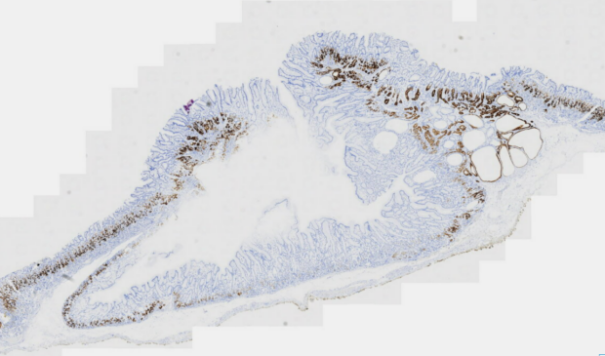
图8 胃黏膜病变免疫组化MUC6
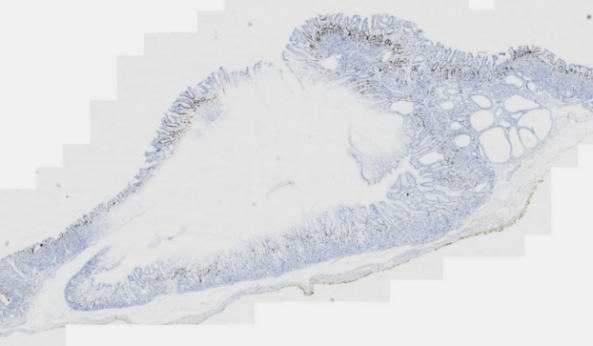
图9 胃黏膜病变免疫组化Ki-67
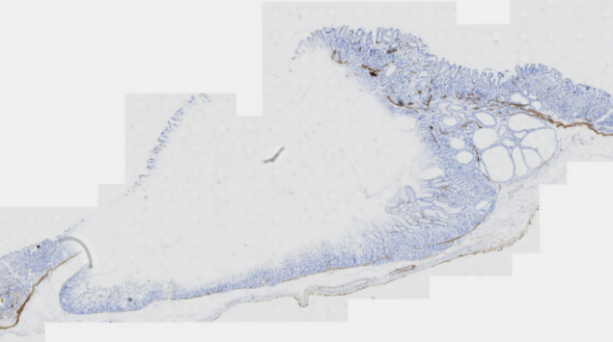
图10 胃黏膜病变免疫组化Desmin
免疫组化结果:
MUC5AC(胃黏膜表面上皮+),MUC6(胃底腺+),Ki-67(约20%+),Desmin(黏膜肌层+)。
病理诊断
病理诊断结果:(胃体)结合形态学及内镜所见,符合胃内翻性增生性息肉,该形态罕见,建议随访。
胃内翻性息肉
一、概述
胃息肉是内镜诊断经常遇到的疾病,它是一组异质性的上皮和上皮下病变(SELs),分为肿瘤性的和非肿瘤性的,每种都有独特的组织学形态、恶变潜能和处理方式。大多数胃息肉是起源于黏膜的上皮源性性病变,在内镜下表现为腔内突起,病理上分为胃底腺息肉、增生性息肉、腺瘤性息肉和错构瘤性息肉。上皮下起源的胃息肉相对少见,内镜下通常表现为圆形隆起,被覆胃黏膜外观正常,病理包括多种类型,如神经内分泌肿瘤、间充质肿瘤和异位所致的病变。
胃内翻性息肉(Gastric Inverted Polyps,GIPs)是一种罕见的胃息肉,它的独特特征是上皮性的黏膜成分呈内生方式向黏膜下生长,形成黏膜下息肉。既往认为它是异位或错构瘤,曾用术语:孤立性息肉性错构瘤、幽门腺异常异位、不寻常的黏膜下息肉等,目前常用:内翻性增生性息肉、错构瘤性内翻性息肉,他们统称为胃内翻性息肉。由于其内生生长的黏膜固有成份形态多变,给准确诊断带来挑战。
二、临床特点
-
发生年龄:23岁-87岁(平均55岁左右)。
-
男比女多(男性占66.7%)。
-
发生部位:绝大多数位于胃体,偶见胃底、胃窦部,多为单灶。
-
肿瘤大小:比一般的胃息肉稍微大一些,平均为14.9mm(10mm-25mm)。
-
内窥镜表现:息肉82%无蒂、18%有蒂,被覆黏膜正常。黏膜表面改变有:充血隆起,糜烂、凹陷、孔口渗出黏液。
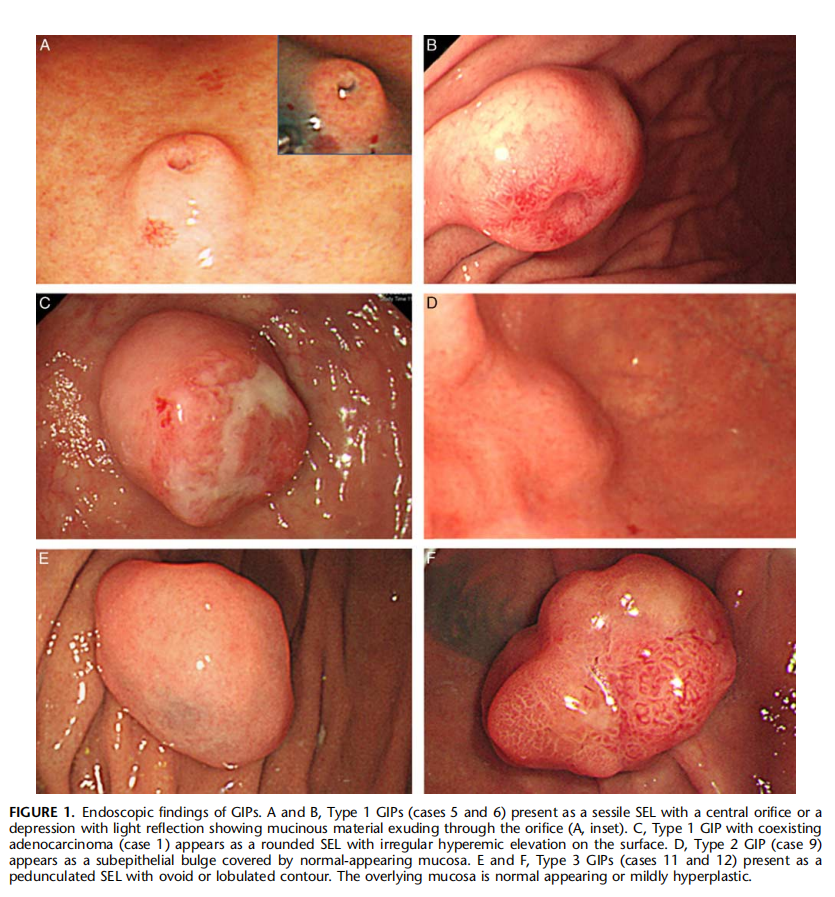
图11:A、B:1型GIP有中央孔口或凹陷,显示孔口渗出黏液;C:1型GIP与腺癌共存,表现为圆形病变,表面不规则隆起;D:2型GIP表现为正常黏膜覆盖的上皮下隆起;E 、F:3型GIP形状不规则,有分叶状轮廓,表面黏膜正常或轻度增生。
三、病理特征
GIPs位于黏膜下层,界限清楚,大部分或完全被黏膜覆盖,由胃型腺上皮和平滑肌组成,结构与正常黏膜相似,或明显扭曲变形。腺体成分包括胃小凹上皮、幽门腺或胃底腺,很少有肠嗜铬细胞样细胞,平滑肌束环绕病灶外侧或周围有分叶状的腺体簇。根据与黏膜表面是否交通、平滑肌边界及组织结构模式将GIP分为1型、2型、3型,其特点分别为:
1型GIP:
约占50%,与上覆胃黏膜有交通,平滑肌边界清晰,组织结构完整。病变区整个黏膜向黏膜下倒置,周围有与邻近黏膜肌层相连的平滑肌束,并有中央扩张的导管状或裂隙状结构,开口入管腔,低倍镜显示病变类似于一个圆形花瓶。高倍镜:倒置的黏膜保存正常胃黏膜结构,中央小凹上皮增生、幽门腺或胃底腺在外周,薄平滑肌束在最外层;中央交通结构与内镜中央孔口或凹陷结构相对应。
-
内镜:黏膜下隆起,可见中央孔状结构,黏膜与正常黏膜相似。ME-NBI下边界明显,表面不规则,MCE弧形、延长,微血管大小不等、增宽。
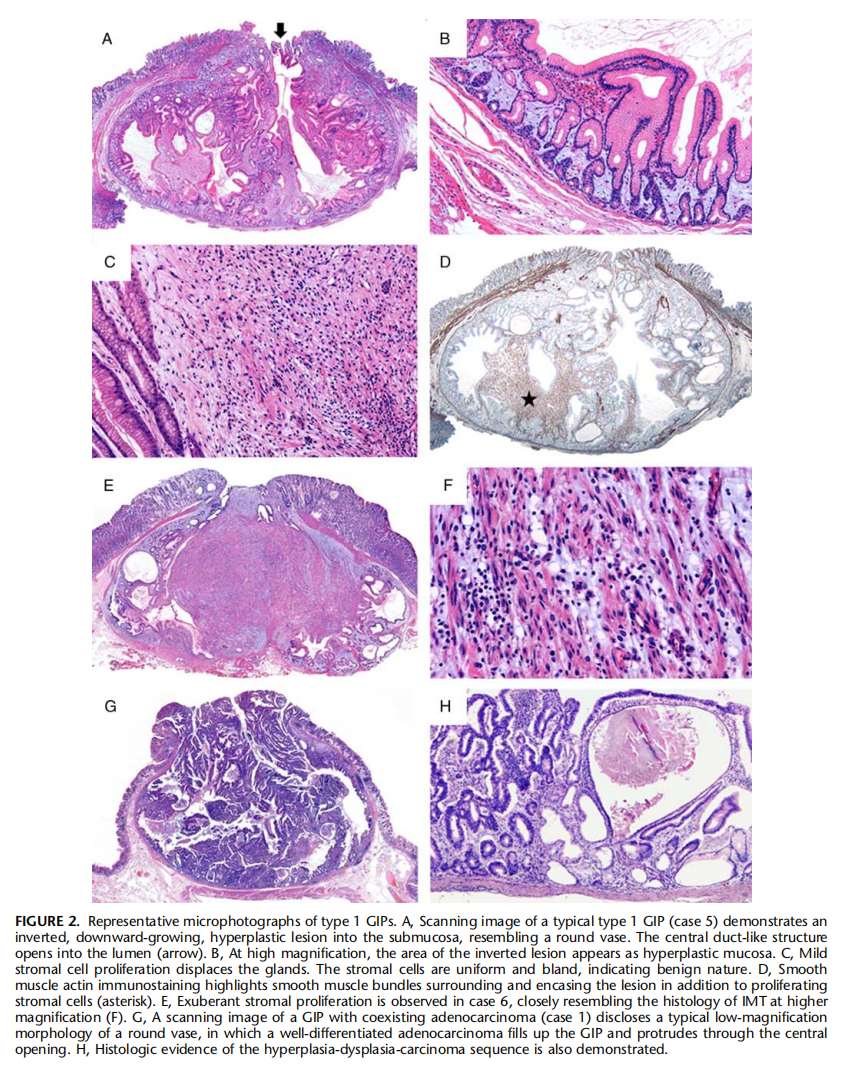
图12:典型的1型GIP镜下改变。A:1型GIP低倍镜显示一个倒置向黏膜下层生长的增生性病变,类似瓶子。中心瓶口状结构进入囊腔(黑色箭头)。B:高倍镜下病变倒置区域表面黏膜增生性改变。C:间质轻度增生而腺体减少。间质细胞淡染,形态温和,显示良性。D:SMA免疫组化染色突出显示病变周围和包裹的平滑肌束,以及增生的间质细胞(星号)。E,在病例6中观察到间质细胞增生旺盛,与高倍镜下IMT(炎性肌纤维母细胞瘤)的组织学非常相似(F)。G,一个与GIP共存的腺癌(病例1)的扫描图像显示了一个典型的圆形花瓶的低倍镜形态,其中一个高分化腺癌填充了GIP,并通过中央开口突出囊腔外。H,也有增生-非典型增生-癌渐变的组织学证据。
2型GIP:
约占33%,表现为孤立的黏膜下病变,被平滑肌束包围,没有中央交通结构。高倍镜:病变包括小凹上皮、幽门腺或胃底腺以及周围的平滑肌,形似分化良好的胃黏膜。病变周围出现囊肿结构,囊肿位于黏膜下层,内衬单层柱状上皮,类似深在性囊性胃炎,但它们被复杂的腺体包围,并与主病变合并。
-
内镜:黏膜下隆起,但是黏膜完整。
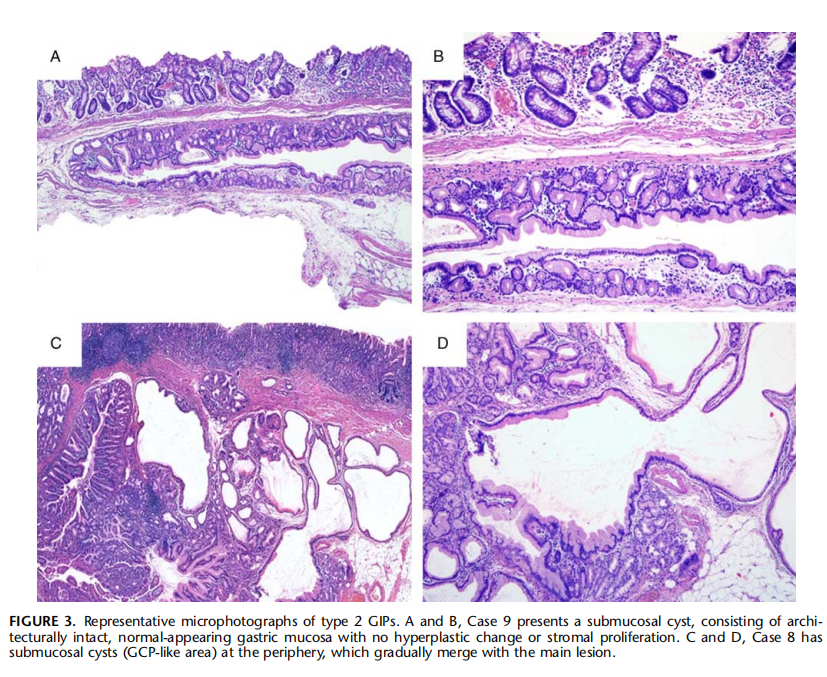
图13:2型GIPs的典型图像。A和B:病例9表现为黏膜下囊肿,由结构完整、外观正常的胃黏膜组成,没有增生性改变或间质增生。C和D,病例8在周围有黏膜下囊肿(GCP样区),并逐渐与主病变合并。
3型GIP:
无黏膜交通结构及平滑肌边界,组织结构明显扭曲,被覆黏膜完整。由富含黏蛋白的囊肿、增生的腺体和平滑肌构成,排列成类圆形或小叶状结构。囊肿内衬单层黏液上皮,周边围绕复杂的腺体、平滑肌结构,病变集中在黏膜下层,可延伸至黏膜深层。
-
内镜:有蒂息肉,表面黏膜完整。
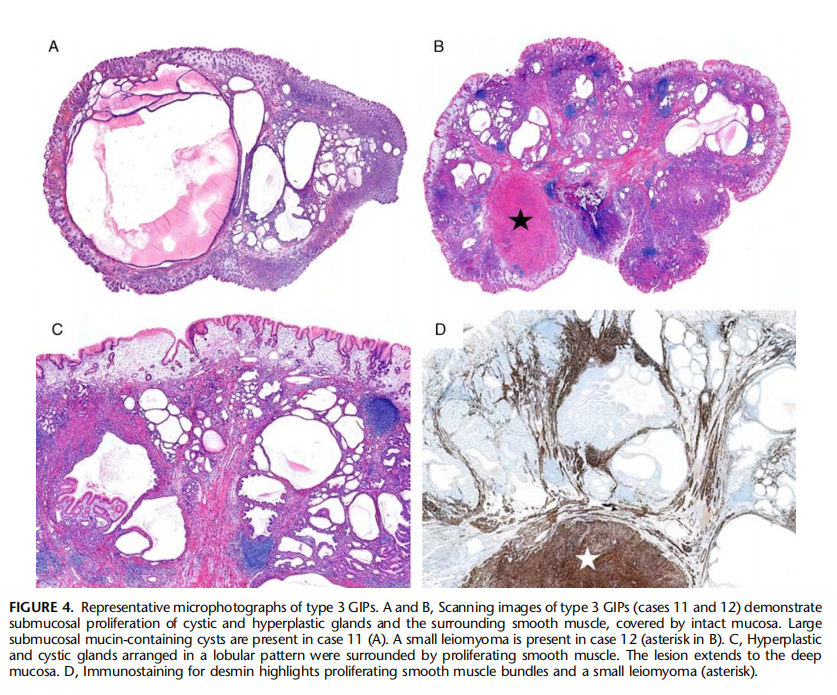
图14:3型GIP的典型图像:A和B:3型GIP(病例11、12)的扫描图像显示囊性、增生性腺体及周围平滑肌,被完整的黏膜覆盖。病例11 (A).中存在大的黏膜下黏蛋白囊肿病例12为一个小的平滑肌瘤(B中为星号)。C、增生性和囊性腺体被增生的平滑肌包围。病变延伸到黏膜深层。D,Desmin免疫组化染色显示增生的平滑肌束和一个小的平滑肌瘤(星号)。
四、治疗
1型GIP是具有腺癌发展潜能的癌前病变,也可伴发腺癌,建议完全切除,无论肿瘤大小。一般采用ESD或楔形切除术,切除边缘应保证阴性,随访无复发或转移迹象。
五、鉴别诊断:
GIP的鉴别诊断取决于其组织亚型。
1型GIP有中央管结构和分化好的平滑肌边界,很容易区分其他常见的黏膜下病变。
2型GIP没有特征性沟通结构,难以与深在性囊性胃炎和胃腺肌瘤区分:
1、深在性囊性胃炎是一种罕见的黏膜下病变,组织学上,它由囊性腺体组成,囊性腺体内衬黏液上皮,可轻度增生,有或没有固有层边缘,缺乏各种腺体或发达的平滑肌。
2、胃腺肌瘤,被称为流产变异型或III型胰腺异位,因为在内镜下,它表现为具有中央凹陷的黏膜下病变,类似于一些具有中心孔或凹陷的1型GIP。然而,胃腺肌瘤主要发生在胃远端(胃窦或幽门),是由平滑肌包裹的Brunner型上皮的异位导管结构,它们没有胃型腺体,这与GIP不同。
3型GIP鉴别诊断包括错构瘤性息肉,特别是幼年型息肉或peutz-jeghers息肉(PJP):
1、幼年型息肉的特征是多个含黏蛋白的囊肿,常伴有表面溃疡和肉芽组织形成,没有平滑肌增生;
2、PJP以平滑肌、腺体分别增生为特征,与3型GIP相似;
然而,PJP的平滑肌增生经常以树形模式延伸到中央凹上皮。最重要的是,与内生性生长的GIPs相比,错构瘤性息肉是外生性生长的上皮性病变。
参考书籍及文献:
[1]Kamata Y, Kurotaki H, Onodera T, et al. An unusual heterotopia of pyloric glands of the stomach with inverted downgrowth. Acta Pathol Jpn. 1993;43:192-197.
[2]Kim J Y, Ahn S, Kim K M, et al. Gastric inverted polyps—distinctive subepithelial lesions of the stomach: clinicopathologic analysis of 12 cases with an emphasis on neoplastic potential[J]. The American journal of surgical pathology, 2021, 45(5): 680-689.
[3]Ng H I, Li Z Q, Zhang Y M, et al. Gastric inverted hyperplastic polyp, an exceptional case diagnosed after endoscopic submucosal disp[J]. Clinics and Research in Hepatology and Gastroenterology, 2022, 46(4): 101890.
[4]李常娟,徐瑞,李鹏. 不同内镜表现的胃错构瘤性内翻性息肉三例[J]. 中华消化内镜杂志,2020,37(5):369-371. DOI:10.3760/cma.j.cn321463-20191031-01029.
[5]化宏金,吴靓,李可栋,等. 胃型内翻性增生性息肉临床病理学特征分析[J]. 中华病理学杂志,2022,51(8):749-751. DOI:10.3760/cma.j.cn112151-20220117-00039.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#ESD# #胃息肉# #内翻性息肉#
91