新进展!中山大学团队研究发现晚期实体瘤治疗新方案
2023-06-18 转化医学网 转化医学网 发表于上海
目前,外周血单核细胞衍生的新抗原特异性CD8 + T细胞(Neo-T)治疗的最佳淋巴细胞耗竭强度尚未确定。
6月10日,中山大学徐瑞华教授团队等在《Nature Communications》上在线发表研究论文“A pilot study of lymphodepletion intensity for peripheral blood mononuclear cell-derived neoantigen-specific CD8 + T cell therapy in patients with advanced solid tumors”,研究表明没有淋巴细胞耗竭的Neo-T疗法可能是治疗晚期实体瘤的安全且有前途的方案。

https://www.nature.com/articles/s41467-023-39225-7
研究背景
过继性T细胞疗法(ACT)正在成为癌症患者的首选治疗选择。这包括嵌合抗原受体(CAR) T 细胞、T 细胞受体(TCR)T 细胞和肿瘤浸润淋巴细胞(TIL)的过继转移。许多临床研究表明,新抗原特异性肿瘤浸润淋巴细胞(TIL)的过继转移可以介导几种类型的实体瘤的持久消退。然而,收集TIL需要对肿瘤组织进行侵入性取样,并且通常受到切除肿瘤组织相对较小的尺寸的限制,而且一些肿瘤部位也不容易到达。最近,几项研究报告说,在癌症患者的外周血中发现了识别新抗原的T细胞克隆,外周血淋巴细胞(PBL)中的T细胞可以识别与TIL相同的P53新抗原。因此,PBL可能是T细胞的可靠且无创的来源,用于开发新抗原靶向ACT疗法来治疗癌症患者。
非清髓性淋巴细胞耗竭常在ACT之前用于抑制宿主免疫系统以降低免疫原性,增加IL2,IL7,IL15等的可用性,减少调节性T细胞,并增加输注T细胞的持久性。氟达拉滨和环磷酰胺是淋巴细胞耗竭化疗最常用的药物。然而,淋巴细胞耗竭也可导致神经毒性、中性粒细胞减少、贫血和更大的感染风险。目前,淋巴细胞耗竭的给药强度在不同的中心和临床试验中差异很大,并且由于T细胞产物的特异性,还没有针对淋巴细胞耗竭的标准化方案。
研究进展
在研究中,我们开发了一种从患者的外周血单核细胞中产生个性化Neo-T(新抗原特异性CD8 + T细胞)的方法。我们建立了一个管道,包括通过生物信息学分析进行新抗原预测,并在25天内对T细胞进行大规模新抗原特异性扩增。为了评估Neo-T治疗的临床疗效并确定Neo-T治疗的最佳淋巴细胞耗竭强度,我们对Neo-T疗法进行了首次人体研究,氟达拉滨和环磷酰胺的剂量递增。这项研究被设计为一项开放标签的I期临床试验(NCT02959905),包括标准治疗难治的局部晚期或转移性实体瘤患者。
在研究中,我们发现PBMC可以在所有患者中成功产生Neo-T,并识别出几种预测的新抗原。尽管以4.78e7至9.0e8之间的相对小剂量输注,但Neo-T治疗显示出有希望的33%ORR,与TIL/TCRT疗法相当,后者输注的T细胞数量通常在1e10至1e11的范围内。出乎意料的是,未进行淋巴细胞耗竭化疗的患者组的临床反应最佳。
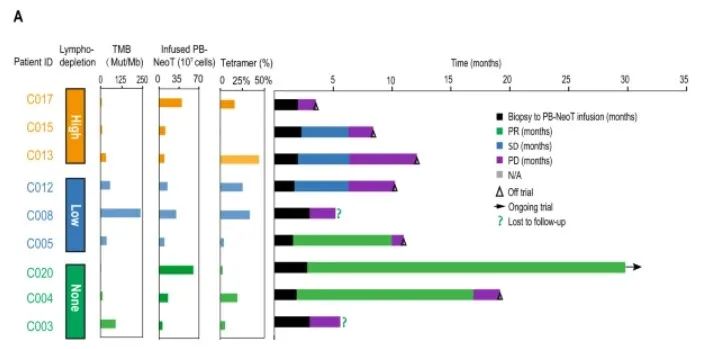
Neo-T产品的特点,患者特征和每位患者的治疗结果
一种合理的解释是,LD化疗在体内为Neo-T的增殖和激活创造了不利的微环境。因此,在没有LD化疗的情况下,较少数量的Neo-T可以获得与其他过继性T细胞转移研究相当的临床反应,LD化疗和更多的T细胞给药。虽然我们的研究结果表明LD化疗可减少淋巴细胞计数,抑制和延缓新抗原特异性TCR克隆的扩增,并表明LD可能会降低Neo-T治疗的疗效,但其他因素也可能影响结果。例如,患者特征、肿瘤微环境、新抗原的免疫原性以及注入的新抗原特异性 Neo-T 细胞数量的差异都可能影响结果。受当前研究规模的限制,我们无法调查所有这些变量的影响,也无法将我们的发现推广到更大的人群。因此,未来有必要进行更大样本量的研究,以更好地了解淋巴细胞耗竭对Neo-T治疗反应的影响。
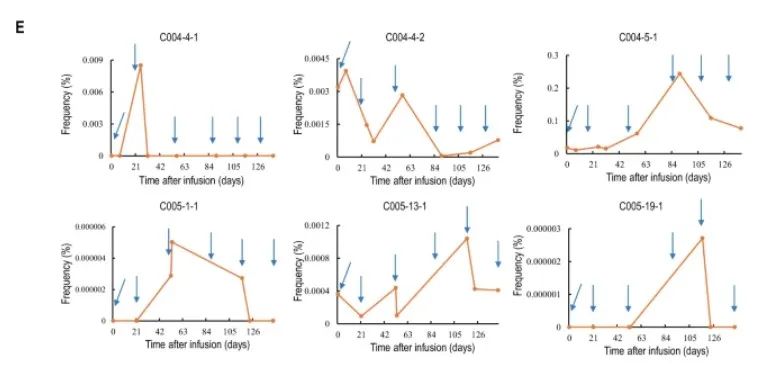
Neo-T治疗期间患者C004和C005外周血中几种代表性新抗原特异性TCR克隆的频率。
研究意义
本研究表明,在Neo-T治疗期间,从无淋巴细胞耗竭到高剂量治疗,不同的淋巴细胞耗竭剂量耐受性良好。Neo-T疗法在晚期实体瘤患者中显示出有希望的临床疗效,ORR为33.3%(3/9),DCR为66.7%(6/9)。与高强度组相比,无淋巴细胞耗竭组在 Neo-T 治疗期间出现 PR 的患者更多。在两名有反应的患者中检查新抗原特异性 TCR,并在淋巴细胞耗竭治疗后显示延迟扩张。
综上所述,研究表明从外周血淋巴细胞中过继转移Neo-Ts在各种淋巴细胞耗竭方案中是安全的,并且能够在不进行淋巴细胞耗竭化疗的情况下介导持久的肿瘤消退。
参考资料:
https://www.nature.com/articles/s41467-023-39225-7
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言