三维成像技术在心脏再同步化治疗中的应用
2012-01-01 杨水祥 北京世纪坛医院
摘要:心脏再同步化治疗能改善心力衰竭患者的临床症状及预后。然而,研究表明,约40%的病人对这种治疗的反应较差。确定心脏再同步化治疗效果的三个主要因素是:左心室收缩不同步,左心室电极的位置, 心肌疤痕组织的部位范围。二维超声心动图是第一个用来评估心脏再同步化治疗病人的成像技术。然而,三维成像技术可以更全面的评价这些患者心脏再同步化治疗前后病理生理的改变及其效果。 关键词:心力衰竭;再同步化治疗;三维
摘要:心脏再同步化治疗能改善心力衰竭患者的临床症状及预后。然而,研究表明,约40%的病人对这种治疗的反应较差。确定心脏再同步化治疗效果的三个主要因素是:左心室收缩不同步,左心室电极的位置, 心肌疤痕组织的部位范围。二维超声心动图是第一个用来评估心脏再同步化治疗病人的成像技术。然而,三维成像技术可以更全面的评价这些患者心脏再同步化治疗前后病理生理的改变及其效果。
关键词:心力衰竭;再同步化治疗;三维成像技术
前言:心脏再同步化治疗(CRT)能改善心力衰竭患者的临床症状、左心室收缩压(LV),心脏功能和长期预后[1]。然而,许多研究表明,30%到40%的患者心衰未改善[2-4]。目前心脏再同步化治疗的纳入标准是基于纽约心脏病协会(NYHA)功能分类III-IV级,LV射血分数(LVEF)< 35%,和QRS波群时限> 120毫秒的患者,这些似乎仍然不能精确确定哪些病人将会受益。目前已经发现决定CRT治疗反应的三个主要病理生理学证据:LV收缩不同步[5],心肌疤痕组织的部位范围[6]及LV电极的位置[7,8]。二维超声心动图(2 D)是第一个评估CRT患者的成像技术[9]。然而,三维(3 D)成像技术已经证明了他们在选择心衰患者CRT治疗中的价值和作用,并提供了综合评价CRT治疗的病理学机制方法[10-12]。本文综述了三维超声心动图、心脏磁共振(CMR)成像、核素心脏影像学和多排计算机X线心脏断层扫描(MDCT)选择CRT患者的重要作用。
三维成像评价左心室不同步
目前的指南在CRT植入前强调QRS间期评价[13,14]。然而,心脏的电重构即基线QRS时限与CRT植入后的临床症状改善或超声心动图终点之间缺乏直接相关关系。15242例宽QRS心力衰竭患者CRT植入后6个月的随访显示,基线QRS间期与患者临床反应的百分比之间没有直接相关[15]。QRS间期大于等于163毫秒预测CRT临床疗效的敏感和特异性(两者均为53%)欠佳。根据这些结果,越来越多的研究集中于心脏机械不同步预测CRT治疗获益的准确性方面。利用不同的心脏成像技术,得到心脏机械不同步的结果将具有重要的预测价值[9]。从三个层面上能确认心脏的不同步:心房心室不同步,左右心室之间不同步,及左室内部不同步。这三部分构成了一个独立预测CRT反应和长期结果的体系。二维超声心动图一直被用来评价LV力学方面的不同步(例如,室间隔与左室后壁内向运动的时间差,如峰收缩速度的时间差) [16]。然而,为了获得评价整体左室收缩不同步的独特价值参数,3 D心肌成像技术,即三维超声心动图、核素成像和心脏核磁共振已成为评估左室不同步很有价值的影像方法,和预测对CRT治疗反应的技术手段。此外,初步的经验证明多排螺旋CT在评估LV收缩不同步方面也非常有价值[17]。
三维超声心动图
三维超声心动图可以通过三平面组织同步成像(triplane tissue synchronization imaging)、实时三维超声心动图和3 D斑点示踪心肌应变成像来评估LV不同步[11,18]。
三平面组织同步成像技术是评价心动周期中左心室12个阶段心肌组织运动时差(6个基底段,6个中间段)的组织多普勒成像技术。左心室12个阶段的峰收缩速度时间标准差(Ts-12-SD)被用来评估左室的不同步。此外,后续处理软件也提供了一个色彩编码的心肌基底段和中间段峰收缩速度时差的重建牛眼图,来确定心脏机械运动的最晚点(图1)。几个研究已经证实了这种方法评估左室不同步的准确性。Ts-SD-12 ≥ 33ms能显著预测CRT治疗6个月后的心脏逆重构(左心室收缩末期容量减少≥15%),其预测的敏感性为90%,特异性为83%[11,19] 。
此外,实时3 D超声心动图也提供了一个基于整个心动周期中,左心室的16或17个阶段达到最小收缩容量的时间标准差(SD)(即所谓的收缩不同步指数(SDI)) 来准确评估LV不同步的方法[20]。色彩编码参数成像图显示了左室激动的时间弥散差和最晚心脏机械激动点 (图2)。已有报道证实了三维实时超声心动图SDI评估LV不同步和CRT治疗反应的优点。SDI≥6.4%能显著预测CRT治疗6个月后左心室的逆重构,其预测的敏感性和特异性分别为88%和85%[18]。 
A
图1。三平面组织同步成像评价左室不同步的最晚激动位点。A:色彩编码三维成像,显示左室心尖4 –腔, 2 –腔 和3 – 腔图。激动最早区域用绿色最晚区域用红色表示。用心室12阶段峰值速度的标准时间差值计算,显示左室的显著不同步(64毫秒)。B:牛眼图显示心室12阶段中每个阶段心肌速度的峰值时间。从而,确定了心室最晚激动位点。 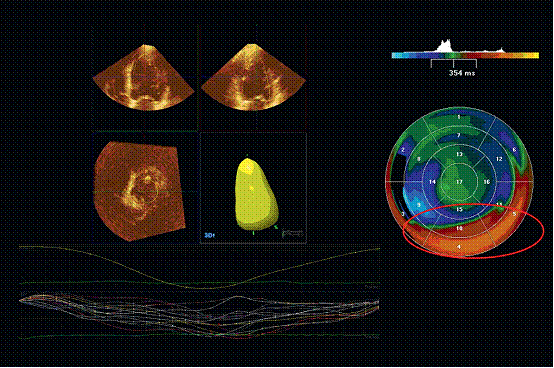
图2。实时三维超声心动图评价左室不同步和最晚激动位点。A:心内膜轮廓由心尖4 腔,2腔图显示。B:牛眼图为软件显示的整个左心室收缩末期容积曲线时间和左心室16个阶段中每个阶段的时间。显示左心室显著不同步(收缩不同步指数:8.9%)。C:显示心室16阶段中每个部分最小左心室收缩末期容积时间,红色显示被确定的心室最晚激动区。
然而,这些三维超声心动图的模式和技术并不能检测主动收缩心肌,特别是缺血性心力衰竭患者如此。因此,鉴别左室主动收缩心肌与没有活性而被周围心肌带动收缩的心肌阶段意义很大。近年来,三维超声心动图也用来分析心肌的应变或张力变化。斑点示踪成像能通过心肌超声束角度的变化独立示踪心肌声学标记(斑点),来准确评估心肌的变形[21]。通过多界面视图成像显示左心室至真正心尖部位的最大长轴尺寸,左心室总容量体积数据可通过5个交叉界面如左心室心尖、中部和基底短轴,心尖4腔和2腔视图获得。这样,心内膜可通过心尖视图通过手动操作示踪,于是,医生所关注的心室壁部位能够自动显示出来(图3)。最后,时间-张力曲线(time-strain)软件能显示LV 16 个阶段心肌在心动周期内的曲线图。通过计算LV不同阶段的峰收缩时差值可得出心脏不同步的结果。三维斑点径向应变示踪超声心动图量化LV收缩的不同步性,已经在心力衰竭和CRT治疗的患者中得到很好地使用[22]。田中等研究表明,心衰需要接受CRT治疗的患者,心室相对应室壁运动时间的延迟与健康志愿者相比明显推后。然而,斑点示踪径向应变三维超声心动图用于CRT预测反应的价值尚需进一步证实。 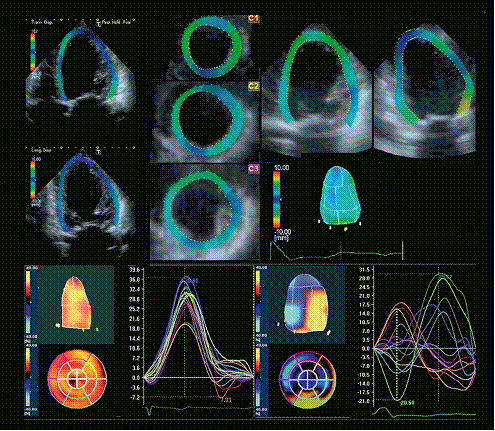
图3。三维应变评价左室不同步。A:多层面队列显示左室长轴后,3个横断面显示感兴趣的心室区域(心尖,心室中部和基础短轴)和心尖2腔和4腔图。得到左室容积和左心室射血分数,及左心室16阶段的时间 - 应变曲线图。B:一个健康志愿者的时间 - 应变曲线和参数图像,显示左心室同步收缩。C:左心室不同步收缩的心衰患者参数图像。显示左室最晚激动区域及其对应的左心室后段。转载自Nesser等21 Tanaka等22参考文献。
核素成像
近年来,相位分析方面的研究进展,已允许心肌灌注单光子断层发射计算机体层摄像(SPECT)用于心室不同步的评估[23,24]。常规心肌灌注门控SPECT的数学算法,可以获得心动周期中室壁运动的振幅(室壁收缩的厚度)和时相(机械收缩阶段)的差异资料。这些LV收缩的均一性和同质性的数据,可以用单极曲线图和直方图进行显示评价,从而,左室收缩的不同步可以用5个参数:即高峰相,SD位相,频带宽度,峰态和斜率来定量表示。图4说明了使用相位分析LV不同步的方法。直方图的频宽(95%相位角范围)和SD位相是最常用的评价左室不同步的指标。Henneman等[4]应用这些指标对NYHA≥I级的患者CRT治疗6个月的疗效进行了评价[25]。他们对42例心力衰竭CRT治疗患者,确定的最优切点直方图的频宽≥135°(敏感性和特异性70%),SD位相≥43°(敏感性和特异性74%)。
心脏磁共振成像(CMR)
用CMR评估LV左室不同步有几种方法,如快速电影梯度反射脉冲序列(fast cine gradient echo pulse sequences), CMR源性应变(CMR-derived strain), 速度编码CMR (velocity-encoded)图3。
稳态自由进动反射序列(Steady-state free precession gradient echo sequence)通常用于LV容积和功能评价。基于此方法,几种评价LV不同步的指标已被开发出来。例如,在一个RR间隔内,将室壁心肌运动在径向方向上分为20个阶段,以正弦波曲线形式,从LV短轴图上分析,可以评估心室壁运动情况。左室壁阶段运动最大径向位移可以从正弦波曲线获得。因而,左室不同步指数,也称作CMR组织同步指数(TSI),可以从左室阶段室壁运动的径向位移时间差值(SD)得到[26]。Chalil等最近证明,若心力衰竭病人CMR TSI≥110 ms,与<110 ms患者相比,全因死亡和心力衰竭住院危险性高(危险比[HR]=2.21;95%可信区间[95%CI1.33-4.14,P =0.018),及心血管疾病死亡的较高风险(HR =4.1, 95%CI1.83-17.47,P=0.001)。因此,与以往超声心动图技术的研究一致,CMR左室不同步的TSI结果是一个独立的预后指标。这些使用稳态自由进动CMR 获得的LV不同步指数对预测患者未来对CRT的反应和治疗后的远期结果很有价值。35例心力衰竭接受CRT植入的患者,从左室3个短轴切面(包括基底部,中部和心尖部),使用16个阶段心肌达到最大收缩期厚度的时间差值SD,来评价LV的不同步性。(图5A ,5 B)。CMR预测左室不同步指数大的患者植入CRT,较左室不同步不明显的患者, 在6个月随访中左室收缩末期容积减少15%(中位数97ms [四分位:90-106] vs 60ms [47-71],P <0.001)。而且,CMR左室不同步与超声心动图CRT的反应结果独立相关(odds ratio=6.3,95%CI3.1-9.9,P <0.001)[10]。
此外,示踪CMR基于心肌应变分析评估LV不同步。在心动周期中通过心肌标记模式,利用谐振相方法,测量左室圆周心肌的应变指数。在示踪CMR获取的LV不同步数据中,左心室圆周均匀比估算指数(circumferential uniformity ratio estimate (CURE))能提供最广泛的资料来预测患者对CRT的反应和长期临床结果[12]。在LV短轴切面,沿心动周期变化可以测量圆周应变张力,以及通过傅里叶级数分解测量左心室瞬时圆周形变弥散度,从而获得CURE指数。CURE指数介于0(绝对同步)和1(相对左室同步)之间。Bilchick等在最近一个包括43例心力衰竭病人的研究中显示,CURE指数<0.75充分预测1 NYHA患者CRT植入6个月后心功能改善(灵敏度100%,特异性为71%)。因此,基于示踪CMR的不同步应变分析指数,可以改善病人对CRT的选择过程,准确地确定显著LV不同步患者从CRT获益。基于三维示踪序列和光流法的CMR新方法已问世,能够在3D层面上对心肌应变进行评估,目前正在进行的研究将进一步表明,这种新技术有助于进一步对CRT治疗患者的选择[27]。
此外,CMR对LV不同步的评估也有报导可使用速度编码成像方法[28]。沿LV长轴切面,应用速度编码CMR方法,能够测量心动周期中心室壁心肌的运动,并提供类似组织多普勒成像的时间 - 速度曲线。在对立的心室壁之间峰收缩速度的时间差,能提供LV不同步的数据。与正常对照相比,左束支阻滞的心力衰竭患者用这种方法显示左心室不同步更明显(分别为5-17ms vs 49-38 ms)。到目前为止,使用速度编码CMR预测LV不同步,提供患者选择CRT的反应和长期预后结果的优点尚未见报道。 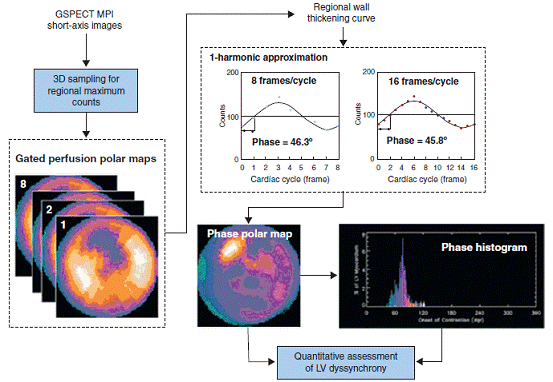
图4。核成像技术评估左心室不同步。门控单光子发射计算机断层心肌灌注摄像,取得心室各阶段的最大计数,用门控灌注极性图显示心动周期三维图像。此后,得到心动周期心室各阶段最大计数变化值,按第一谐波傅立叶功能获得心室壁增厚曲线,并计算各阶段时相。从而得到重复计算后左心室各阶段的机械收缩图,即位相极性图和直方图。转载之陈等参考文献24。GSPECT:门控单光子发射断层摄像;LV:左心室; MPI:心肌灌注显像 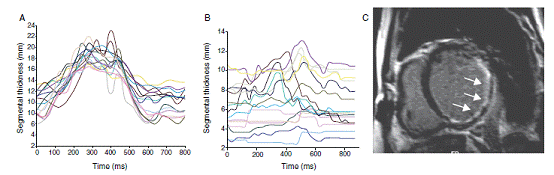
图5。心脏再同步治疗患者的心脏磁共振成像。A:显示左心室不同步评估结果:一个正常的人的心脏磁共振,没有左心室不同步。 B:显示左心室不同步的分析:缺血性心力衰竭患者心脏再同步治疗前,有显著的左心室不同步,通过计算左室最大增厚时间的标准差获得(92毫秒)。 C:显示心内膜瘢痕组织(亮)延迟对比增强心脏磁共振序列图,在左室侧后下壁(箭头)。
基于这方面的证据,LV不同步是决定CRT治疗的重要因素,三维成像系统可以准确评估左室不同步。比较低的瞬时分辨率和实用性是这些成像技术的主要限制。此外,这些成像技术评估左室不同步要求有高技术专业知识的专门人才,以提供准确、重复性好的评估结果。 LV机械不同步不是植入CRT的绝对标准。尽管许多试验的结果显示,该参数具有预后价值。但PROSPECT试验表明,2- D超声心电图成像评估的LV不同步参数,对预测CRT反应方面仅有中等程度的准确性[29]。正在进行的随机试验,如EchoCRT试验,将提供评估不符合当前标准(QRS时限> 120毫秒)的心力衰竭患者,LV不同步的再同步化治疗的进一步信息[30]。因而, LV不同步的信息与其它病理生理因素的整合分析,如心肌疤痕的程度和位置可能有利于进一步确定患者对CRT治疗的反应结果。因此,3D成像技术如核素成像和CMR可以提供植入CRT能够获益患者的综合信息。下一部分我们将讨论能够评价心肌纤维化程度和存活心肌的CMR三维成像技术。
疤痕组织的位置和总负荷
最近,具有里程碑意义的试验,缺血性和非缺血性心力衰竭患者CRT获益的预后方面亚组分析比较,发现缺血性心力衰竭患者LV的逆重构和左心功能改善,比非缺血性心力衰竭患者差[31]。高负荷心肌疤痕组织可能会阻止LV的逆重塑,和对CRT植入获益的反应。另外,在LV电极植入部位的疤痕组织可能会影响CRT.的疗效[32,33]。增强CMR,SPECT心肌灌注显像,正电子发射断层扫描是目前确定心肌疤痕组织和存活心肌的成像技术。此外,斑点示踪超声心动图的应变分析与心肌造影超声心动图可以显示心肌的疤痕组织[34,35]。
心脏磁共振
晚期钆(Gd)增强序列CMR是评估心肌疤痕组织的金标准。顺磁造影剂积聚在间隙组织,提供了一个铊(T1)加权序列增强的影像。在心肌疤痕区域,钆对比CMR可以分别准确确定疤痕间隙较正常心肌增强的(亮)部位和低信号(暗)组织(图5 - C)。此外,CMR技术能够精确区分透壁的疤痕和心内膜下的疤痕组织。
一些研究已经显示了心肌疤痕组织的位置与CRT获益之间的关系[32,33,36]。在一个40例终末阶段缺血性心力衰竭病人CRT植入前行钆增强CMR的研究表明,LV起搏电极植入部位的透壁性疤痕组织,是CRT无获益的指标。心脏后外侧壁区域存在透壁性疤痕(> 50%的左心室壁厚度)的患者,与无后外侧透壁性疤痕相比,对CRT的反应率明显降低(14%VS 81%,P <0.001)。此外,与无后外侧透壁疤痕的患者相比,存在透壁疤痕的患者有明显的LV不同步。这些结果表明,起搏部位的透壁疤痕面积可能会减少对CRT获益的效果。此外,White等研究表明,钆增强CMR确定的心肌疤痕组织的程度与CRT获益反应相关。在一组28例心力衰竭接受CRT植入患者的3个月随访研究发现,占LV心肌15%的疤痕组织,能够准确预测对CRT治疗的获益程度(敏感性为85%,特异性为90%; P = 0.001)。这些结果,在一项包括34例缺血心力衰竭病人,植入CRT之前行晚期钆增强CMR检查的研究中进一步得到了证实。CRT植入后6个月结果显示,LV总的疤痕负荷与左心室的逆向重塑方面存在显著的反比关系(R = 0.91,P <0.05)。而且,左室透壁疤痕组织越少,CRT无反应的程度就越少(1.61.5 VS 5.61.6,P <0.05)。最后,Chalil等分析了45例缺血性心力衰竭的整个心室疤痕负荷和疤痕位置对CRT植入获益的影响,结果表明左心室总的疤痕负荷和透壁程度百分比的多变量分析,是CRT获益最强的决定因素(P <0.05,X2 = 5.21和8.23),而疤痕的具体位置则没有决定性[33]。
核素成像
SPECT心肌灌注显像的使用提供了左心室疤痕负荷和部位有价值的资料。 Ypenburg等描述了51个接受CRT植入的患者,使用SPECT心肌灌注成像技术来评估疤痕组织和存活心肌的程度,预测对CRT获益的反应[37]。植入6个月的随访表明, 27例(53%)患者获益。值得注意的是,获益的患者存在明显的存活心肌阶段(示踪剂摄取75%以上的阶段),而无获益者比较低(12 阶段[11,13] vs 8阶段[5,10]; P <0.001)。而且,CRT植入6个月发现,在LV电极植入部位存在透壁疤痕组织(示踪剂摄取<50%)的患者,与没有透壁性示踪剂充盈缺损的患者相比,缺乏明显的左心室逆重构。此外,对心肌疤痕与CRT长期结果的关系进行了研究[38], 380例非缺血性心力衰竭病人和190例缺血性心力衰竭病人的队列研究表明, CRT基线201铊1心肌灌注成像和随访1.9年(中位数; 范围为:2天至10年),疤痕容量根据心室17个阶段的示踪剂充盈程度(0 =正常摄取,4 =示踪剂充盈缺损)显示,结合总的疤痕计分来确定,疤痕负荷重的缺血性心力衰竭病人(疤痕评分27)比非缺血性心力衰竭(P <0.001)和缺血性心力衰竭疤痕负荷轻(疤痕评分<27)(P = 0.002)的患者相比,预后明显较差。
正电子发射断层扫描也被用来评估CRT治疗患者的存活心肌。61例缺血性心力衰竭患者,在接受CRT治疗前行正电子发射断层扫描检查[39],总的存活心肌阶段数(示踪活动> 75%)与CRT植入6个月后的左心室射血分数(LVEF)的绝对值呈直接相关(R = 0.56,P <.05)。存活心肌阶段数11(总数为17阶段)是可充分预测CRT后6个月获益的最佳切入值(敏感性74%,特异性87%)[39]。
超声心动图
2D超声斑点示踪收缩期应变峰值已被用来确定心肌疤痕组织和存活心肌[40]。高应变值与高存活心肌相关。Becker等显示2 D斑点示踪应变峰值为16.5%时,是确定透壁和非透壁性疤痕的切入值,其灵敏度和特异性分别为70%和71%。此外,三维应变超声心动图对32例患者室壁运动的分析[41],已经得到了CMR的验证。但三维应变超声心动图在评估心力衰竭患者存活心肌与CRT获益的关系方面尚未见报道。
左室电极位置
最后,除了左心室的不同步和心肌疤痕组织,LV电极的最佳位置也对最大限度地提高CRT获益率和生存率是非常重要的。已经提出LV最晚的激动区域是LV电极放置的最佳位置,这样可提供最大的血流动力学获益[42]。实时三维超声心动图,三维斑点追踪应变分析和SPECT灌注显像已被用来寻找心室最晚的机械激动位点。Becker在58例患者的CRT植入中,用实时三维超声心动图确定心室最晚激动位点。LV的最晚激动位点被用来确定左心室电极植入的最佳位点[43]。确定的最佳植入位点患者的左室容积,左室射血分数,和最大O2耗量,较非最佳起博位点植入的患者,有显著的统计学改善(所有的比较值均为P <0.001)。此外,Boogers在一项95例CRT治疗患者的研究表明,LV最晚激动点与SPECT心肌灌注显像和LV电极植入位点一致,使NYHA心功能分级,左室容积与LVEF显著得到改善(P <0.05,基线和6个月随访)[44]。相反,LV电极位置与最晚激动点不一致,CRT后6个月患者心功能没有显著改善。最近一项54例心脏衰竭CRT治疗的研究也评估了使用3D斑点应变示踪的可行性。
不断累积的证据表明,左心室电极应放置在LV的最晚激动位点。然而,冠状静脉解剖可能不会总能适合这种位置。事实上,个体间的冠状静脉解剖变异相当大[45]。以前有过心肌梗死的患者可能更是如此。在一组100例用多排螺旋CT评价的患者,van de Veire等的研究显示,后静脉和左侧边缘静脉(通常用于放置LV电极),在有心肌梗死病史的患者与对照组相比,通常很难用来放置左心室电极(26.5% vs 71.4%; P <0.001)(图6)。因此,除了确定心室最晚激动点外,用无创性多排螺旋CT(MDCT)显示心脏静脉解剖分支,寻找最佳左室电极植入位置受到关注[46]。事实上,已有报道CRT植入前,结合三维超声心动图心室最晚激动点与多排螺旋CT冠状静脉造影解剖确定植入血管。21例心衰患者CRT植入前,心室最晚激动点用三平面组织同步成像(triplane tissue synchronization imaging)技术确定,结合64排MDCT确定植入冠状静脉血管分支,12例患者左心室植入电极位置与最晚激动点一致,这些患者左室收缩末期容积显著减少(平均减少26毫升,13.3%)和LVEF明显改善(平均增加12%),而不一致的患者没有显著性改善。此外,最晚激动点与LV电极植入位点一致的患者,CRT后72小时内,LV 不同步显著改善(43- 7ms 至11-9ms,P <0.0001),左室收缩末期容积显著下降(188-54毫升 vs 162-48毫升,P <0.01)和LVEF的明显改善(22-9% vs 34-9%, P <0.01)。相反,二者之间不匹配的患者,左心室的不同步和左室功能没有明显改善。然而,X线的辐射暴露和含碘造影剂的应用,限制了MDCT的广泛使用。未来对球管的改良和连续扫描技术能够有效减少辐射剂量[47]。 
图6。心脏再同步治疗患者的冠状静脉解剖。多排CT重建的三维冠状静脉解剖图。2例心脏再同步治疗选择。左图显示了一个合适的静脉解剖分支,是最佳左心室电极导线的放置位置。相反,右图显示缺失左室后静脉和左侧缘静脉分支。 LMV,左侧缘静脉;LV,左心室; PIV,室间后静脉; PVLV,左心室后静脉;RCA,右冠状动脉;;RV,右心室。 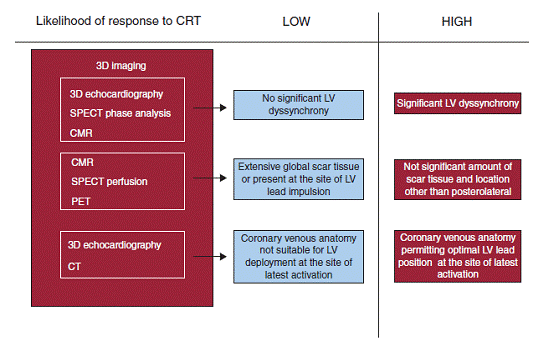
图7。多种方法联合确定心脏再同步治疗的个体反应图。CMR,心脏磁共振; CRT,心脏再同步治疗,CT,计算机断层扫描; LV,左心室; PET,正电子发射断层扫描显像;SPECT,单光子发射计算机断层。
心脏再同步化治疗三维成像技术的综合评估
LV不同步,心肌疤痕组织和LV电极植入位置是评价CRT治疗获益性和长期结果的3个主要决定因素。每一个决定因素均可用三维成像方式加以评估,从而提供选择CRT患者的全面评价数据。例如,Bilchick等报告了结合CMR评价左心室疤痕组织和LV不同步(CURE指数)预测的准确性,CURE指数<0.75和疤痕组织为LV心肌量的15%时,对确定有获益的患者,阳性预测值93%,预测的准确性最高(95%,P <0.001),阴性预测值[100%]。最后,综合决定因素的评估可能进一步提供CRT候选患者的预后信息。因此,Leyva等。提出了一个综合预后评分系统,包括CMR TSI左心室不同步和后外侧壁疤痕位置[48]。一组148例心力衰竭病人CRT术前进行预后评分,随访913天(中位数;四分位为967天)。在基线计算得到的预后计分值是一个强有力的预测心血管疾病死亡率的指标。而且,与最低得分(得分指数<3)的患者相比,具有较高得分(指数>5)的患者心血管事件的风险最高(HR = 30.5,95%CI 9.15-101.8; P <0.0001)。中间计分(>3评分<5)的48例患者,表现出心血管事件的中等风险(HR = 11.1,95%CI 3.0-41.1,P = 0.003)[48]。
此外,为了提高预测的准确性,结合LV的不同步、存活心肌,以及2D斑点示踪径向收缩应变预测评估,最新对397例缺血性心力衰竭病人植入CRT后的全因死亡率进行了预测研究。根据这些研究证据,一个综合多种模式的方案被提了出来,如结合评价LV不同步,左心室电极的最佳位置(冠状静脉解剖),和疤痕组织程度范围等评价患者可能的反应性。左心室显著的不同步,左室电极植入的靶部位缺乏疤痕组织,整体左室疤痕负荷较轻,以及冠状静脉允许最佳电极植入(左心室最晚激动点位)的患者有可能具有最高的获益反应性(图7)。这样选择的CRT病人,才有可能获益和改善心功能。
综上所述,三维成像技术的最新进展提供了全面评估CRT患者的方法,它们提出了那些患者可能从CRT获益。但日常临床实践中明确实施这些成像技术的重要挑战是,决定患者对CRT反应的三维病理生理因素,准确可重复性的评估方法,结合辐射暴露和费用等问题的综合考虑。正在进行的研究将提供足够的证据,来进一步说明这些成像技术在选择CRT治疗过程中的作用价值。
参考文献(略)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#心脏再同步化#
55
#三维成像#
63
#成像技术#
56