Lenzilumab 治疗 COVID-19 住院患者,未达到主要终点
2022-07-25 MedSci原创 MedSci原创
FDA 已经拒绝了该公司寻求紧急使用该疗法治疗新住院 COVID-19 患者的请求。美国监管机构确定,它无法得出 lenzilumab 的潜在益处超过潜在风险的结论。
美国国立卫生研究院 (National Institutes of Health) 的一项评估 lenzilumab 和 Gilead Sciences 的 Veklury (remdesivir) 治疗 COVID-19 住院患者的试验(ACTIV-5/BET-B 研究)未能达到其主要终点。虽然 ACTIV-5/BET-B 研究显示出临床效果的迹象,但所证明的益处无法证实在 III 期 LIVE-AIR 研究中看到的积极结果。
ACTIV-5/BET-B 试验在入院的 COVID-19 患者中评估了 lenzilumab 联合 Veklury vs. Veklury 联合安慰剂的有效性和安全性。主要终点定义为第 29 天仍存活且无需机械通气的患者比例。Humanigen 表示,数据显示总体死亡率降低的“非显著趋势”。研究中没有新的安全信号归因于 lenzilumab。
去年 3 月,Humanigen 报告了 III 期 LIVE-AIR 研究的结果,显示与安慰剂和其他治疗相比,lenzilumab 将 COVID-19 住院成人在无需侵入性机械通气的情况下存活的机会提高了 50% 以上。
LIVE-AIR试验在美国和巴西进行,招募了 520 名 18 岁以上的 COVID-19 肺炎住院患者,这些患者存在缺氧症状,但尚未进展到需要侵入性机械通气的程度。参与者被随机分配接受 lenzilumab 或安慰剂,在 24 小时内每 8 小时接受一次其他治疗,其中包括地塞米松或其他类固醇和/或 Gilead Sciences 的 Veklury(remdesivir)。
LIVE-AIR试验的结果显示,在 479 名患者的意向治疗分析中,lenzilumab 组中有 15.6% 的患者在 28 天时进展为机械通气和/或死亡,而安慰剂组为22.1%,即实现了 54% 的改善。Humanigen 表示,在总体生存率方面也存在“有利趋势”,因为 lenzilumab 治疗的患者中有 9.6% 在试验中死亡,而安慰剂组为 13.9%(图1)。
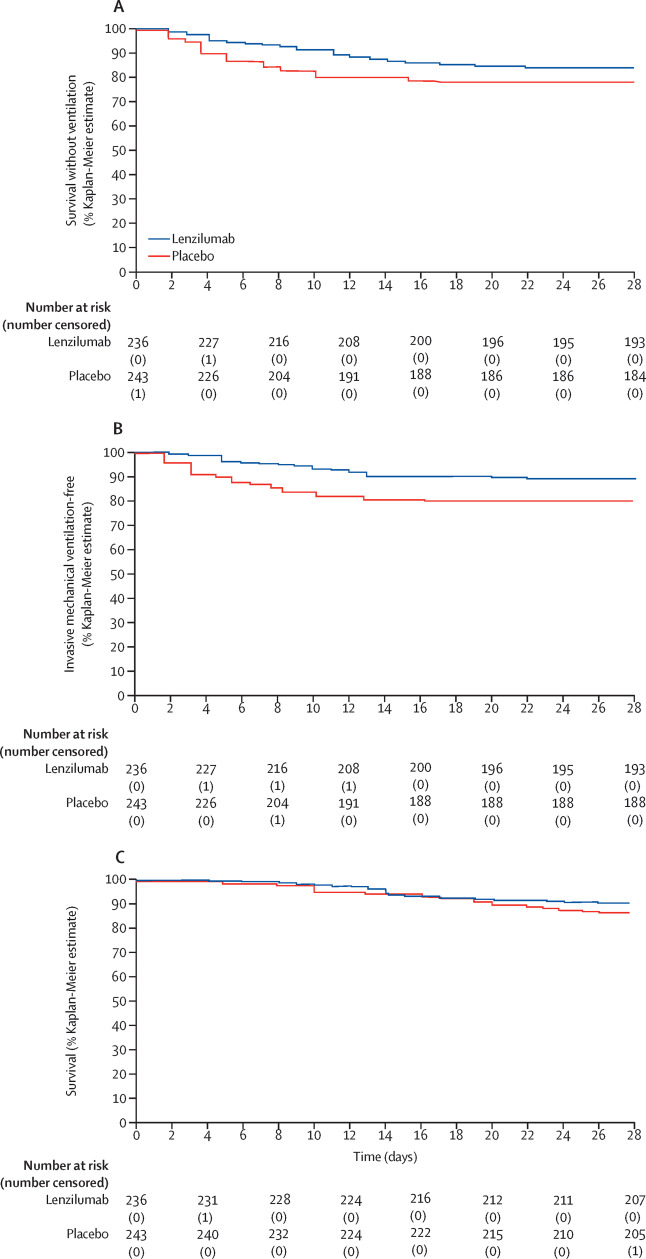
图1. Kaplan-Meier 生存图
然而,FDA 已经拒绝了该公司寻求紧急使用该疗法治疗新住院 COVID-19 患者的请求。美国监管机构确定,它无法得出 lenzilumab 的潜在益处超过潜在风险的结论。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#主要终点#
96
#mAb#
72
学习
72
学习
70