ATVB 温州医科大学附属第一医院叶浡之团队揭示巨噬细胞来源的GSDMD在动脉粥样硬化中的新机制
2024-05-07 论道心血管 论道心血管 发表于上海
该研究揭示了巨噬细胞来源的Gasdermin D在动脉粥样硬化发生发展过程中的重要作用,并深入探讨了GSDMD介导的线粒体-STING-IRF3/NF-κB通路在巨噬细胞间的信号传递机制。
动脉粥样硬化是一种慢性炎症性心血管疾病,基于炎症反应的治疗策略成为动脉粥样硬化的研究热点和重点。细胞焦亡是一种炎症性细胞程序性死亡,焦亡执行蛋白GSDMD在动脉粥样硬化进程中发生活化,表明GSDMD在动脉粥样硬化中扮演重要角色。
2024年5月2日,温州医科大学附属第一医院心血管内科叶浡之团队在Arteriosclerosis, Thrombosis, and Vascular Biology杂志在线发表研究论文“Macrophage-Derived GSDMD Plays an Essential Role in Atherosclerosis and Cross Talk Between Macrophages via the Mitochondria-STING-IRF3/NF-κB Axis”。该研究揭示了巨噬细胞来源的Gasdermin D (GSDMD)在动脉粥样硬化发生发展过程中的重要作用,并深入探讨了GSDMD介导的线粒体-STING-IRF3/NF-κB通路在巨噬细胞间的信号传递机制。

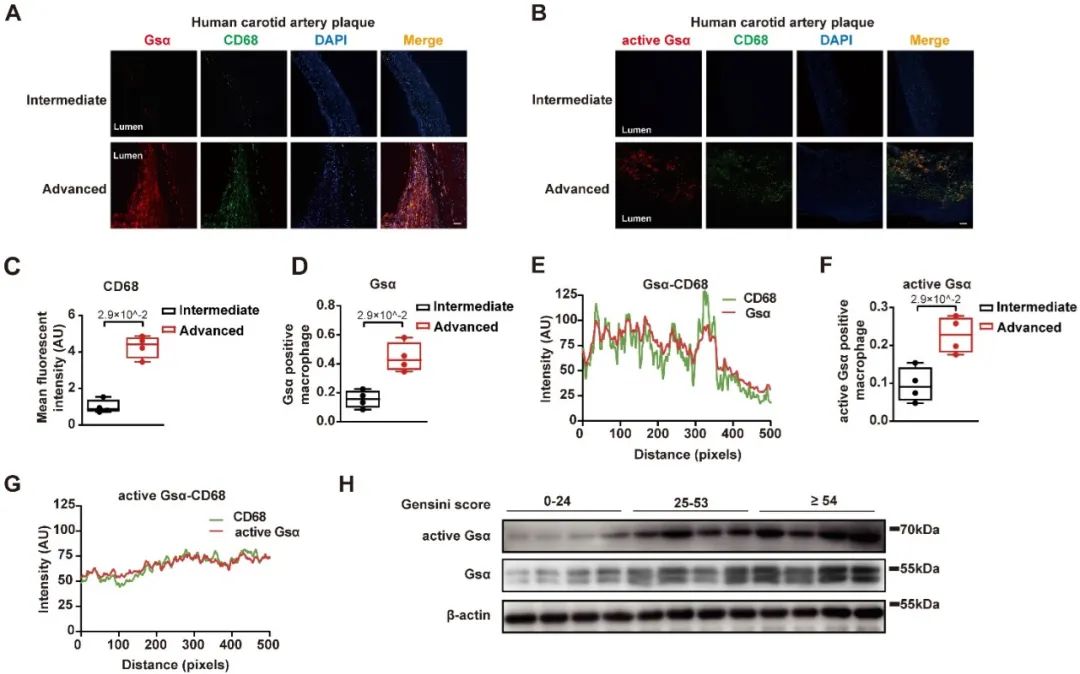
首先,作者对人体和小鼠的动脉粥样硬化血管样本分析发现,与正常血管组织相比,动脉粥样斑块中的GSDMD蛋白水平显著激活。随后,作者成功构建了Gsdmd-/-ApoE-/-小鼠。实验结果显示,与高脂喂养的ApoE-/-小鼠相比,高脂喂养的Gsdmd-/-ApoE-/-小鼠主动脉动脉粥样硬化病变程度显著减轻。
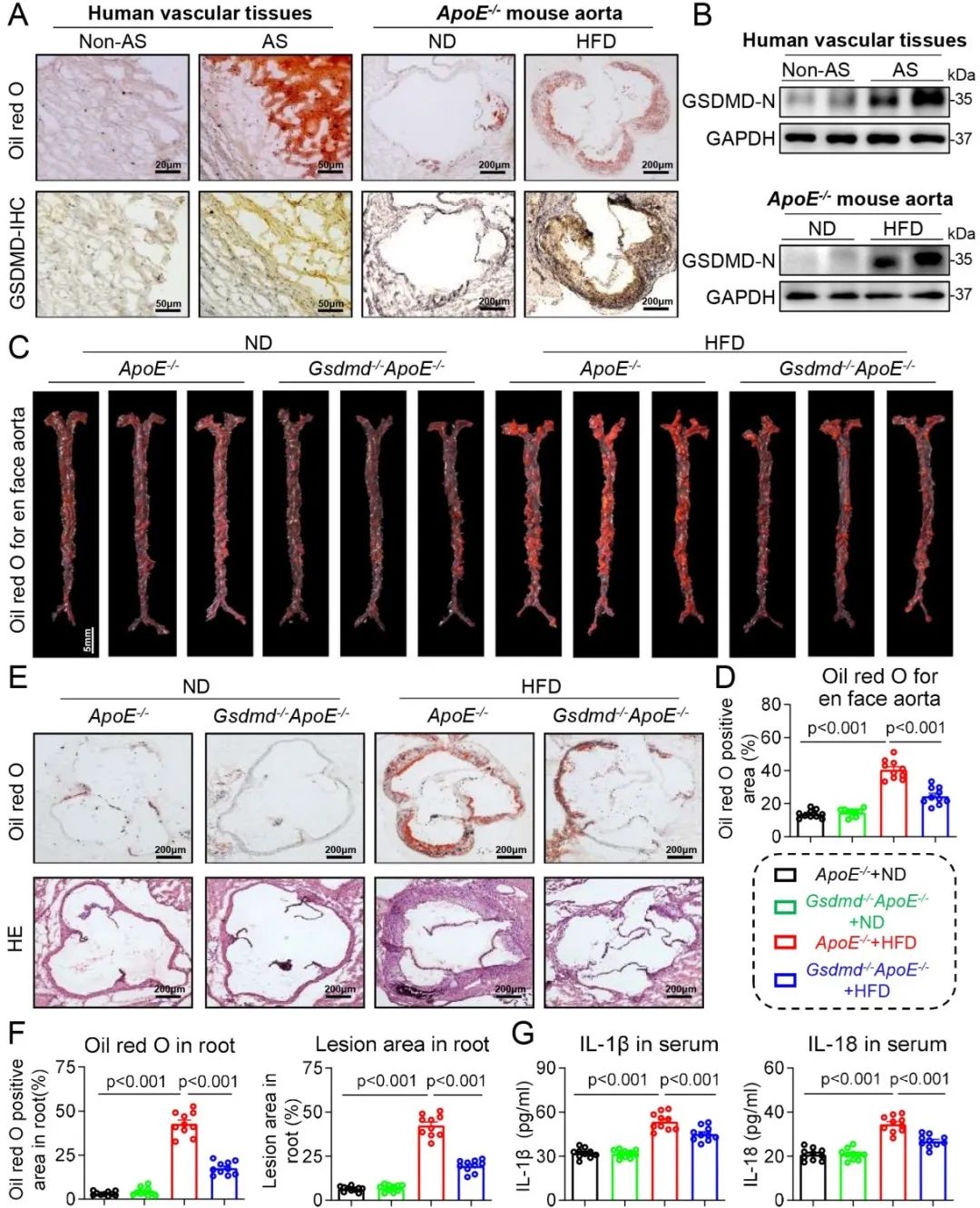
此外,作者对小鼠动脉粥样硬化组织进行了单细胞测序分析。结果表明,GSDMD主要在动脉粥样硬化巨噬细胞(特别是M1巨噬细胞)中表达。研究团队利用骨髓移植实验及重组腺相关病毒血清型9干预巨噬细胞GSDMD的在体表达,证实了巨噬细胞来源的GSDMD参与了动脉粥样硬化的进程。
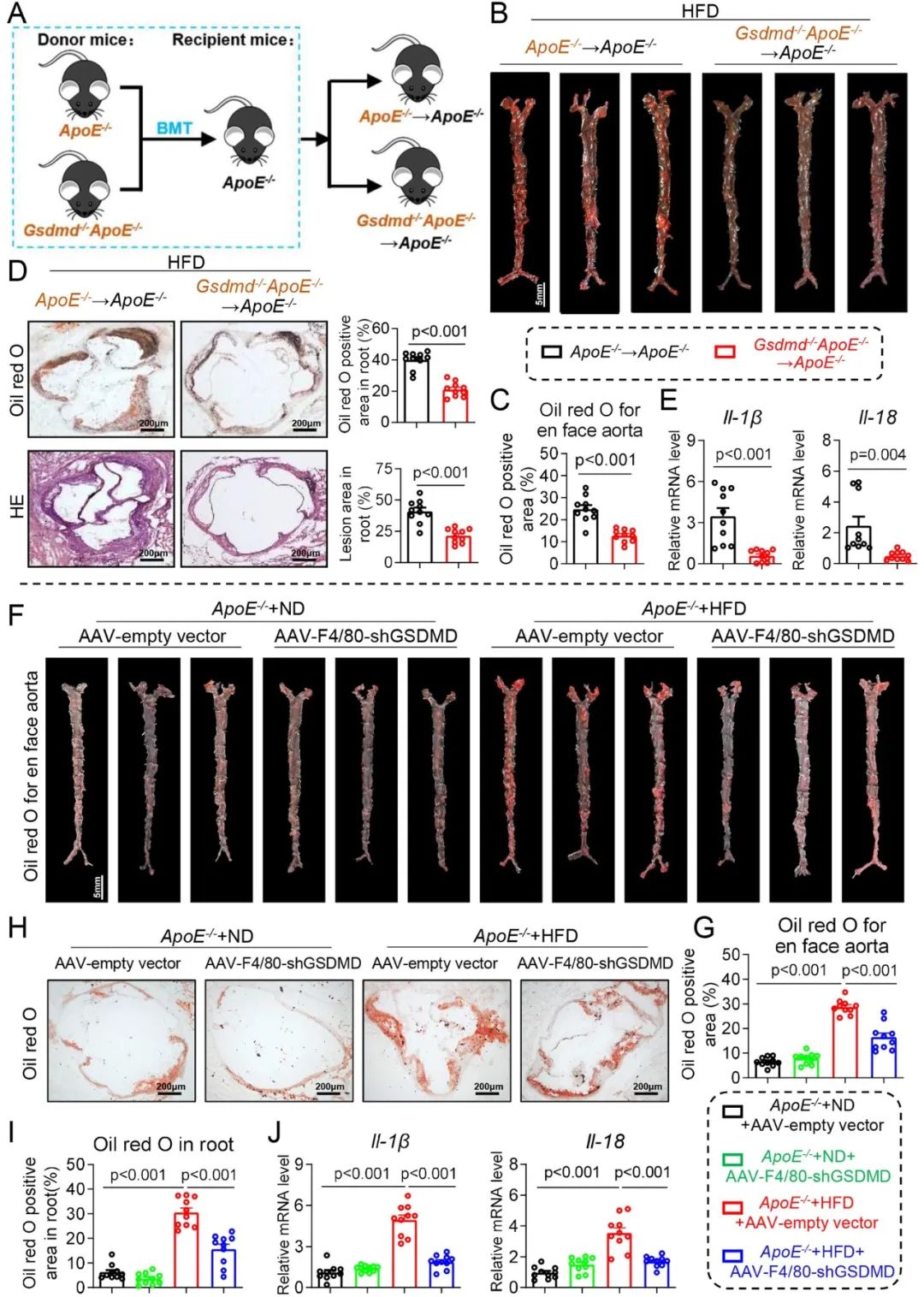
为了进一步验证GSDMD在巨噬细胞中的作用,作者通过提取小鼠腹腔原代巨噬细胞,发现抑制巨噬细胞GSDMD可以显著改善ox-LDL(氧化型低密度脂蛋白)诱导的线粒体损伤,并减轻巨噬细胞焦亡。
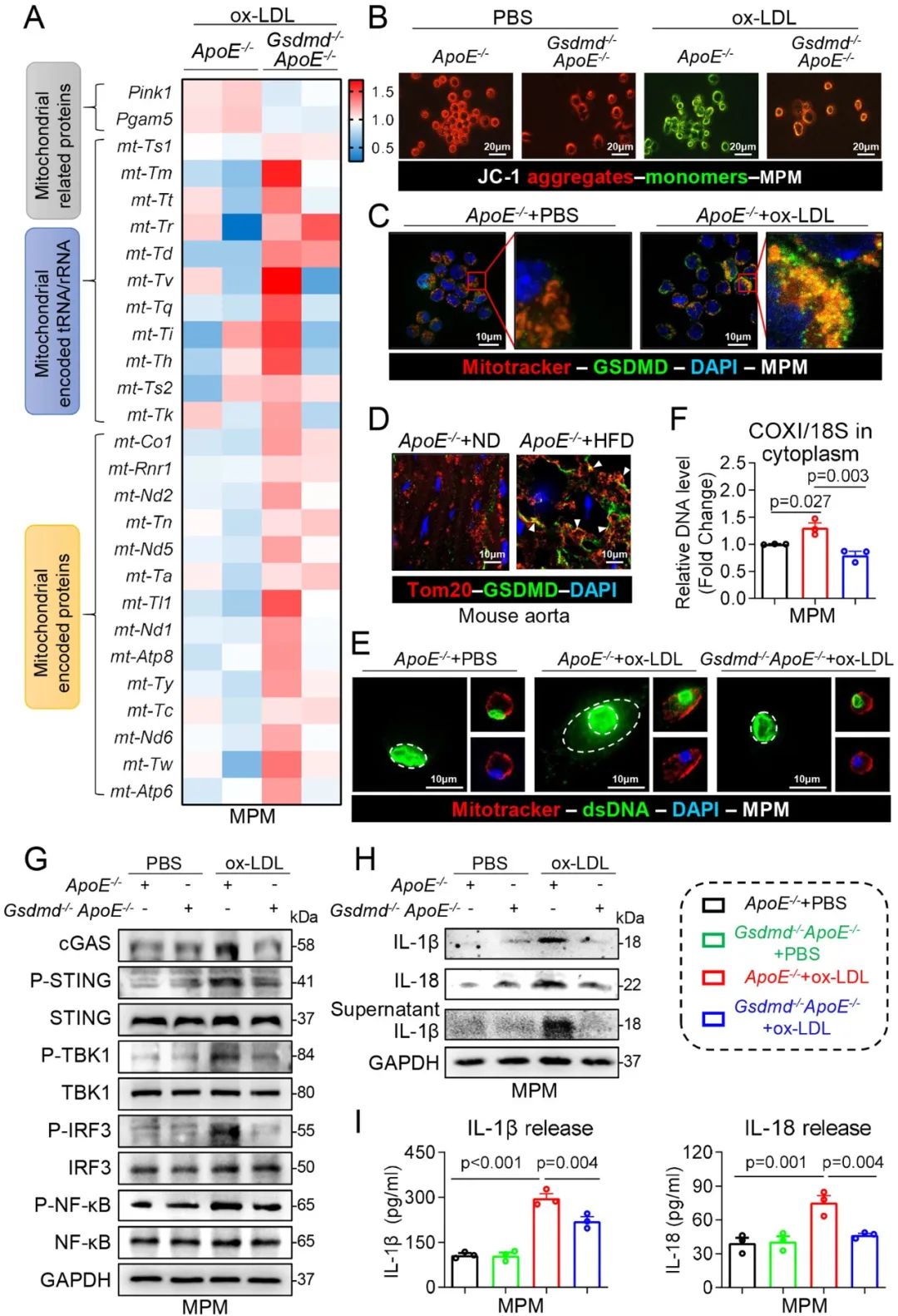
值得注意的是,作者进一步发现GSDMD可以通过促进细胞因子(尤其是IL-1β)的分泌,进而级联激活巨噬细胞中cGAS/STING/TBK1/IRF3/NF-κB信号通路和巨噬细胞的迁移。这一发现为我们理解动脉粥样硬化的发展过程提供了新的视角。
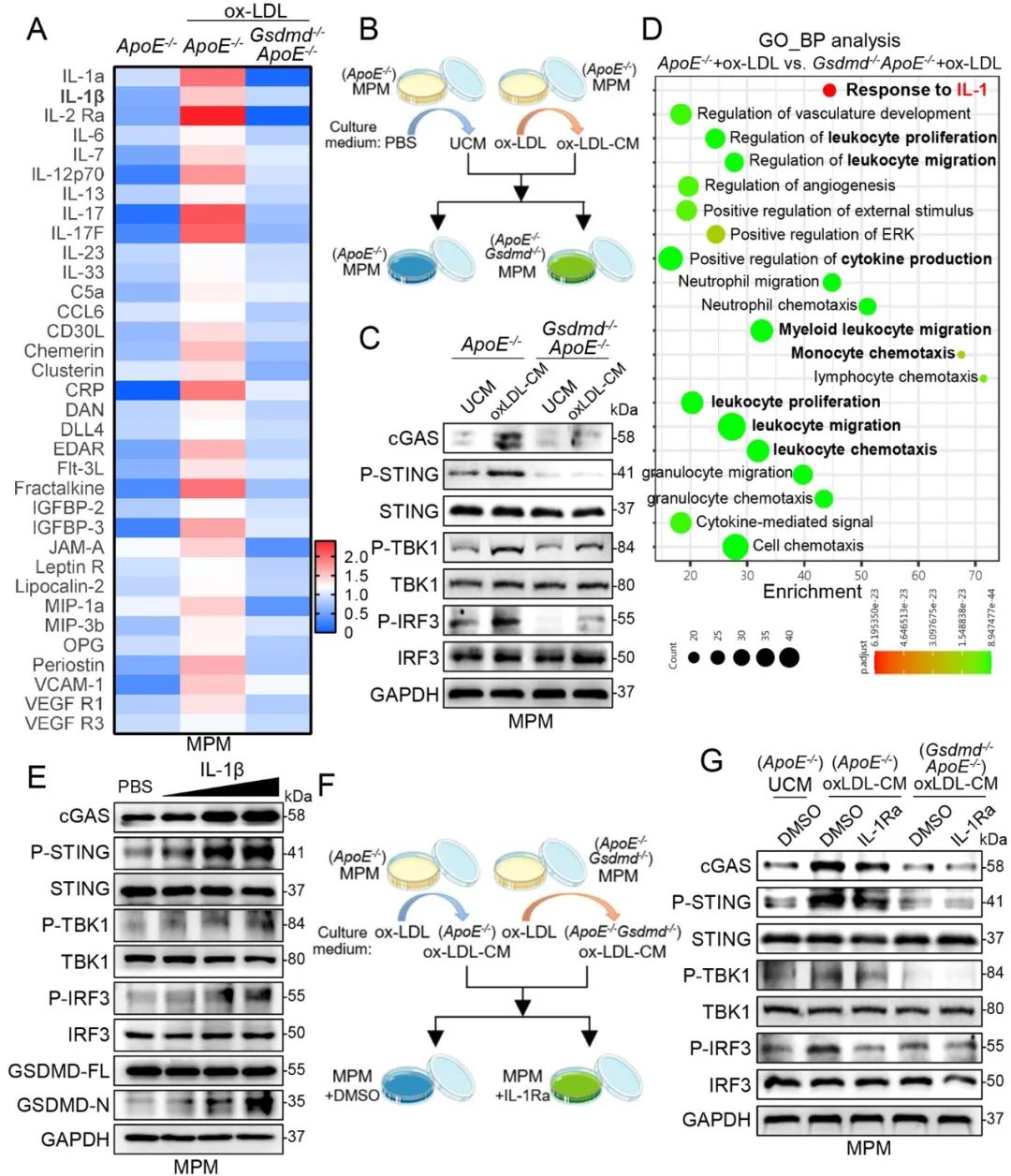
为了探索GSDMD作为治疗动脉粥样硬化的潜在靶点,作者使用了团队自主开发的一种新型GSDMD小分子抑制剂GI-Y1。实验结果表明,GI-Y1可以通过抑制GSDMD改善线粒体mtDNA泄露进而抑制STING信号通路,减少动脉粥样硬化斑块形成。这一发现为动脉粥样硬化的防治提供了新的潜在策略。
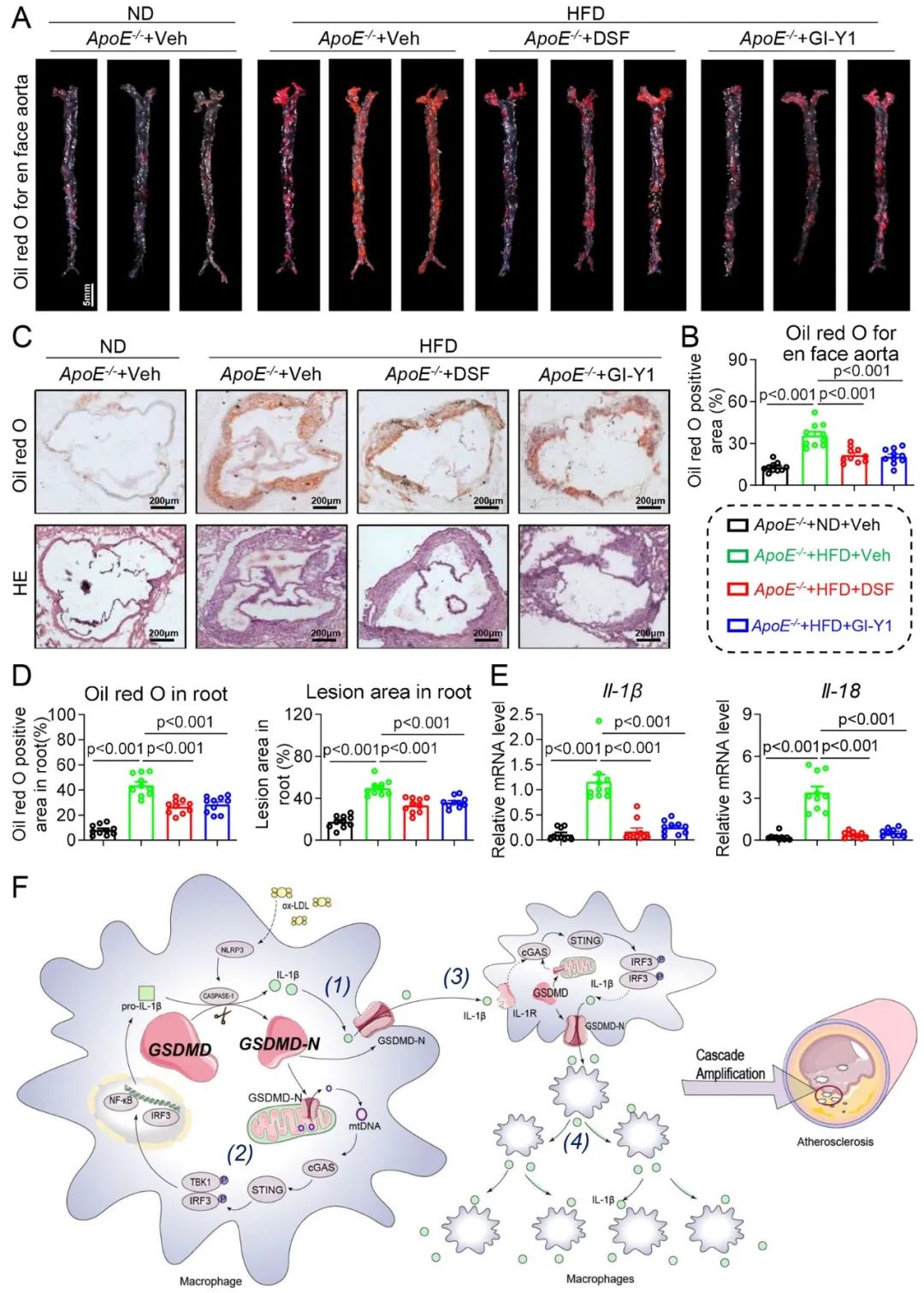
综上,这项研究不仅揭示了GSDMD在动脉粥样硬化发展过程中的重要作用及其机制,还为该疾病的防治提供了新的潜在方案。未来,团队将继续深入研究GSDMD的功能及其与心血管疾病的关系,以期开发出更加有效的治疗方法与临床策略。
该研究工作在温州医科大学附属第一医院心血管内科、温州市心血管病研究重点实验室开展。温州医科大学附属第一医院心血管内科黄伟剑主任医师、蔡雪黎主任医师以及叶浡之副研究员为论文的共同通讯作者,心血管内科硕士研究生樊晓浠、嘉兴市第二医院心内科韩集波为共同第一作者。本研究获得浙江省动脉粥样硬化疾病精准医学研究重点实验室开放基金、国家自然科学基金、浙江省自然科学基金等项目资助。
原文链接:
https://www.ahajournals.org/doi/10.1161/ATVBAHA.123.320612
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#动脉粥样硬化# #GSDMD#
143