一名肝硬化患者接受血管紧张素转换酶抑制剂/血管紧张素II 受体拮抗剂联合疗法后发生重度肝性脑病:病例报告
2011-06-07 MedSci原创 MedSci原创
引言 在初步显示出疗效后,血管紧张素转换酶抑制剂(ACEI)/血管紧张素II受体拮抗剂(ARB)联合疗法即被用于控制蛋白尿 [1]。然而,最近出现了对该疗法安全性的担心,使得几名作者敦促慎用此疗法[2]。在这份病例报告中,我们描述了一名肾病综合征和肝硬化伴严重门脉高压的患者用ACE I和ARB联合疗法后出现的一种严重非预期药物不良反应。我们认为上述不良反应很可能
引言
在初步显示出疗效后,血管紧张素转换酶抑制剂(ACEI)/血管紧张素II受体拮抗剂(ARB)联合疗法即被用于控制蛋白尿 [1]。然而,最近出现了对该疗法安全性的担心,使得几名作者敦促慎用此疗法[2]。在这份病例报告中,我们描述了一名肾病综合征和肝硬化伴严重门脉高压的患者用ACE I和ARB联合疗法后出现的一种严重非预期药物不良反应。我们认为上述不良反应很可能与联合疗法的肾脏效应有关,患特定共病的高风险患者用此联合疗法时应考虑这种情况。
病例报告
一名患肝硬化和肾病综合征的40岁白人男性于2007年12月来我院肝病中心就诊。他在14岁的时候被诊断出患有肝病。当时排除了病毒和自身免疫性病因以及先天性代谢异常。患者28岁时发生了一次静脉曲张破裂出血后,开始用普萘洛尔,成功预防了再次出血。经组织学检查,他在30岁时被诊断为肝门静脉硬化,33岁时被诊断为膜性肾小球肾炎,需用呋塞米治疗(125 mg/天)。
2008年1月,患者入住我院肝病中心,进行全面评估是否适合肝移植。患者无症状,体检发现轻度肝脾肿大,无扑翼样震颤、黄疸或腹水。超声显示有门脉高压的证据,包括门静脉直径增大和侧支循环开放。虽然用了6周前开处的氯沙坦50 mg/天,患者仍有尿蛋白3.7 g/24小时,肌酐值正常。因此加用雷米普利2.5 mg/天。
第一次用雷米普利约12小时后,患者失去了意识。格拉斯哥昏迷(GCS)评分为6分(睁眼反应1分,言语反应1分,运动反应4分),血压(BP)为 130/80 mmHg,心率(HR)是60 bpm,未发现生化和血气分析较基线有明显变化(表 1);毒理学筛查为阴性。脑部计算机断层扫描(CT) 未见压迫或出血征象,而脑电图(EEG)显示脑活动性整体偏慢,符合毒性或代谢改变。停用口服治疗,开始用乳果糖灌肠和支链氨基酸静脉补液,患者于 30-36小时内恢复意识。完全恢复意识后,重新阻断血管紧张素,48小时候后患者再次出现脑病症状(GCS = 6)。 他的CT扫描仍是阴性的,EEG与之前的相似;血氨浓度急剧上升至990 μg/dL。患者入住重症监护病房(ICU),在此病情成功得到治疗。

表 1. 入院以及两次肝性脑病时的血液检测和血气分析
此时再次阻断血管紧张素(第3次),添加最大量的乳果糖治疗(口服和灌肠)以及口服利福昔明。那时患者是清醒的,虽然他没有感觉,并且脱离了周围环境。4 天后,停用ACEI和ARB,神经功能完全恢复。患者出院,此后10周仍无症状,没有再次发作肝性脑病,反复检测血氨浓度都是低的(正常)。
讨论与结论
上世纪80年代,随着ACEI和ARB这两大类药物被批准上市,引入了针对肾素-血管紧张素系统控制血压的方法。ACEI是一种可阻止血管紧张素 I(ATI)转换为血管活性血管紧张素酶II (ATII)的药物,而ARB可抑制参与血管收缩、醛固酮分泌以及钠重吸收的ATI受体。这两种药物显示出相似的疗效特征,因此,最近对初始治疗该选这两种降压药物中的哪一种产生了争议[3]。
几项在人类中进行的临床试验旨在研究这些药物单用或联用时控制高血压[4,5]、心力衰竭[6,7]和蛋白尿肾病[2]的效应。大部分结果证实ACEI和 ARB联合疗法可轻度改善高血压控制[4],如果同时存在肾脏受损,则可明确减少蛋白尿[8,9]。然而,ACEI和ARB联合疗法会引起低血压发生率升高[6,7]、中至重度高钾血症[7]以及肾脏预后不良[2],其中后者主要报告于无蛋白尿的患者,这使得必须重新考虑权衡该联合疗法的风险(增加血肌酐)和益处(减少蛋白尿)。必须对高钾血症、肾小球滤过率过度降低以及并发症(例如急性肾衰竭)可能恶化等肾脏副作用进行更多和更系统的评价。因此,建议慎用该联合疗法,直至几项正在进行中有特定肾脏终点的试验(血管紧张素受体拮抗剂和血管紧张素转换酶抑制剂联用治疗糖尿病肾病的设计(VA NEPHRON-D),检验常染色体显性多囊肾病新疗法的方法:来自CRISP 和 HALT-PKD研究的认识,以及抑制RAS对心肾结局的长期影响(LIRICO)的随机试验研究方案)得出结果。
就我们所知,本病例首次描述了ACEI和ARB联合疗法的一种致命不良效应,该效应可能与该门脉高压患者肝功能异常有关。我们推断这种不良反应可能与ATII影响血氨排泄直接相关,但是共病和多药治疗的影响也不能排除。
如以前对动物模型的描述[10],ATII是控制近曲小管氨生成和排泄必不可少的。虽然通过药物阻断人肾素-血管紧张素系统对血氨浓度的影响目前仍未明确,我们的病例提示通过双肾的排泄总体上是减少的。反之,肾排泄减少解释了这名因同时患肝硬化和严重门脉高压(图 1)导致易感性增加的患者检测到血氨浓度突然升高的原因。我们建议,肝硬化和门脉高压患者用ACEI和ARB联合疗法时,应认真进行临床随访,可能还需要监测血氨浓度。应严格评估这些高风险患者用普通治疗相关的严重副作用的发生率。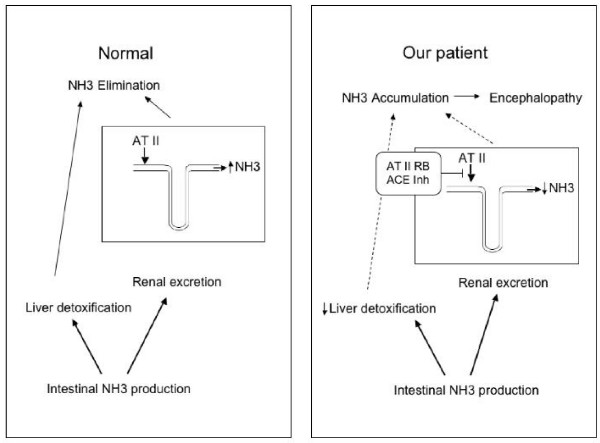
图1 健康对照者血氨排泄由两种机制介导:肝解毒和肾排泄。肾排泄由近曲小管水平的血管紧张素II (ATII)调节。我们病例中的患者因患肝硬化,肝脏机制已被破坏,这使得肾脏途径是清除氨所必需的。联用血管紧张素转换酶抑制剂和血管紧张素II受体拮抗剂抑制了ATII的活性,从而阻止了肾脏充分排泄,导致血氨浓度突然上升以及上述神经系统并发症。
参考文献:
[1] Mogensen CE, Neldam S, Tikkanen I, Oren S, Viskoper R, Watts RW, Cooper ME: Randomised controlled trial of dual blockade of renin-angiotensin system in patients with hypertension, microalbuminuria, and non-insulin dependent diabetes: The candesartan and lisinopril microalbuminuria CALM study.BMJ 2000 , 7274:1440-1444.
[2] Mann JF, Schmieder RE, McQueen M, Dyal L, Schumacher H, Pogue J, Wang X, Maggioni A, Budaj A, Chaithiraphan S, Dickstein K, Keltai M, Metsarinne K, Oto A, Parkhomenko A, Piegas LS, Svendsen TL, Teo KK, Yusuf S: Renal outcomes with telmisartan, ramipril, or both, in people at high vascular risk (the ONTARGET study): A multicentre, randomised, double-blind, controlled trial.Lancet 2008 , 9638:547-553.
[3] Matchar DB, McCrory DC, Orlando LA, Patel MR, Patel UD, Patwardhan MB, Powers B, Samsa GP, Gray RN: Systematic review: Comparative effectiveness of angiotensin-converting enzyme inhibitors and angiotensin II receptor blockers for treating essential hypertension.Ann Intern Med 2008 , 1:16-29.
[4] Doulton TW, He FJ, MacGregor GA: Systematic review of combined angiotensin-converting enzyme inhibition and angiotensin receptor blockade in hypertension.Hypertension 2005 , 5:880-886.
[5] Weir MR, Smith DH, Neutel JM, Bedigian MP: Valsartan alone or with a diuretic or ACE inhibitor as treatment for African American hypertensives: Relation to salt intake.Am J Hypertens 2001 , 7(Pt 1):665-671.
[6] Cohn JN, Tognoni G: A randomized trial of the angiotensin-receptor blocker valsartan in chronic heart failure.N Engl J Med 2001 , 23:1667-1675.
[7] Yusuf S, Teo KK, Pogue J, Dyal L, Copland I, Schumacher H, Dagenais G, Sleight P, Anderson C: Telmisartan, ramipril, or both in patients at high risk for vascular events.N Engl J Med 2008 , 15:1547-1559.
[8] Nakao N, Yoshimura A, Morita H, Takada M, Kayano T, Ideura T: Combination treatment of angiotensin-II receptor blocker and angiotensin-converting-enzyme inhibitor in non-diabetic renal disease (COOPERATE): A randomised controlled trial.Lancet 2003 , 9352:117-124.
[9] Kunz R, Friedrich C, Wolbers M, Mann JF: Meta-analysis: Effect of monotherapy and combination therapy with inhibitors of the renin angiotensin system on proteinuria in renal disease.Ann Intern Med 2008 , 1:30-48.
[10] Nagami GT: Ammonia production and secretion by S3 proximal tubule segments from acidotic mice: Role of ANG II.Am J Physiol Renal Physiol 2004 , 4:F707-712.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#联合疗法#
70
#脑病#
77
#抑制剂#
96
#病例报告#
129
#血管紧张素II#
71
#拮抗剂#
77
#血管紧张素转换酶抑制剂#
79
#血管紧张素#
49