重磅!Cell发布抗病毒药物综述,如何应对下一次新发病毒流行?
2021-03-19 JACKZHAO MedSci原创
复旦大学姜世勃/陆路团队以及上海科技大学杨海涛研究员共同发表在《细胞》(Cell)杂志的综述回顾了目前主流抗病毒药物的共同靶点以及具有共同靶点的抗病毒药物的开发,为新发病毒的抗病毒药物提供线索。

Antivirals with common targets against highly pathogenic viruses,https://doi.org/10.1016/j.cell.2021.02.013
3月19日,《细胞》(Cell)杂志在线发表复旦大学姜世勃/陆路团队以及上海科技大学杨海涛研究员共同研究综述,本综述回顾了目前主流抗病毒药物的共同靶点以及具有共同靶点的抗病毒药物的开发,这将为开发针对未来可能出现的新发病毒的抗病毒药物提供线索。
新发病毒在人类历史上不断出现,累计已造成数千万人死亡。当前,气候变化和全球化都为病毒传播创造了更有利的条件。未来,新发病毒的暴发可能更为频繁。因此,开发有效的抗病毒药物,尤其是针对不同病毒中的保守靶点的广谱抗病毒药物,来对抗未来可能暴发的新发和再现病毒是目前学术界以及产业界普遍关心的议题。
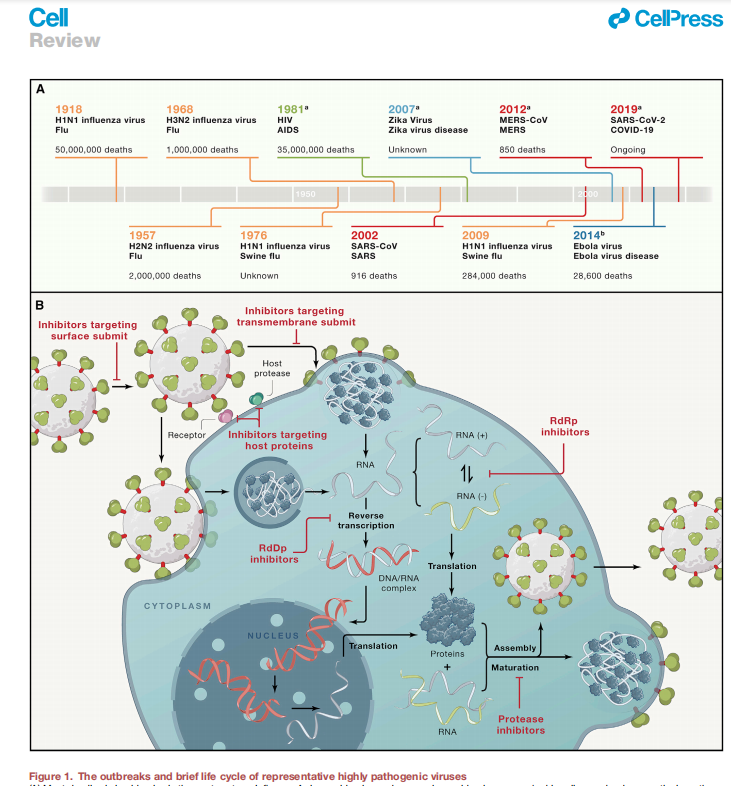
代表性高致病性病毒的爆发及其生命周期
抗病毒药物共性靶点
在所有病毒或者同一病毒属中,执行相同功能的蛋白质序列和结构往往高度相似,如SARS-CoV和SARS-CoV-2的刺突蛋白结构就高度相似。这些蛋白质通常可作为抗病毒药物开发的共性靶点。首先,病毒通过受体识别以及膜融合或内吞等步骤进入靶细胞,开启生命周期。该过程中,介导病毒与细胞受体识别的病毒表面蛋白(surface protein, SP)的受体结合亚基、介导膜融合的病毒SP跨膜亚基、细胞上的受体、切割SP所需的宿主细胞蛋白酶等均是常见的抗病毒靶点。病毒进入靶细胞后,病毒基因组DNA/RNA被释放到细胞中,作为模板指导病毒蛋白的合成。一些病毒前体蛋白需要经过病毒蛋白酶切割,所以病毒蛋白酶也是重要的抗病毒靶点。病毒基因组也在同步发生复制, RNA病毒的基因组复制需要RNA依赖的RNA或DNA聚合酶(RdRp和RdDp),这类酶在人体中不存在,因此是理想的抗病毒靶点。新合成的病毒基因组与病毒蛋白组装成新的病毒颗粒,通过出芽或细胞运输通路释放到细胞外。
1. 针对病毒表面蛋白(SP)表面亚基(surface subunit, SfS)的病毒进入抑制剂
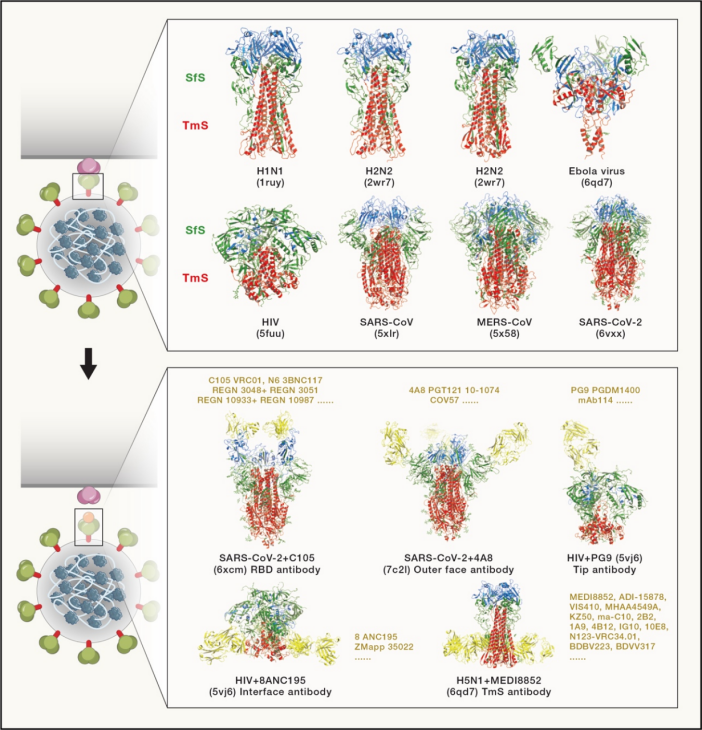
靶向病毒SfS的病毒进入抑制剂包括:来源于靶细胞受体的蛋白和多肽、靶向病毒受体结合域以阻断SP与受体的结合或者靶向非结合域引起SP构象变化以阻断SP与受体结合的小分子化合物、多肽以及抗体。其中的代表药物是2020刚刚上市的HIV药物Rukobia (fostemsavir, BMS-663068)以及在COVID-19疫情中获得紧急使用批准的再生元和礼来公司的SARS-CoV-2抗体。但是病毒SfS通常处于高突变压力下,所以针对该靶点的抑制剂很难开发成广谱抗病毒药物。因此,为应对新发病毒暴发的紧急情况,我们需要建立起靶向SfS的抗病毒药物的快速筛选和安全性评估体系。
2. 针对病毒SP跨膜亚基(transmembrane subunit, TmS)的病毒进入抑制剂
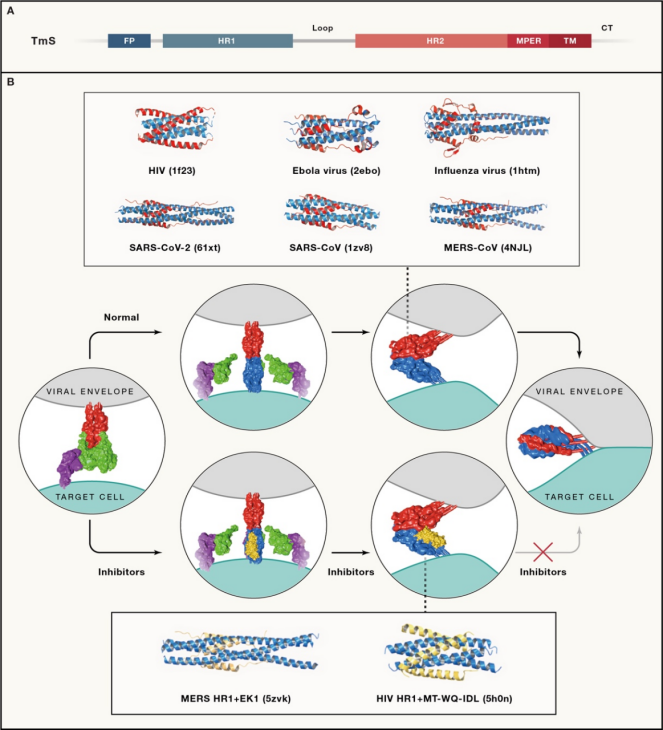
I类融合蛋白的TmS结构和功能高度相似,大致分为融合肽(FP)、七肽重复序列1(HR1)、七肽重复序列2(HR2)、近膜区域(MPER)、跨膜区域(TM)和 胞内区(CT)。病毒进入靶细胞过程中,FP负责插入宿主细胞膜,HR1与同源HR2相互作用形成六螺旋束(6-HB)。 6-HB的形成将病毒和靶细胞膜拉近以进行融合。靶向病毒TmS的抑制剂包括:针对FP、HR1及HR2、MPER及CT的小分子化合物、多肽以及抗体。其中代表药物为HIV药物T20 (Fuzeon, enfuvirtide),通过结合HIV的HR1区来阻断病毒与靶细胞胞膜融合。与SfS相比,TmS序列在同属病毒中更保守,使得这些蛋白成为开发针对同属病毒的广谱抑制剂的可能靶点。
3. 靶向宿主蛋白的病毒进入抑制剂
靶向宿主蛋白的病毒进入抑制剂包括:靶向细胞受体(或共受体)、宿主蛋白酶、内吞途径的小分子化合物、多肽以及抗体。代表性药物为HIV药物maraviroc(Selzentry)和ibalizumab(TMB-355),分别为靶向HIV共受体和受体的小分子化合物和抗体。针对宿主蛋白酶和内吞途径的药物是新发病毒暴发时筛选“老药新用”的重要来源,但因其靶向宿主的功能性蛋白,相较作用于病毒蛋白的药物作用机制更为复杂,在运用于治疗新发病毒时,仍需要经过详细的安全性和有效性的评估。
4. 针对RNA依赖的RNA聚合酶(RdRp)和RNA / DNA依赖的DNA聚合酶的病毒复制抑制剂
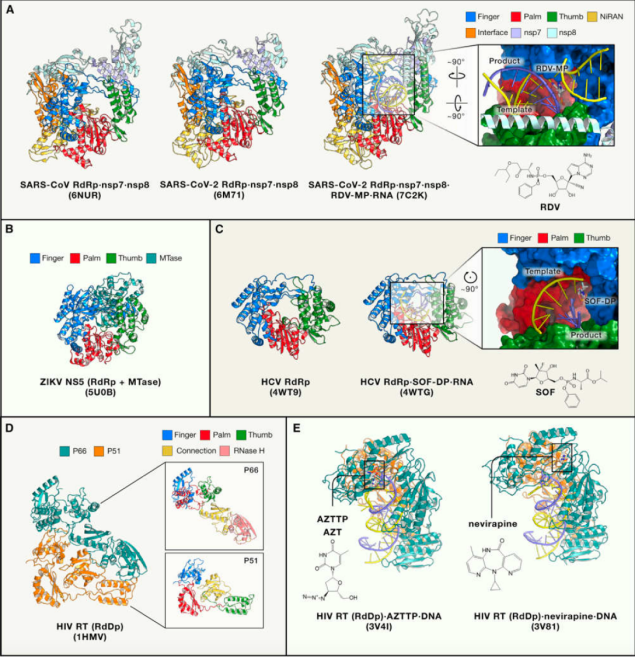
该类药物需要进入细胞发挥作用,所以目前只包括小分子化合物。该类药物中的favipiravir、sofosbuvir(SOF)、zidovudine(AZT) 、nevirapine、ribavirin等药物均是临床上使用已久的抗病毒药物,且很多具有广谱抗病毒活性,说明DNA或者RNA聚合酶是真正意义上的广谱药物靶点。RdRp抑制剂可储备为针对RNA病毒的广谱药物,如RdRp抑制剂瑞德西韦(remdesivir, RDV)就在本次COVID-19流行中被批准紧急使用;RdDp抑制剂可储备为针对逆转录病毒的广谱药物;DdDp抑制剂则可储备为针对DNA病毒的广谱药物。
5. 针对病毒蛋白酶的病毒复制抑制剂
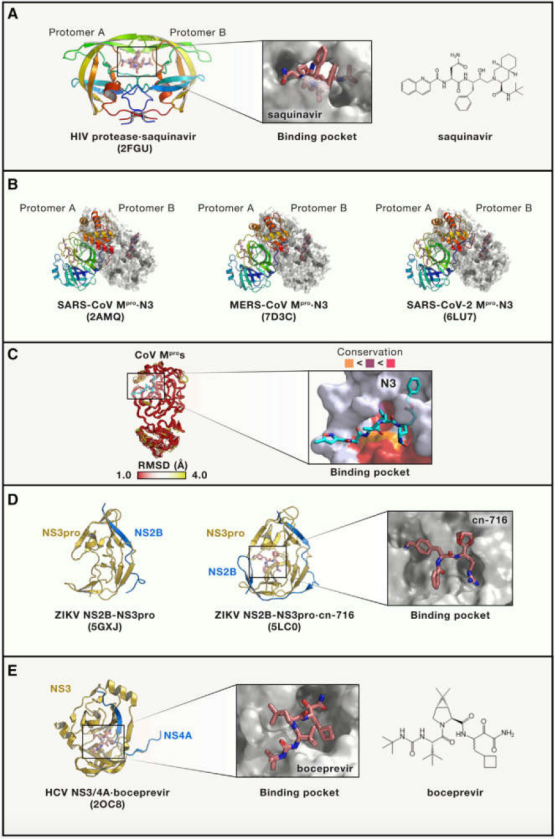
该类抑制剂包含众多已上市的HIV以及HCV治疗药物,如saquinavir、ritonavir、boceprevir,、telaprevir等,均为针对相应病毒蛋白酶的小分子抑制剂。由于不同病毒的蛋白酶不同,所以病毒蛋白酶类抑制剂没有DNA/RNA聚合酶抑制剂广谱,但是也具有开发成针对同属病毒的广谱抑制剂的潜力。
目前,仅有靶向病毒DNA/RNA聚合酶的核苷类似物,例如ribavirin和favipiravir,以及靶向宿主蛋白的化合物,可以用作针对一大类病毒的广谱抗病毒药物。来自同一病毒属的病毒通常含有几个高度保守的表位,如TmS和病毒蛋白酶,可以作为同属广谱抗病毒药物开发的靶点。例如,在COVID-19暴发之前开发的针对冠状病毒TmS的病毒抑制剂--EK1也显示出针对SARS-CoV-2的抗病毒活性,表明针对同属病毒提前设计广谱抑制剂的可行性。文章总结道,由靶向DNA/RNA聚合酶的广谱病毒药物和2-3种针对SP跨膜亚基或病毒蛋白酶等同属内广谱靶点的药物组成的鸡尾酒疗法可作为治疗相应病毒属的新发病毒的储备方案。
文章通过剖析各靶点的优势与劣势以及广谱性的差异,作者最后提出了新发病毒三层次药物策略。
第一层次:如果经过序列鉴定发现新发病毒来自已知病毒属,且与现有的同属病毒同源性较高,则可由储备的针对该属病毒的鸡尾酒疗法加以治疗。这种新发病毒出现的可能性较大,因此全球可针对现有病毒属联合开发有效药物进行储备。
第二层次:如果该新发病毒来自已知病毒属,但是与同属病毒同源性低,则可以首先尝试使用靶向DNA/RNA聚合酶的广谱病毒抑制剂,如ribavirin和favipiravir等进行治疗。同时,需要通过已经建立的快速筛选技术鉴定新的抗病毒药物。抗病毒药物常用靶点蛋白质(例如SP、SfS或受体结合域)可被用于筛选。
第三层次:对于完全未知的新发病毒,由于缺少参考模板,我们可能无法在短时间内确定该未知病毒的SP序列等序列,从而较难研发抗体等特异性药物。
在这种情况下,我们可能需要使用整个病毒作为诱饵,或者直接测试患者B细胞培养上清的抗病毒活性,以在不完全了解其特定表位的情况下找到有效的中和抗体。对于该情况,可能需要加强和完善快速、高质量的病毒分离纯化及细胞感染模型建立等技术。
总之,在新发病毒暴发期间,储备的广谱抗病毒药物将是第一道防线。快速的筛选系统,加上可靠的安全性和有效性评估体系,将构成第二道防线。
原文出处:
Lu Lu,Shan Su,Haitao Yang,and Shibo Jiang,CELL, Antivirals with common targets against highly pathogenic viruses,https://doi.org/10.1016/j.cell.2021.02.013
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#Cell#
84
#CEL#
89
#抗病毒#
99
#抗病毒药物#
118
#重磅#
82
学习
143
学习,抗病毒药物是第一道防线,疫苗是最后胜出的武器
140
在新发病毒暴发期间,储备的广谱抗病毒药物将是第一道防线。快速的筛选系统,加上可靠的安全性和有效性评估体系,将构成第二道防线。
167