读书报告 | DeLLphi-301研究:塔拉妥单抗后线治疗广泛期小细胞肺癌
2024-07-30 iCombo iCombo 发表于上海
该研究显示出Tarlatamab在既往治疗过的小细胞肺癌患者中的抗肿瘤活性、持久的客观反应和有希望的生存结果。
导读
小细胞肺癌是一种高侵袭性疾病,虽然大多数晚期小细胞肺癌患者对初始治疗有反应,但通常在几个月内发生进展。二线治疗选择有限,反应持续时间较短(3.6-5.3个月),总生存期很少超过8个月。
塔拉妥单抗2024nian(Tarlatamab)是一种双特异性T细胞结合免疫治疗药物,主要靶向DLL3和CD3。Tarlatamab可以使肿瘤细胞上的DLL3和T细胞上的CD3结合,导致T细胞介导的肿瘤溶解。
DeLLphi-301是一项2期临床试验,旨在评估Tarlatamab的在小细胞肺癌中的抗肿瘤活性、安全性、副作用和药代动力学。纳入的患者为既往接受过多线治疗的小细胞肺癌患者,Tarlatamab为每2周静脉给药,剂量为10 mg或100 mg。主要终点是客观缓解。
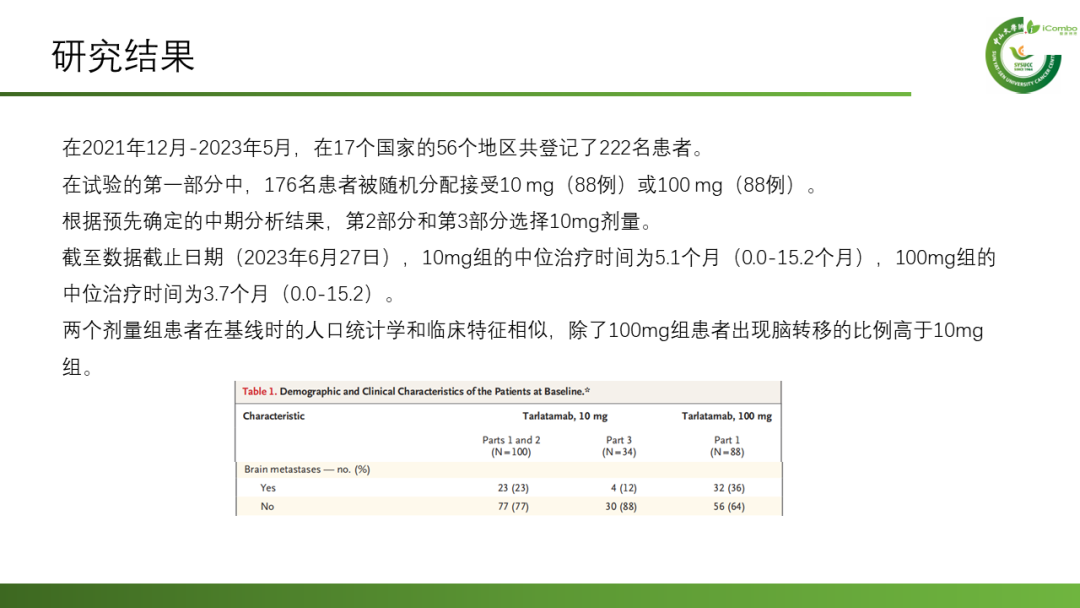
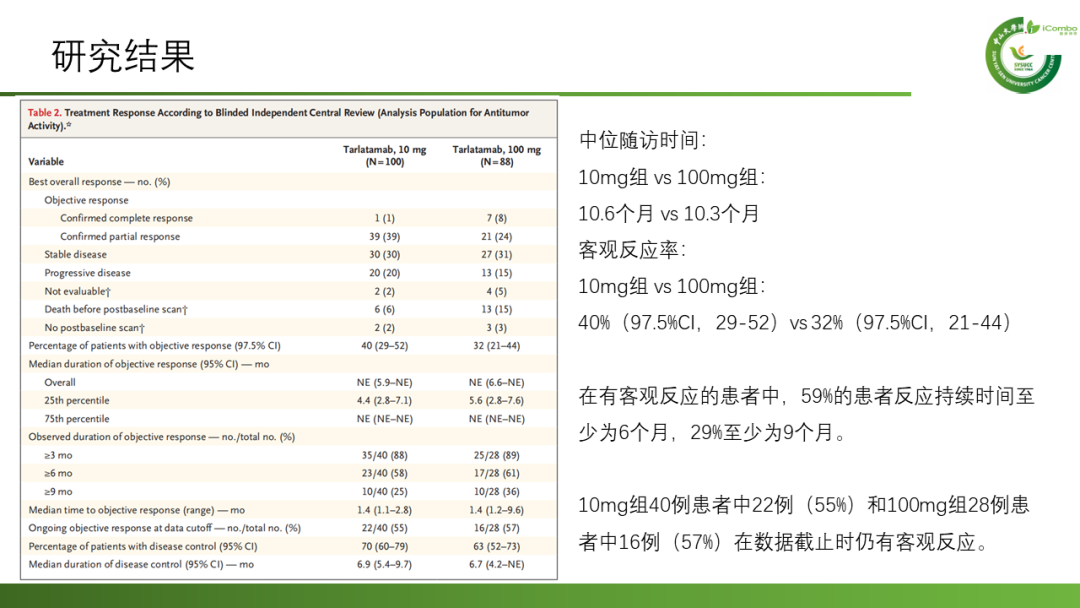
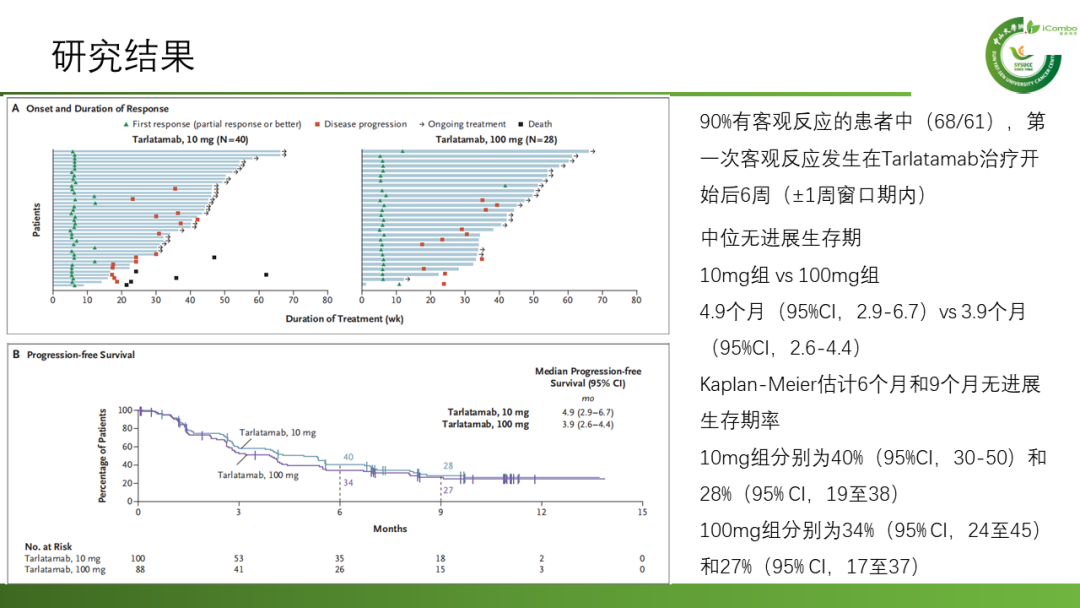
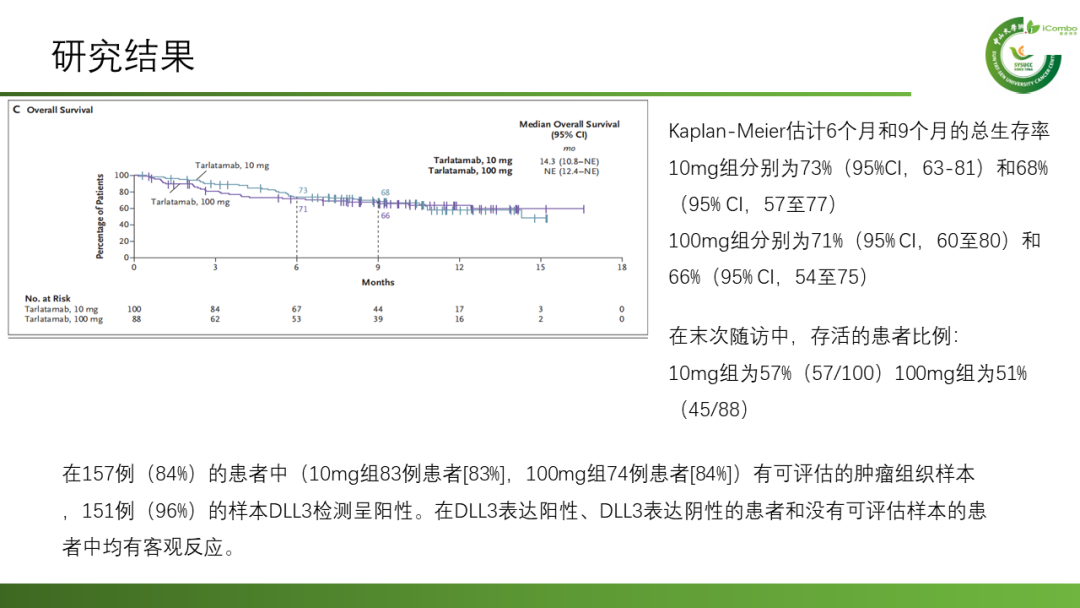
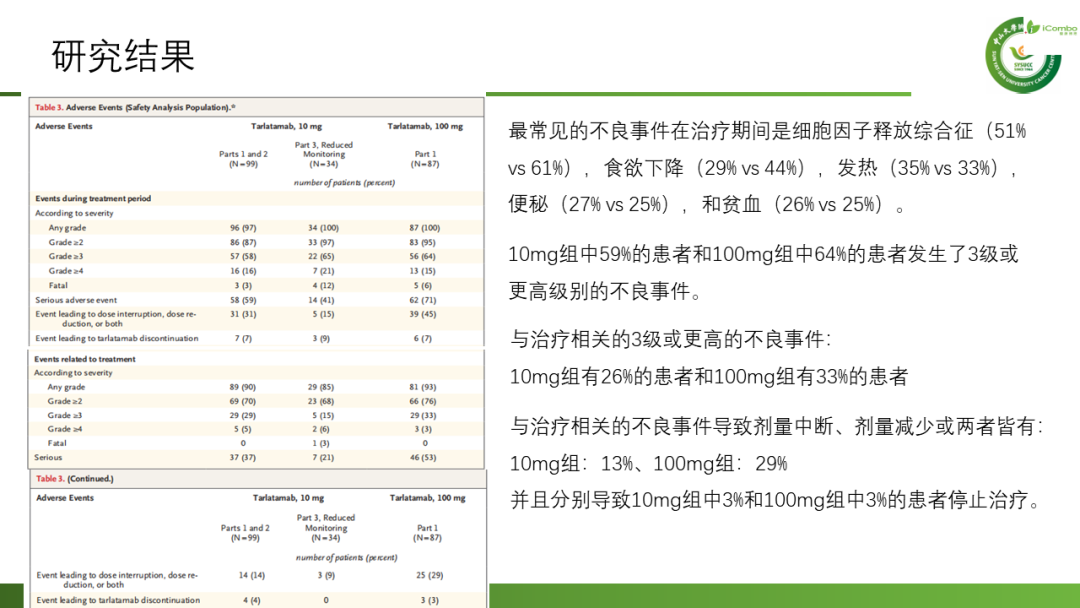
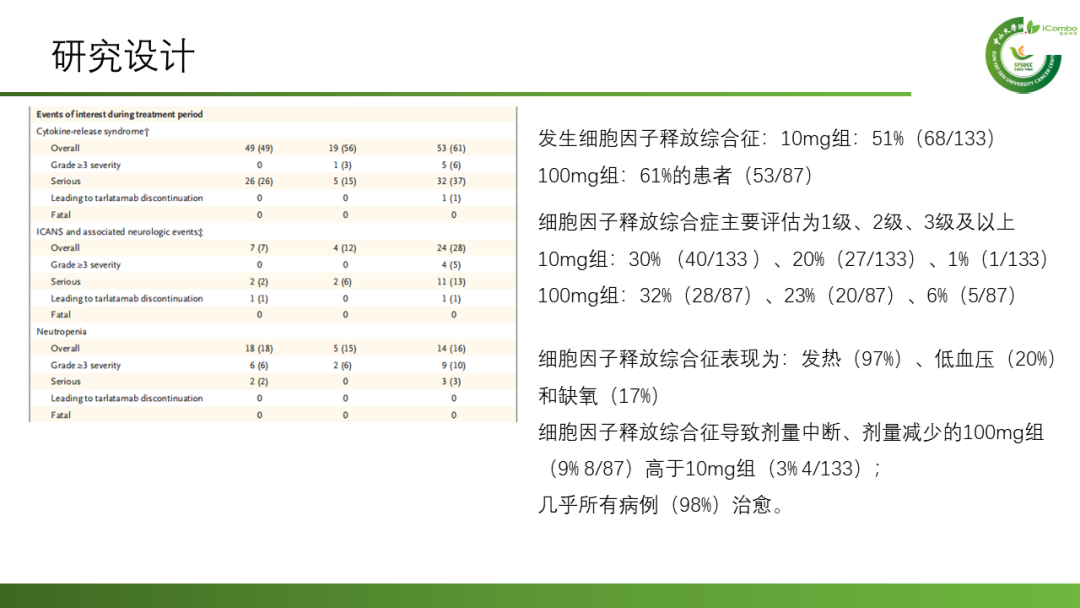
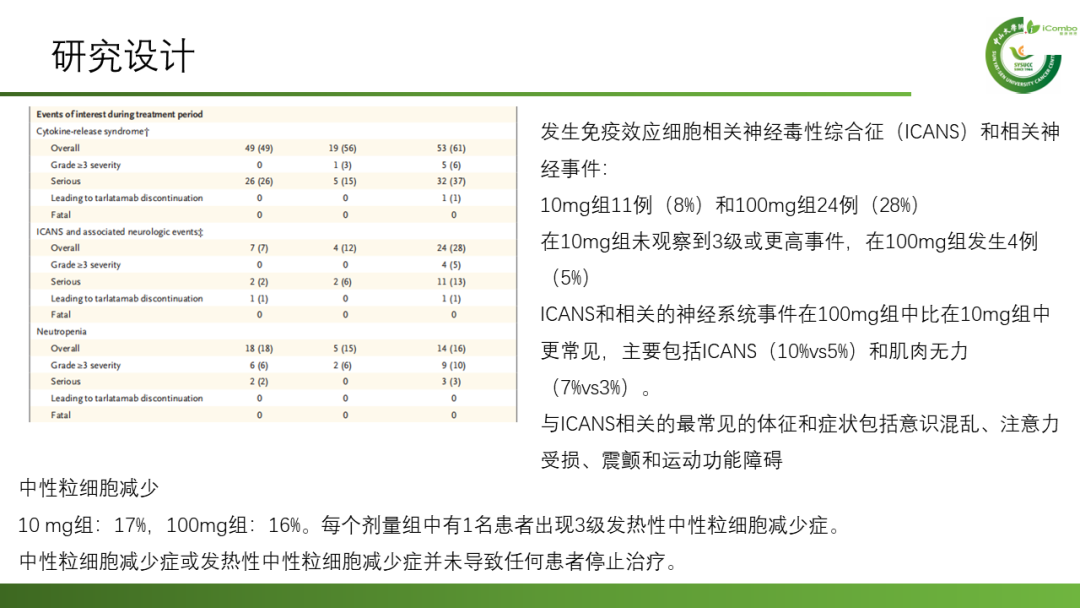
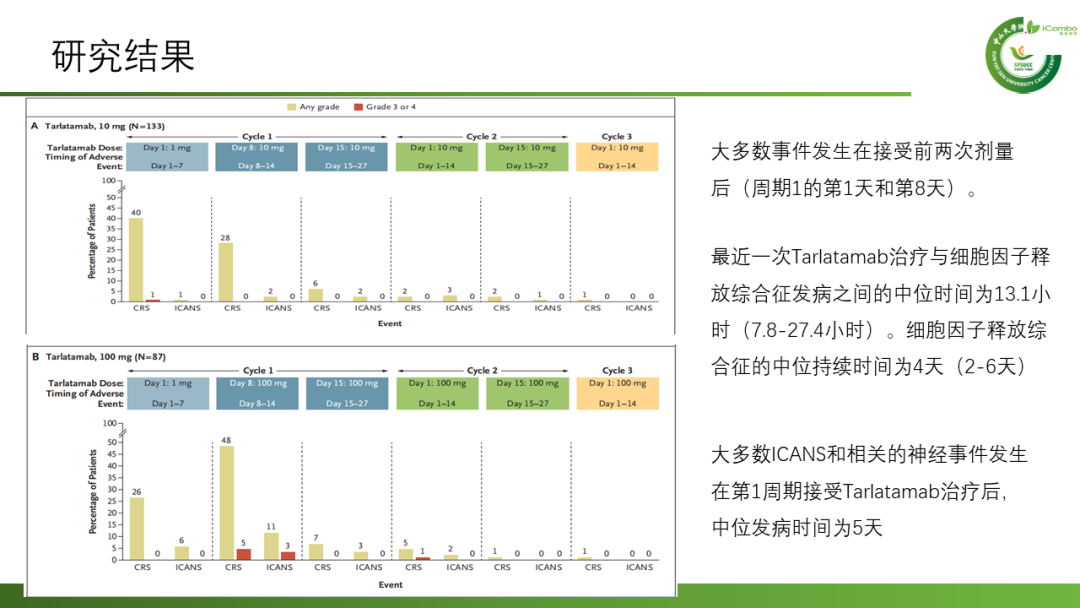
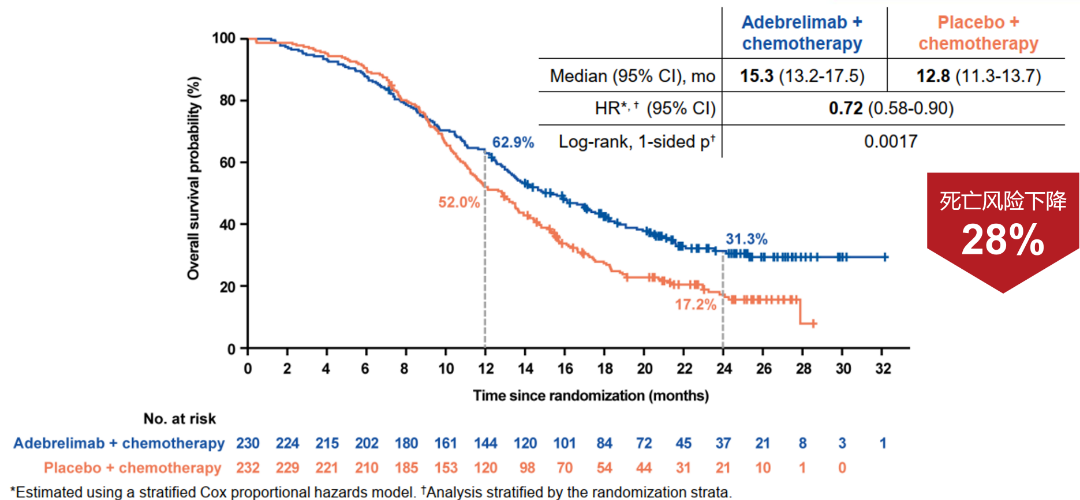
共有220名患者接受了Tarlatamab治疗,10mg组的中位随访时间为10.6个月,100mg组为10.3个月。10mg组的中位无进展生存期为4.9个月(95% CI2.9-6.7),100mg组为3.9个月(95%CI2.6-4.4);9个月的总生存期分别为68%和66%。10mg组中40%(97.5%CI:29-52)的患者,100mg组中32%(97.5% CI:21-44)的患者出现了客观反应。不良反应方面:最常见的是细胞因子释放综合征(10mg组:51%,100mg组:61%)、食欲下降(分别为29%和44%)和发热(35%和33%)。10mg组(1%)中3级细胞因子释放综合征的发生率低于100mg组(6%)。较低比例的患者(3%)因治疗相关不良事件停用Tarlatamab。
该研究显示出Tarlatamab在既往治疗过的小细胞肺癌患者中的抗肿瘤活性、持久的客观反应和有希望的生存结果。2024年5月美国FDA批准Tarlatamab后线治疗广泛期小细胞肺癌(N Engl J Med. 2023 Nov 30;389(22):2063-2075. doi: 10.1056/NEJMoa2307980)。







本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#广泛期小细胞肺癌# #塔拉妥单抗#
54