Cancer Cell 重磅揭示全球首个早期肺癌头对头对比MRD检测策略的前瞻性临床研究结果
2023-09-13 测序中国 测序中国 发表于上海
该研究在全球范围内首次建立了Landmark MRD状态联合TNM分期指导患者预后分层的TNMB分期方法,以及ctDNA定量变化率可指导临床治疗决策等新的MRD应用策略。
近日,由北京大学人民医院胸外科/胸部肿瘤研究所王俊院士团队的陈克终教授引领的全球首个早期肺癌头对头对比分子残留病灶(molecular residual disease,MRD)检测策略的前瞻性临床研究MEDAL(NCT03634826)的相关研究结果正式发表于Cancer Cell[1]。

MEDAL系列研究历时长达5年,此次公布的研究结果聚焦早期可手术的非小细胞肺癌患者,对比了肿瘤未知(tumor-agnostic,不依赖肿瘤组织检测信息)的固定化Panel、肿瘤先验(tumor-informed,基于肿瘤组织检测)的固定化Panel、基于WES的个性化定制MRD Panel(PROPHET)的三种MRD策略的检测性能。其中,固定化Panel(LungPlasma Panel)在2021FDA MAQC协会领导和发布的SEQC2研究(考核二代基因测序技术的临床应用标准和质量管理措施)的血液检测能力测评的报告中显示出优异的灵敏度、特异性、准确性、可重复性和稳定性[2]。
更为重要的是,该研究创新性地解答了MRD临床应用转化中的常见问题,如MRD监测策略、非Ⅰ/Ⅱ类变异的MRD检测价值、个性化的MRD检测在复发监测较传统影像学检测的领先时间等。同时,该研究在全球范围内首次建立了Landmark MRD状态联合TNM分期指导患者预后分层的TNMB分期方法,以及ctDNA定量变化率可指导临床治疗决策等新的MRD应用策略。
1 PROPHET(基于WES的个性化定制MRD Panel)在早期肺癌患者中的检测性能显著优于2种固定化Panel
分析验证结果表明,基于WES检测、包含50个定制化位点设计的个性化定制MRD Panel(PROPHET)在20 ng DNA投入量、100,000×的原始测序深度的情况下,LOD可达到0.0036%,实现稳定检出十万分位LOD。术前血检测结果表明,个性化定制MRD Panel的敏感性显著高于两种固定化MRD检测。相较于其他两种方法学,个性化定制MRD Panel能多检出30例MRD阳性患者,且中位ctDNA fraction显著低于3种方法均检出阳性的患者。值得注意的是,这些患者96.9%个性化定制MRD Panel检测到的突变未包含在固定Panel中,进一步说明个体化定制MRD的必要性。
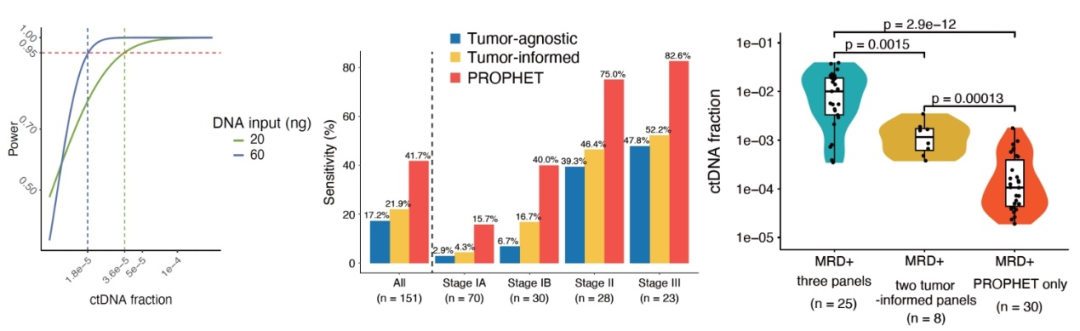
图1:20 ng和60 ng DNA投入量时,PROPHET LOD分别为0.0036%和0.0018%(左);三种不同策略检测不同临床分期患者术前血浆的敏感性(中);MRD阳性患者中位ctDNA fraction(右)
同时,Landmark 检测中个性化定制MRD Panel显示出比另外两种固定Panel更好的预测性能(HR:16.4 vs 4.26 vs 4.68)。
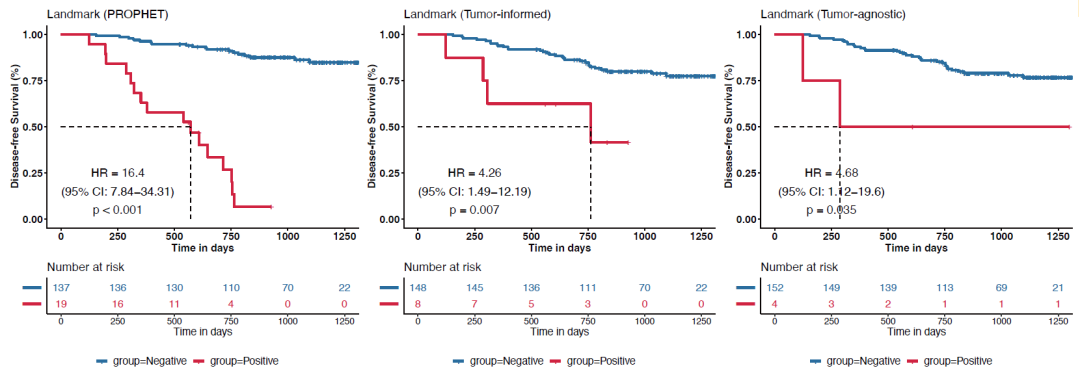
图2:Landmark 检测中,个性化定制Panel较2种固定化Panel策略可更好区分患者DFS
2 在TNM分期上正式明确了Blood在预后中的价值,国际首次建立TNMB分期,为未来其他实体瘤分期做出重要参考
个性化定制MRD Panel在Landmark 检测点出色的预后能力,该研究提出了一个新的预后分层工具-TNMB分期,即在经典的临床TNM分期的基础上结合术后一个月MRD血检的分子检测结果,用于早期肺癌更加精准的预后分层。在MEDAL中,TNMB分期显示出比TNM分期更精准的预后分层,并通过其他公开队列进行了样本量的扩大验证,肺癌TNMB分期有望为未来其他实体瘤更精准的分期做出重要参考。
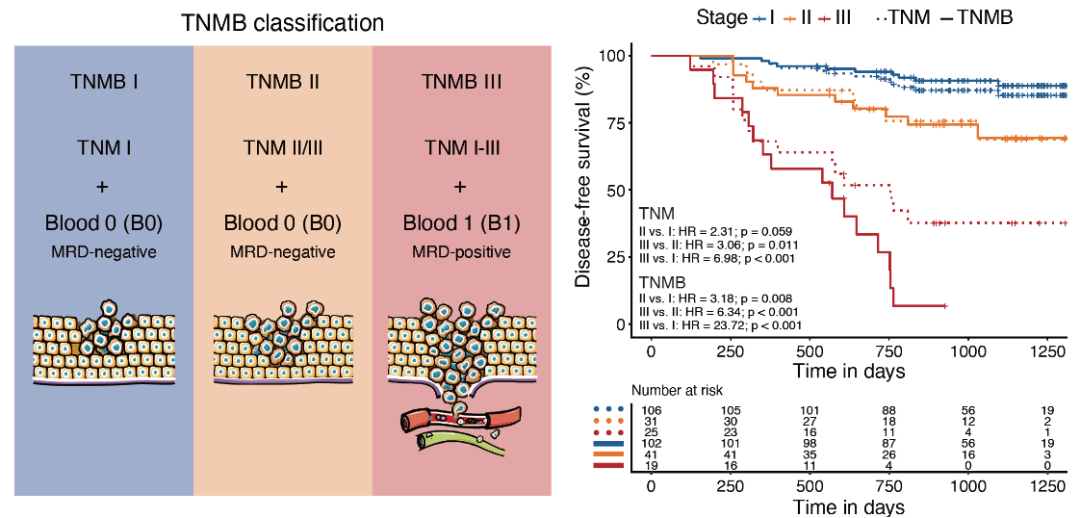
图3:结合TNM分期和Landmark PROPHETMRD检测结果的TNMB分期(左);术后三十天,TNMB和TNM分类的DFS分析(右)
3 非Ⅰ/Ⅱ类变异与Ⅰ/Ⅱ类变异在MRD预后价值、辅助临床诊断上均具有重要意义
研究发现,追踪Ⅰ/Ⅱ类变异或非Ⅰ/Ⅱ类变异对于MRD检测均具有重要意义:接近一半的MRD阳性仅依靠非Ⅰ/Ⅱ类变异识别,并与Ⅰ/Ⅱ类变异识别的MRD阳性具有相似的预后预测效能。该研究中的MEDAL-010案例显示,当出现模棱两可的影像学诊断时,患者在253天基于PROPHET通过非Ⅰ/Ⅱ类变异判定的MRD阳性可以辅助临床判断疾病复发。
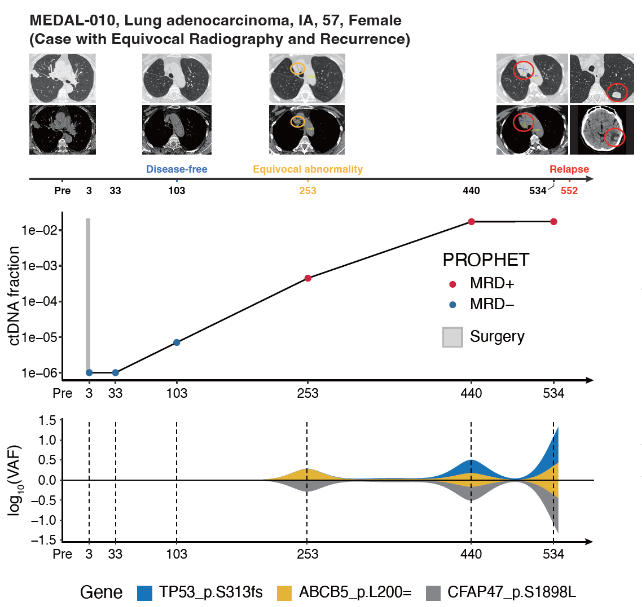
图4:通过非Ⅰ/Ⅱ类变异判定MRD阳性并出现复发的案例
4 首次提出ctDNA定量变化率可更好指导临床治疗决策
为了探索ctDNA定量能力的临床效用,研究团队在Longitudinal分析中定义了相邻测试之间ctDNA定量变化率(dynamic changing rate,DCR)。根据PROPHET的检测结果,在MRD阳性受试者中,复发受试者的ctDNA DCR显著高于未复发受试者,这一现象并未在MRD阴性受试者中观察到。这提示我们,基于个体化定制MRD检测,ctDNA定量变化率或为预测患者预后带来新的参考维度。
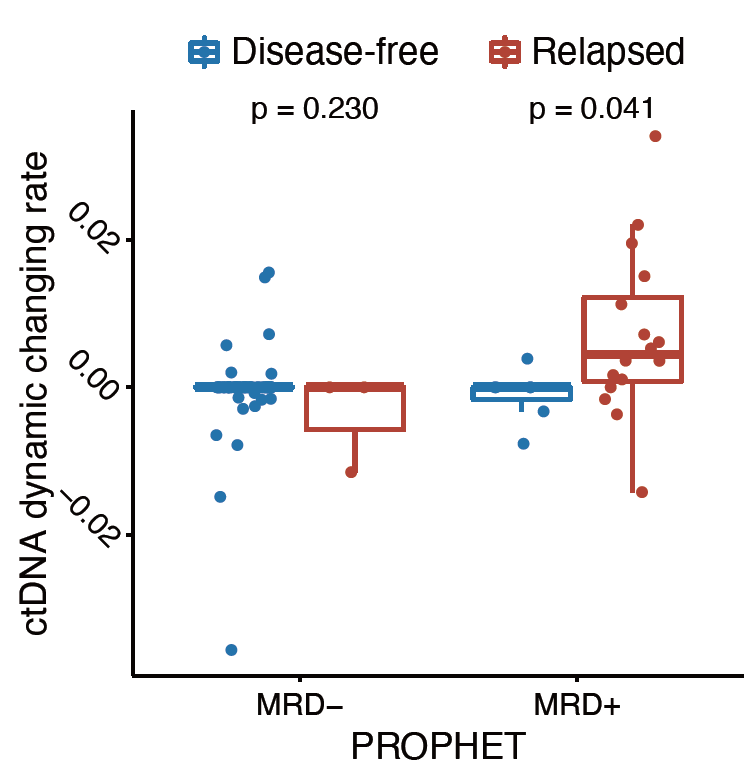
图5:Longitudinal分析中所有患者MRD状态和DFS状态的ctDNA定量变化率
5 PROPHET 2年动态监控的NPV高达95.5%,较影像学中位预警复发时间提前299天
在Longitudinal监测策略分析时,如果在任何时间点上MRD呈阳性,研究团队定义患者为Longitudinal MRD阳性。Longitudinal监测结果发现:
PROPHET监测MRD阳性与DFS显著相关,风险比为37.42(p < 0.001),敏感性为84.2%(16/19),阴性预测值为96.6%(84/87),均优于Landmark MRD;Longitudinal监测中,个性化定制MRD Panel的PROPHET再次显示出比两种固定Panel更好的预测性能(HR:37.42 vs 7.1 vs 5.12);
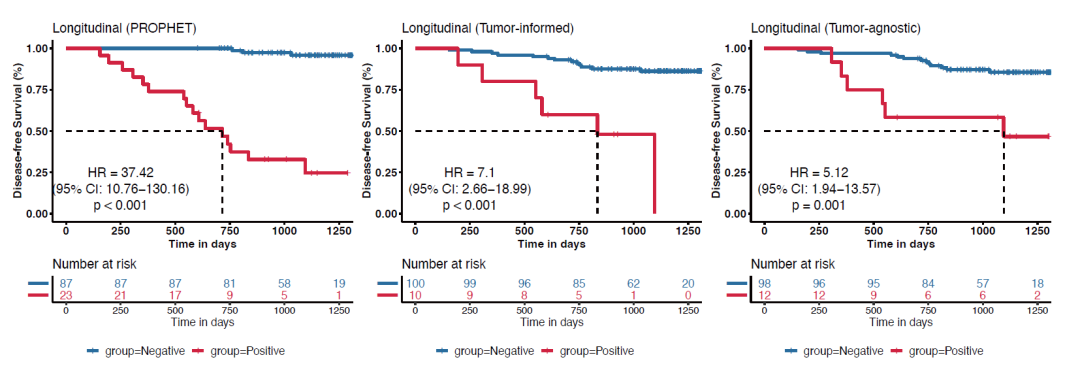
图6:Longitudinal监测中,个性化定制MRD Panel较2种固定化MRD策略可更好区分患者DFS
PROPHET监测到的MRD阳性中位超前时间较影像学中位预警复发时间提前299天,而tumor-informed固定化 Panel监测复发患者的超前时间为95天,tumor-agnostic固定化 Panel复发患者的超前时间为129天。这意味着,对比影像学,个体化定制MRD Panel可带来中位近10个月的lead time;
PROPHET在第180天、360天和720天,动态MRD监测的NPV高达99.4%、98.4%和95.5%。
即使是ctDNA non-shedder人群,PROPHET也可预测其复发风险。Non-shedder受试者中,对比MRD阴性患者,MRD阳性患者的预后较差。
MEDAL作为一项为期5年的系列性临床研究,继前期在技术维度进行了全球首个甲基化MRD的突破之后[3],此次又为临床带来了基于液体活检技术MRD检测策略的临床解决方案。基于在MEDAL中的发现,研究人员已经启动了一个全国性的前瞻性III期随机对照试验(ChiCTR2200061108),探索由MRD状态和TNM分期综合指导下的辅助治疗。从技术到临床全方位的液体活检组合拳解决方案,将切实助力肿瘤的临床精准诊治。
参考文献:
1.Chen et al., Individualized tumor-informed circulating tumor DNA analysis for postoperative monitoring of non-small cell lung cancer, Cancer Cell (2023), https://doi.org/10.1016/j.ccell.2023.08.010
2.Deveson, I.W., Gong, B., Lai, K. et al. Evaluating the analytical validity of circulating tumor DNA sequencing assays for precision oncology. Nat Biotechnol 39, 1115–1128 (2021).
https://doi.org/10.1038/s41587-021-00857-z
3.Chen, K., Kang, G., Zhang, Z. et al. Individualized dynamic methylation-based analysis of cell-free DNA in postoperative monitoring of lung cancer. BMC Med 21, 255 (2023).
https://doi.org/10.1186/s12916-023-02954-z
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言