Cancer Immunol Immunother:肿瘤突变评分(TMS)取代肿瘤突变负荷(TMB)预测NSCLC患者对ICI治疗的反应性?
2021-02-05 Nebula MedSci原创
肿瘤突变负荷(TMB)位置不保,肿瘤突变评分(TMS)更准确、更经济!
免疫检查点抑制剂(ICI)逐渐成为癌症治疗的最新技术,并已为晚期癌症患者(尤其是非小细胞肺癌[NSCLC])的治疗带来了巨大变化。因此,当下迫切需要临床实用的生物标记物,可识别可能从ICI治疗中获益的患者。
目前,PD-L1表达和肿瘤突变负荷(TMB)已获得FDA批准用于预测NSCLC对免疫治疗的反应。高TMB代表基因组不稳定性,并可能触发癌细胞突变产生的新抗原改善免疫原性。现在TMB评估主要通过全基因组测序(WGS)或全外显子测序(WES),费用昂贵,且结果也差强人意。
因此,研究人员开发了一种新的肿瘤突变评分(TMS),定义为候选基因突变的基因数目。在该研究中,研究人员在240例NSCLC患者中将TMS与TMB和PD-L1进行了比较,并额外在34例NSCLC患者中进行了验证。
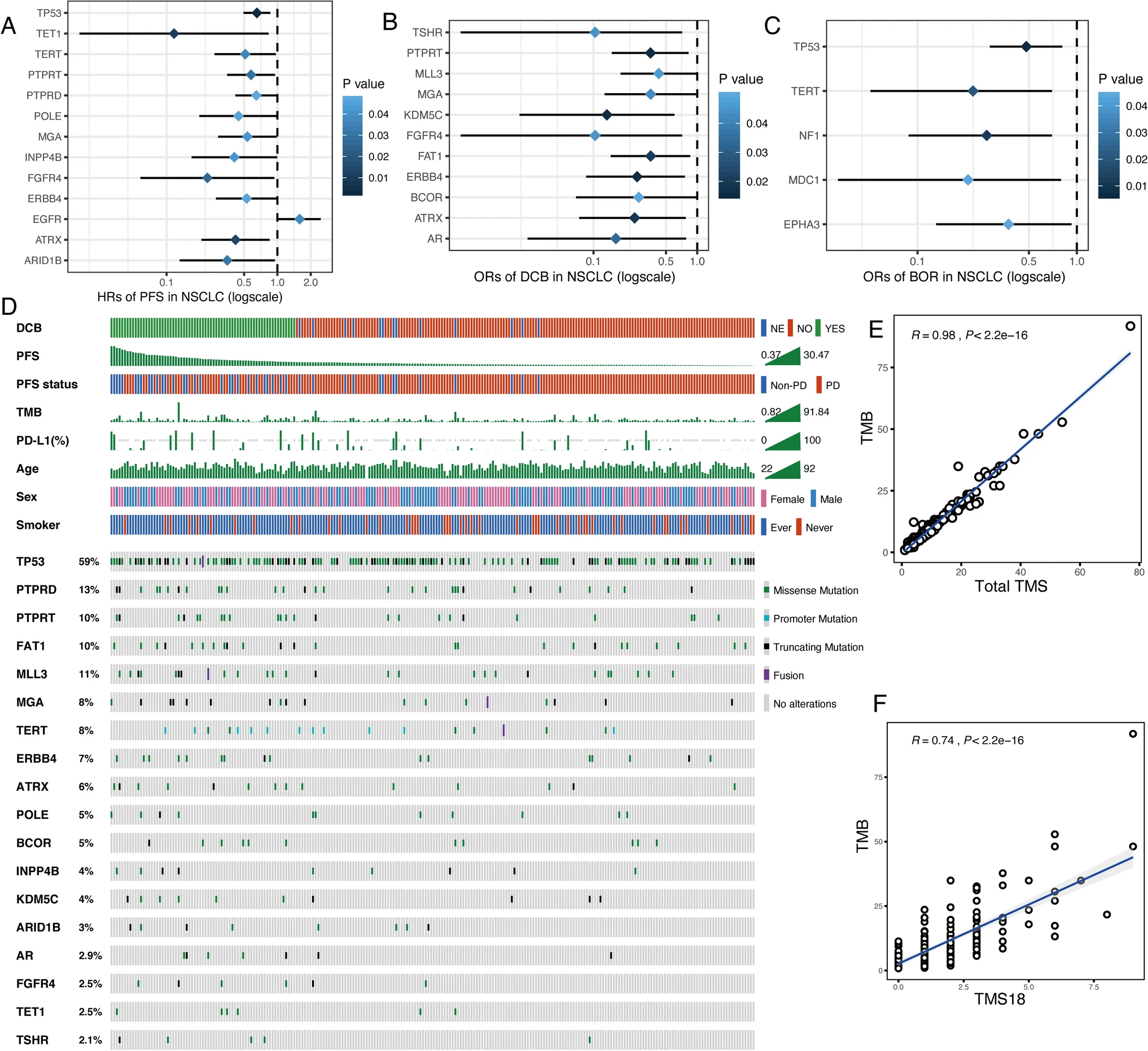
TMS18的18个基因和特征
有18个基因与更长的无进展生存期(PFS)或更好的反应显著相关。研究人员将这18个有利基因中的突变基因数定义为TMS18。
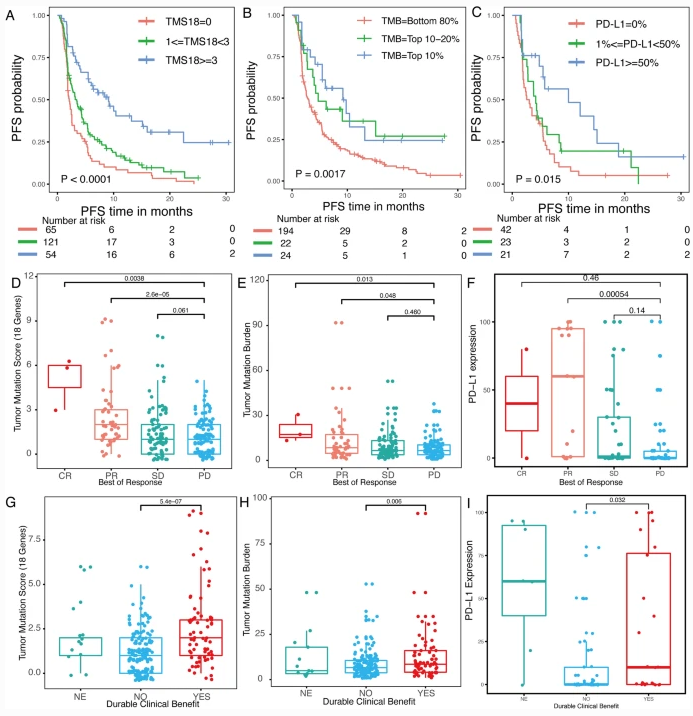
TMS18、TMB和PD-L1表达的预测表现
在生存分析中,TMS18(HR 0.307,P<0.001)的风险比和P值均小于TMB(HR 0.455,P=0.004)和PD-L1表达(HR 0.403,P=0.005)。此外,TMS18的AUC也明显高于TMB,与PD-L1相结合还可进一步提高准确度。TMS18的一般阈值可使更多的患者受益。这些发现在验证队列中基本一致。
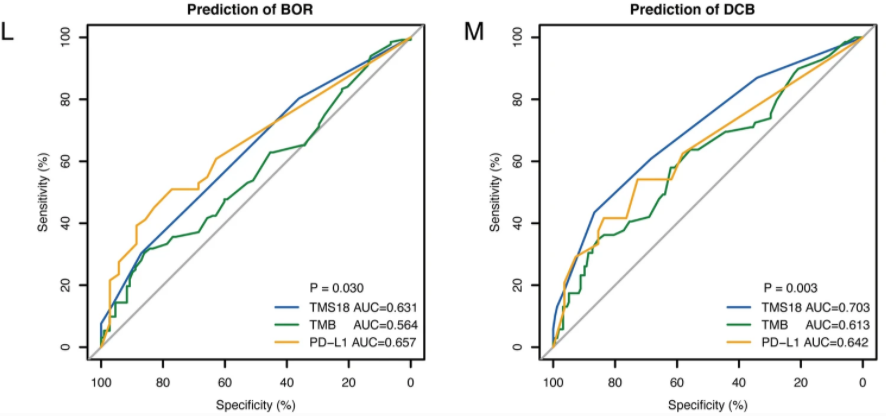
TMS18、TMB和PD-L1表达的预测敏感性
综上所述,在预测NSCLC患者对ICI治疗的反应方面,TMS18比TMB更有效。选择性TMS比非选择性TMB更可行、更经济。TMS18和PD-L1联合应用在预测NSCLC患者采用ICI治疗的疗效方面可能有更高的准确性。
原始出处:
Li, Y., Chen, Z., Tao, W. et al. Tumor mutation score is more powerful than tumor mutation burden in predicting response to immunotherapy in non-small cell lung cancer. Cancer Immunol Immunother (2021). https://doi.org/10.1007/s00262-021-02868-w
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#肿瘤突变#
72
#反应性#
0
#突变评分#
80
#TMS#
70
#SCLC患者#
61
#TMB#
82
#NSCLC患者#
63
#肿瘤突变负荷#
77
这些图好漂亮,怎么做出来的了?
122
涨知识
104