2017年2月Cell期刊不得不看的亮点研究
2017-02-28 生物谷 生物谷
2017年2月28日/生物谷BIOON/---2月份即将结束了,2月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。 1.Cell:重大突破!模拟禁食效果的饮食或可逆转糖尿病 doi:10.1016/j.cell.2017.01.040 在一项新的研究中,来自美国南加州大学、麻省理工学院科赫研究所和加州大学旧金山分校的研究人员证实一种
2月份即将结束了,2月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:重大突破!模拟禁食效果的饮食或可逆转糖尿病
doi:10.1016/j.cell.2017.01.040
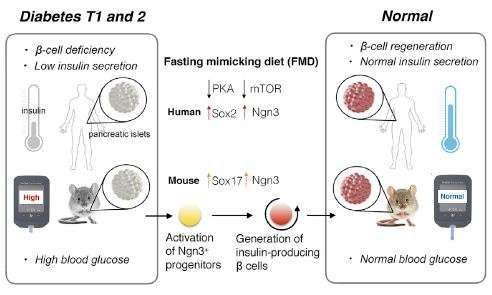
这项研究以小鼠和人类细胞为实验对象,证实这种模拟禁食效果的饮食促进新的产生胰岛素的胰腺β细胞生长,从而降低小鼠体内的1型和2型糖尿病症状。
在1型糖尿病和晚期2型糖尿病中,胰腺丧失产生胰岛素的β细胞,从而增加血糖水平的不稳定性。这项研究证实在每周四天接受FMD饮食的小鼠当中,它们的糖尿病受到显著逆转。它们再次获得健康的胰岛素产生、下降的胰岛素抵抗性,并且展现出更加稳定的血糖水平。即便是对晚期糖尿病小鼠而言,也是这种情形。
这种周期性饮食激活成年小鼠体内的正常情形下仅在小鼠胎儿的发育中的胰腺内有活性的基因。这些基因最终引发蛋白Ngn3表达,因此产生新的分泌胰岛素的β细胞。
Longo和他的团队也研究了体外培养的来自人供者的胰腺细胞,结果发现在来自1型糖尿病患者的胰腺细胞中,禁食也增加Ngn3蛋白表达和加快胰岛素产生。这些结果提示着FMD饮食可能缓解病人的糖尿病病情。
doi:10.1016/j.cell.2017.01.024
有性生殖与病毒感染事实上存在很多共同之处。根据一项新的研究,这两种过程依赖于单个蛋白HAP2,这种蛋白能够让两个细胞(如精细胞和卵细胞)无缝融合,或者让一个病毒与细胞膜融合。蛋白HAP2在病毒、单细胞原生动物、很多植物和节肢动物中广泛存在,这提示着这种蛋白是在地球上的生命历史极早期发生进化的。
论文共同通信作者William Snell教授他的同事们在一种被称作莱茵衣藻(Chlamydomonas reinhardtii)的单细胞绿藻中研究了蛋白HAP2。HAP2在单细胞原生动物、植物和节肢动物中是比较常见的,不过它并未在真菌或人类等脊椎动物中发现到。Snell和他的合作者们以及其他研究团队之前的研究结果表明在具有这种蛋白的有机体中,HAP2是它们的生殖细胞融合所必不可少的。但是它的精确机制仍然是不清楚的。
就当前的这项研究而言,Snell和他的团队利用复杂的计算机分析工具对衣藻蛋白HAP2和已知的病毒融合蛋白的氨基酸序列进行比较。这些结果提示着它们存在显著的相似性,特别是在一个被称作融合环的区域中。这个融合环区域能够让病毒融合蛋白成功地侵入细胞中。Snell推断,如果HAP2像一种病毒融合蛋白那样发挥功能,那么破坏它的融合环应当阻断它将生殖细胞融合在一起的能力。
果然,当Snell团队仅改变衣藻蛋白HAP2融合环上的单个氨基酸时,这种蛋白完全丧失了它的功能。生殖细胞能够附着在一起,但是它们不能够完成最后的一步:它们的细胞膜融合。类似地,当该团队加入一种结合到HAP2融合环上的抗体时,这些生殖细胞也不能够融合在一起。
Snell接触了法国巴斯德研究所结构生物学家、病毒学研究专家Felix Rey。巧合的是,Rey和他的同事们刚利用X射线衍射晶体分析技术解析出衣藻蛋白HAP2的结构。Rey的结果证实确实,HAP2在功能上与登革热病毒和寨卡病毒融合蛋白完全一样。
在很多种有机体(包括致病性的原生动物、入侵植物和破坏性的害虫)中,HAP2似乎是细胞融合所必需的。迄今为止,每个已知的HAP2蛋白版本在融合环区域共享一个关键性的氨基酸。正因此如此,HAP2可能是开发疫苗、疗法和其他控制方法的一种有前景的靶标。
3.Cell:DNA损伤期间,基因转录发生什么?
doi:10.1016/j.cell.2017.01.019
众所周知,当细胞中的DNA遭受损伤时,细胞作出的反应是激活特异性的基因,从而有助维护它的基因组完整性。然而,很少研究的是细胞实际上关闭它的绝大多数其他的基因。
在一项新的研究中,来自英国弗朗西斯-克里克研究所(Francis Crick Institute)的研究人员首次在分子水平上分析了这个现象。他们发现作为对DNA损伤作出的反应,所有基因的转录快速地和显著地放慢下来。他们也发现一个特殊的基因:由于这种放慢,它经转录产生一种更短的非编码RNA,而且是通过所谓的选择性剪接产生的。这种非编码RNA随后有助细胞在DNA损伤中存活下来。
这些研究人员描述的一个功能性的选择性剪接例子是基因ASCC3。基因ASCC3通常编码一种蛋白,但是当细胞中的DNA遭受损伤,基因转录放慢下来时,该基因经转录会产生一种更短的RNA分子。显著的是,这种RNA形式并不编码一种蛋白,因而是一种非编码RNA。他们发现事实上,这种选择性的非编码RNA是在这个发生DNA损伤的细胞中发现的一种稳定的转录本,并且在抵消这个基因编码的原始蛋白中发挥着作用。
4.Cell:挑战常规!细菌利用远程电信号招募其他的细菌物种
doi:10.1016/j.cell.2016.12.014

生物膜是一种由细菌和其他微生物群落在牙石等物体表面上形成的较薄结构,高度抵抗化学物和抗生素。对于它们是如何形成的,它们如何招募其他的微生物和抵抗攻击,人们知道的并不太多,然而了解它们的迁移行为具有实际的应用价值,比如阻止牙齿上的牙石形成从而避免在医院内感染上葡萄球菌。
研究人员在他们的研究中,通过将实验室实验与数学建模整合在一起,发现由枯草芽孢杆菌单个物种组成的生物膜能够通过电信号招募另一种不同的细菌物种:铜绿假单胞菌。
利用微流体生长腔室,研究人员记录了枯草芽孢杆菌生物膜产生的钾离子电信号将远离这种腔室的细铜绿假单胞菌吸引到这种发生电振动的生物膜的边缘。
位于生物膜外边缘的细菌离生长所必需的营养物最近,这可能导致位于生物膜内部的细菌挨饿。但是研究人员已发现生物膜振动产生一种他们称之为“代谢协同依赖性(metabolic codependence)”的解决方法:周期性地抑制外围的细菌生长,从而让内部的细菌获得营养物。
5.Cell:重磅!代谢蛋白迁移会激活胚胎自己的基因组
doi:10.1016/j.cell.2016.12.026
在一项新的研究中,来自美国加州大学洛杉矶分校伊莱和伊迪特-布罗德再生医学与干细胞研究中心的研究人员发现为了激活哺乳动物胚胎的基因组,它需要迁移一组代谢蛋白。这些代谢蛋白在正常情形下是在细胞的线粒体中发现的。在小鼠胚胎受精大约两天后,它们迁移到含有DNA的细胞核中。
在发育早期,哺乳动物胚胎(或者说合子)具有它需要生长和分裂所需的所有材料:卵细胞中含有的基因和蛋白。但是在发生一些细胞分裂后,这种合子需要激活它自己的基因组。科学家从没有完全理解这种转变是如何发生的。他们已知丙酮酸等某些代谢化合物是这种转变所需的,但是也已观察到在这个发育阶段,线粒体比较小,没有活性。在正常情形下,线粒体对丙酮酸进行加工,产生能量。
论文通信作者、加州大学洛杉矶分校布罗德研究所联席主任Utpal Banerjee教授和同事们通过在缺乏丙酮酸的培养皿中培养小鼠合子,证实丙酮酸是合子激活它们自己的基因组所必需的。此后,在小鼠胚胎和人胚胎中,他们利用多种方法确定了在一种被称作三羧酸循环(TCA cycle)的代谢过程中对丙酮酸进行加工的蛋白的位置。他们发现就在小鼠胚胎激活它自己的基因组之前,即两细胞阶段,这些三羧酸循环蛋白从线粒体迁移到细胞核。尽管在缺乏丙酮酸的培养皿中培养的小鼠细胞通常在两细胞阶段停止生长,但是他们能够通过加入三羧酸循环产生的一种代谢化合物来拯救这些细胞。在人胚胎中重复其中的一些实验,他们证实正当它的基因组被激活时(在六到八细胞阶段),这些代谢蛋白从线粒体迁移到细胞核。
6.Cell:深入认识诱导性多能干细胞产生过程
doi:10.1016/j.cell.2017.01.004
在一项新的研究中,来自美国加州大学洛杉矶分校伊莱和伊迪特-布罗德再生医学与干细胞研究中心的研究人员证实特定蛋白如何能够改变皮肤细胞的身份或者说细胞特征,和产生诱导性多能干细胞(iPS细胞)。ips细胞能够转化为体内任何一种细胞类型。这项研究可能影响治愈疾病的健康组织形成。
在这项新的研究中,研究人员将四种转录因子(Oct4, Sox2, Klf4和cMyc)加入到小鼠皮肤细胞中,绘制这些转录因子与这种细胞DNA的相互作用图谱。他们鉴定出改变细胞身份的DNA位点,从而获得关于这些DNA位点如何对这些细胞产生这种影响提供独特的认识。当他们分析这些数据时,他们取得两项关键的发现:这些转录因子同时地关闭小鼠皮肤细胞的身份和激活多能性;在这四种转录因子中,有三种转录因子需要合作定位和调节这些DNA位点。
进一步地,研究人员利用这些数据预测哪些额外的转录因子可能增强这种细胞重编程过程,随后加入第五种转录因子到这些小鼠皮肤细胞中。这种新的转录因子组合更加高效地抑制这些组织特异性细胞的身份,这会加快转变到多能性状态,100倍地增加这种细胞重编程过程的效率。
7.Cell:首次观察细胞内的蛋白复合体结构和功能
doi:10.1016/j.cell.2017.01.004

这种新的策略采用了超分辨率显微技术和计算建模方法。Gallego解释道,它允许研究人员在5纳米的精度下观察蛋白复合体,这一分辨率比“超分辨率显微技术所提供的分辨率高4倍,而且允许我们开展之前不可能开展的细胞生物学研究。”
研究人员对细胞进行基因修饰以便在内部构建出人工支持物。在这些支持物表面上,它们能够附着蛋白复合体。经过设计,这些支持物允许他们调整观察这些固定的纳米机器的角度。随后,为了确定蛋白复合体的三维结构,他们利用超分辨率技术测量不同组分之间的距离,然后在一种类似全球定位系统使用的过程中将它们进行整合。
Gallego采用这种方法研究胞吐作用,即细胞用来与细胞外面进行通信的一种机制。比如,神经元通过胞吐作用释放神经递质而彼此间进行通信。这项研究允许研究人员揭示出胞吐作用中一种关键的纳米机器的完整结构。他解释道,“如今,我们知道这种纳米机器是如何由8种蛋白形成的,每种蛋白在其中具有什么重要的作用。这一知识将有助我们更好地理解胞吐作用在癌症和肿瘤转移中的作用。”
8.Cell:重磅!科学家成功绘制出人类癌细胞的全局基因互作网络!
doi:10.1016/j.cell.2017.01.013
近日,刊登在国际著名杂志Cell上的一篇研究报告中,来自怀海德研究所和博德研究所的研究人员就取得了巨大突破,他们成功鉴别出了对14种人类急性髓性白血病癌细胞增殖和生存必须的一系列关键基因,此前研究人员并未利用基因组测序手段对这些癌细胞的特性进行研究;这项研究中研究人员将基因本质图谱同当前的遗传信息相结合进行研究阐明了多种癌症的特性。
文章中,研究者重点对和Ras癌基因相关联的基因和蛋白通路进行了研究,Ras基因是很多人类癌症中经常发生突变的癌基因,而且其在急性髓性白血病的发病过程中扮演着重要角色,研究者Tim Wang说道,从很大程度上来讲,突变的Ras蛋白自身往往被认为是无法用药物进行靶向作用的,但在本文研究中我们找到了另外一种方法,并且基于这种方法发现了Ras突变的癌症所依赖的一些基因,而且我们希望这些基因是利用药物可以进行控制的,但很不幸的是诸如这些Ras合成致死性基因往往很难进行鉴别。
利用基于CRISPR的基因编辑技术,研究人员测定了敲除掉人类基因组中18000个蛋白编码基因中每一个基因后的影响,这或许能够帮助研究者快速鉴别出仅在Ras突变细胞中需要的候选基因;同时研究者们还认为利用一般的方法也能够帮助寻找很多类型癌症的脆弱点。除了定义Ras特异性的基因网络外,本文研究数据还能够帮助研究人员解析此前未进行研究的基因的分子功能。
9.《细胞》里程碑研究:精准「吃」微生物治病不再遥远
doi:10.1016/j.cell.2017.01.022
过去,已经有一些研究“探听”到了少数细菌和免疫细胞以及基因间的“谈话”,知道细菌是如何“指挥”肠道基因的表达和免疫系统的免疫响应。而这一次,来自哈佛医学院的科学家首次想办法“听到了”肠道中多种肠道微生物与各个免疫细胞以及基因表达之间的“对话”,他们的研究成果发表在了《细胞》杂志上。
研究人员收集了53种肠道中常见的细菌,把它们分别定植入无菌小鼠的肠道中。在两周之后,研究人员鉴定了小鼠体内先天性和适应性免疫细胞的数量、各种免疫分子的含量以及基因的表达量,并且与没有进行定植的无菌小鼠做了对比。结果显示,每种免疫细胞都会受到细菌的影响,但是不同细菌的“影响力”也不完全相同。
对于同样的免疫细胞,一些细菌会提高它的活性,而另一些则会抑制,这也对应了我们前面说的“协同”与“拮抗”的作用。对此,研究的通讯作者Dennis Kasper研究员说:“肠道微生物在调控免疫细胞上的‘对抗效应’其实是提供了一种平衡机制,确保没有哪一种细菌对免疫系统的影响能够超越其他所有细菌,完全占据主导地位。”
类似的,一些细菌会上调某些基因的表达,另一些则会下调,表明肠道微生物对肠道基因的表达起到了表观遗传学层面的调控作用。在Kasper看来,上调基因的表达是为了给细菌自己创造一个“更舒适的”生存环境,而下调基因的表达则是为了给有害的细菌设置“糟糕的”生存环境。这样的“行为”无疑是一种保护机制,为什么这样说呢?因为有害细菌其实也很“聪明”。
10.Cell:科学家发现新型基因突变 为癌症诊断和治疗提供思路
doi:10.1016/j.cell.2016.12.025
借助下一代基因测序技术,科学家们已经知道癌症的根源在于破坏蛋白质序列的突变。突变会导致细胞合成异常活跃或发生功能紊乱的蛋白,也会导致细胞无法合成一些蛋白,最终导致癌症的发生。在最近发表在Cell上的这项研究中,研究人员介绍了一种可能导致癌症发生的新型突变:在基因组的非编码区域发生微小DNA序列(1到50个碱基)的插入或缺失,也叫做“indels”。
在这项研究中,研究人员对几个公共数据库中肿瘤样本的基因序列信息进行了分析,着重研究基因组中占98%的非蛋白编码区域。他们从肺腺癌这种最常见的肺癌开始,发现这些样本的基因组中最常见的indel突变区域位于编码表面活性蛋白的基因中。
研究人员还对12种其他类型癌症的基因组进行分析,发现在肝脏、胃和甲状腺肿瘤中存在类似的模式。
“在每一种癌症中,非编码的indel突变都会聚集在对器官功能非常重要的基因上,但是这些基因之前都未与癌症联系在一起。”Imielinski教授表示。这些非编码的indel突变非常常见,20%~50%的相关癌症中都存在这种突变。
“这种突变发生的频率与最著名的致癌突变一样高,任何基因或序列以这种频率发生突变都可能导致癌症发生。如果我们可以证明这一点,那将会是令人感到非常兴奋的结果。”
11.Cell:远古尼安德特人DNA对现代人健康的影响
doi:10.1016/j.cell.2017.01.038

此前的研究已经发现尼安德特人基因与现代人基因中在代谢、抑郁、狼疮发病率以及血液特征等等方面的关联,但其中的生物学机制已经不清楚。去年,来自蒙特利尔的研究者们发现尼安德特人的基因影响了现代人的免疫系统,这表明尼安德特人的基因对于非洲人种较强的免疫反应具有一定的意义。
如今,Akey等人发现了尼安德特人基因的具体位置,并且提供证据表明现代人与尼安德特人基因的表达方式存在区别。
他们通过分析GTEx数据库中的的RNA样本,找到了包含现代人与尼安德特人血统的人群,并且分析了他们父母亲的基因类型。并且分析了所有基因在不同组织中的表达情况。
结果显示,现代人与尼安德特人的同一等位基因表达特征存在差异。另外,他们发现大脑与睾丸中的基因表达差异最大。这说明这些区域的进化时间较早,进化速度也较快。
相关新闻阅读:
2017年1月Cell期刊不得不看的亮点研究
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#CEL#
60
#Cell#
58
文意真好,值得分享
88
牛逼了,这么样的技术
104
太高深了
79