JCO:替瑞利尤单抗联合阿替利珠单抗加化疗治疗未经治疗的广泛期小细胞肺癌
2024-02-09 daikun MedSci原创 发表于陕西省
该III期研究旨在评估替瑞利尤单抗+阿替利珠单抗+CE在初治ES-SCLC中的生存优势,替瑞利尤单抗联合阿替利珠单抗和CE并未改善ES-SCLC患者的预后,未能达到统计学差异。
目前,广泛期小细胞肺癌(ES-SCLC)的治疗选择有限,且大多数患者会出现疾病进展,中位生存期约为12个月。TIGIT是一种新兴的免疫抑制分子,在SCLC中高表达,可能成为新的治疗靶点。替瑞利尤单抗是一种抗TIGIT单抗,与抗PD-L1单抗阿替利珠单抗联合使用,可能增强抗肿瘤效果。前期II期研究显示,替瑞利尤单抗联合阿替利珠单抗在化疗初治的NSCLC中显示出有临床意义的抗肿瘤效果,并且耐受性良好。基于前期研究结果,该III期研究旨在评估替瑞利尤单抗+阿替利珠单抗+CE(卡铂(carboplatin)和依托泊苷(etoposide)的联合化疗方案)在初治ES-SCLC中的生存优势,以确定是否可以改善该疾病的治疗效果。

方法
符合入组标准的患者按照1:1的比例随机分配进入替瑞利尤单抗组或安慰剂组。患者接受4个周期的替瑞利尤单抗/安慰剂+阿替利珠单抗+CE方案,每个周期包括替瑞利尤单抗/安慰剂、阿替利珠单抗和CE。完成4个周期后,进入维持治疗,接受替瑞利尤单抗/安慰剂+阿替利珠单抗的方案,直至进展或出现不可耐受毒性。主要终点为无脑转移病史/存在患者的无进展生存期(PFS)和无脑转移病史/存在患者的总生存期(OS)。
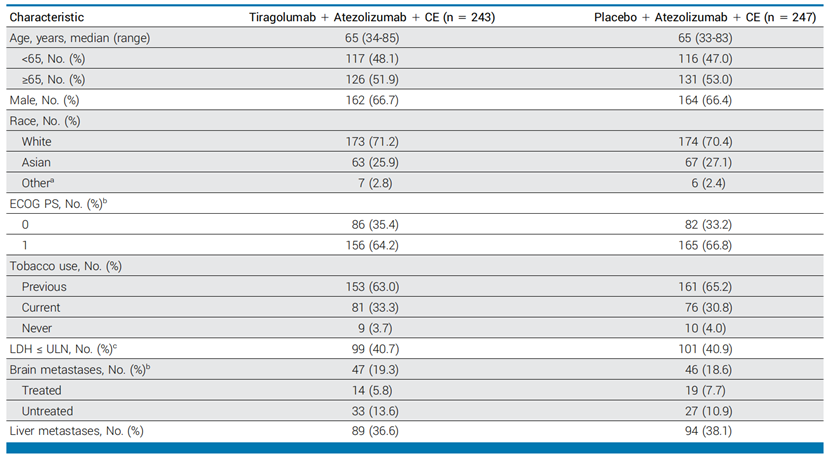
人群和基线特征
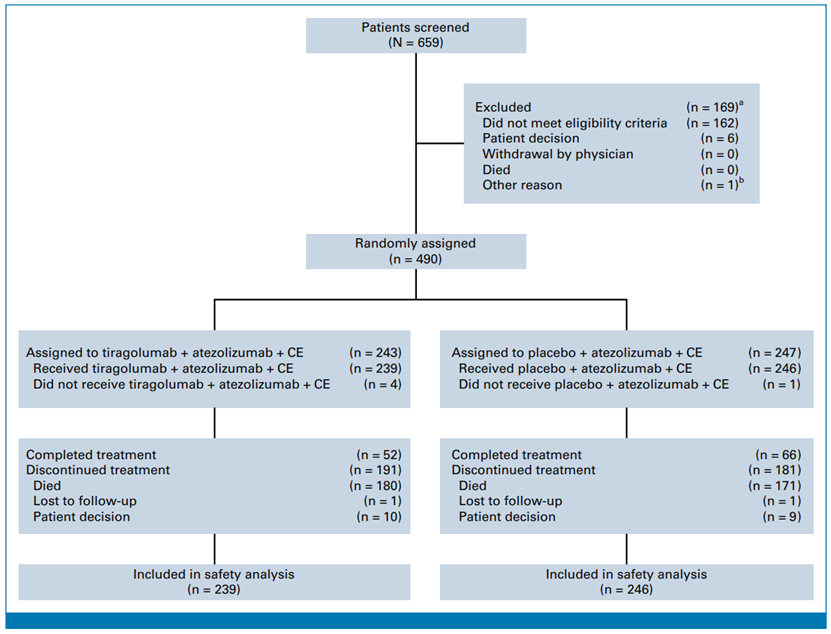
纳入患者年龄≥18岁,性别不限,组织学或细胞学证实的广泛期小细胞肺癌(ES-SCLC)。根据RECIST 1.1标准,有可测量病灶。ECOG PS评分0或1分。允许存在脑转移,但必须无症状且中枢神经系统外存在可测量病灶。共有659例患者接受筛选,最终有490例患者被随机分配到治疗组,其中243例进入替瑞利尤单抗组,247例进入对照组。最终分析中,替瑞利尤单抗组有196例患者,对照组有201例患者。在PFS分析中,替瑞利尤单抗组有196例患者,对照组有201例患者;在OS分析中,替瑞利尤单抗组有243例患者,对照组有247例患者。
研究结果
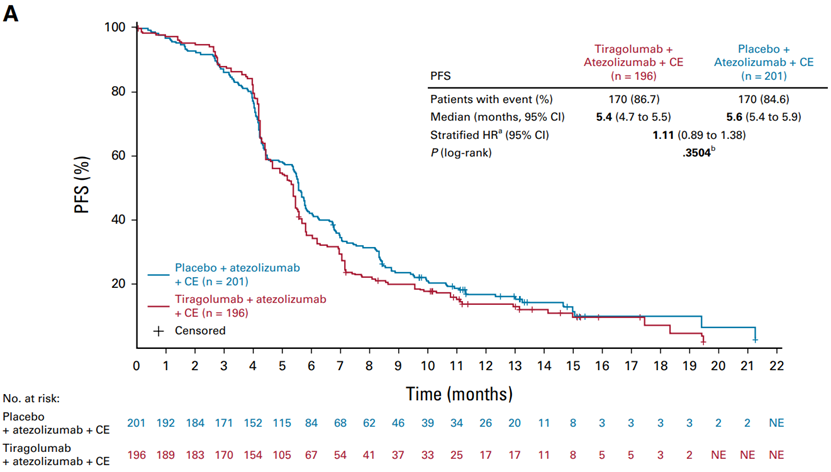
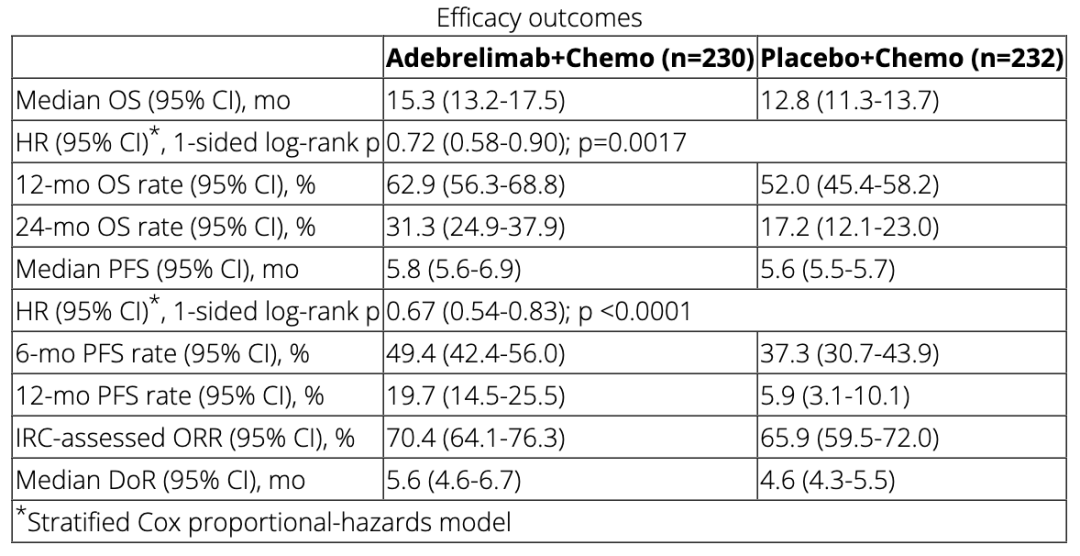
在主要分析集中(替瑞利尤单抗组196例,对照组201例),中位PFS分别为5.4个月和5.6个月,HR=1.11,95%CI 0.89-1.38,P=0.3504,未达到统计学差异。在主要分析集中,中位OS均为13.1个月,HR=1.14, 95%CI 0.90-1.44,P=0.2859,未达到统计学差异。在所有患者中,包括有脑转移的患者,PFS和OS结果与主要分析集一致,没有明显差异。对于PD-L1阳性的患者,两组OS结果也无明显差异。

安全性分析
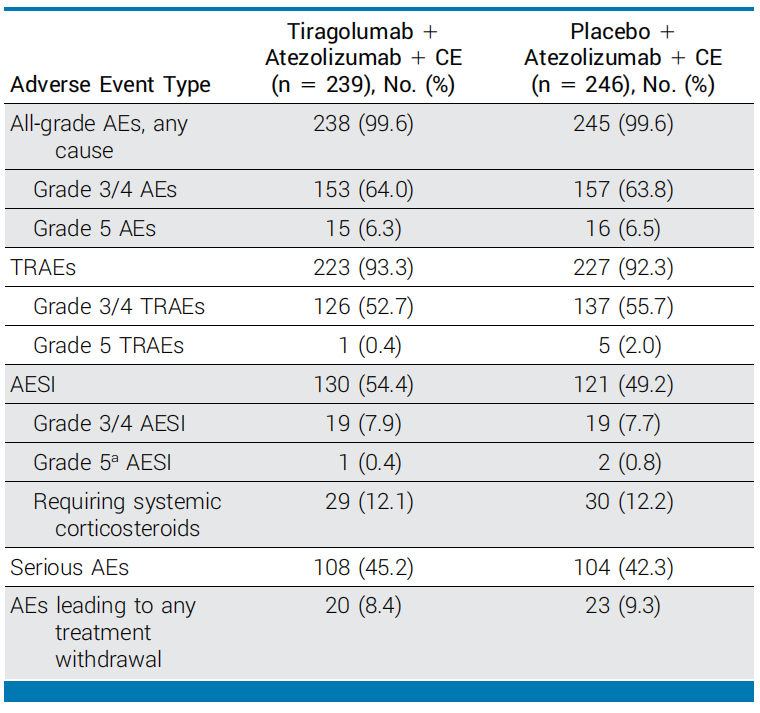
替瑞利尤单抗+阿替利珠单抗+CE和对照组的安全性和耐受性相当。两组患者均出现≥1种AE,替瑞利尤单抗组发生率为99.6%,对照组为99.6%。替瑞利尤单抗组出现3/4级AE的比例为64.0%,对照组为63.8%。两组出现5级AE的比例相似,替瑞利尤单抗组为6.3%,对照组为6.5%。
结论
替瑞利尤单抗联合阿替利珠单抗和CE并未改善ES-SCLC患者的预后,未能达到统计学差异,对照组结果进一步确认了阿替利珠单抗+CE作为ES-SCLC的标准一线治疗方案。在有脑转移的患者中,结果与主要分析集一致,没有明显差异。对于PD-L1阳性的患者,两组OS结果也无明显差异。后续研究需要进一步探索SCLC免疫微环境的分子机制,以确定TIGIT通路在SCLC中的具体作用机制。该研究代表了第一个在ES-SCLC患者中开展的大型III期临床试验,评估了TIGIT单抗联合免疫检查点抑制剂的治疗效果。
原始出处
Charles M. Rudin et al.,SKYSCRAPER-02: Tiragolumab in Combination With Atezolizumab Plus Chemotherapy in Untreated Extensive-Stage Small-Cell Lung Cancer. JCO 42, 324-335(2024).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#SCLC# #阿替利珠单抗# #替瑞利珠单抗#
77