肺静脉前庭隔离和碎裂电位消融治疗阵发性房颤的随机对照研究
2012-01-01 陈明龙 江苏省人民医院
目的:当前阵发性心房颤动的消融策略主要有两种,一种是针对触发机制的肺静脉前庭隔离术,另一种是心房基质改良的碎裂电位消融术;但是,仍然没有随机对照研究来评价阵发性房颤的首选策略是肺静脉前庭隔离抑或碎裂电位消融。 方法: 从2007年7月至2008年12月,共前瞻性的连续入选118例抗心律失常药物治疗无效的阵发性房颤患者(男性79例,年龄56.0±11.2岁),随机接受肺静脉前庭隔离术或者碎裂电位消
目的:当前阵发性心房颤动的消融策略主要有两种,一种是针对触发机制的肺静脉前庭隔离术,另一种是心房基质改良的碎裂电位消融术;但是,仍然没有随机对照研究来评价阵发性房颤的首选策略是肺静脉前庭隔离抑或碎裂电位消融。
方法: 从2007年7月至2008年12月,共前瞻性的连续入选118例抗心律失常药物治疗无效的阵发性房颤患者(男性79例,年龄56.0±11.2岁),随机接受肺静脉前庭隔离术或者碎裂电位消融。碎裂电位消融术后不再诱发房颤者,归入组1;术后仍能诱发者,联合肺静脉前庭隔离术。肺静脉前庭隔离术后不再诱发房颤患者,归入组2;术后仍能诱发房颤患者,联合碎裂电位消融治疗。所有进行联合消融的患者归入组3,依据联合消融术后是否诱发房颤分为两个亚组:不诱发组(S1)及诱发组(S2)。
结果:入选患者随机分为碎裂电位组(58例)及肺静脉前庭隔离组(60例)。两组间的临床基线资料包括性别、年龄、左房内径、左心室射血分数、器质性心脏病及阵发性房颤病程均无统计学差异。单独碎裂电位消融术后,24(41%)例患者不再诱发房颤,其中术中诱发2例二尖瓣峡部依赖型房性心动过速,1例左房前壁局灶房速,2例三尖瓣峡部依赖型心房扑动,所有房速均成功消融。其余34例联合肺静脉前庭隔离术,联合消融后,20例患者不再诱发房颤,其中3例合并三尖瓣峡部依赖型心房扑动。其余14例患者仍能诱发房颤,1例需要电转复。60例进入肺静脉隔离组者,1例术中出现心脏压塞退出研究,单纯肺静脉前庭隔离后35例(59%)患者不再诱发房颤。与单纯碎裂电位消融术式相比,单纯肺静脉前庭隔离术后房颤的不诱发率明显增高(59% vs. 41%, P=0.052)。其余24例单纯肺静脉隔离术后仍能诱发房颤者联合碎裂电位消融,联合消融后,16例不再诱发,但仍有8例诱发房颤。隔离组共9例患者因三尖瓣峡部依赖型心房扑动进行了后位峡部消融。1例合并左前间隔房速成功消融;1例合并左侧旁路并成功消融。平均随访22.6±6.4个月,碎裂电位组的总成功率明显低于肺静脉前庭隔离组(57% vs.73%, P=0.075)。进一步分组分析提示:组2的房颤复发比例最高(17.1%),其次是组1(12.5%),组3最低(8.6%),但三组间并无统计学差异。消融术后房速的发生率在组1中最高(50%),组3次之(22%),组2仅6%,存在统计学差异(P<0.001)。因此,组1的总成功率明显(38%)低于组2(77%)(P=0.002);组3中,两个亚组随访的房颤复发率、房速发生率及总成功率均无统计学差异。
结论:碎裂电位消融组的房颤诱发率和术后房速发生率均明显高于肺静脉前庭隔离组,导致术后成功率明显偏低。本研究提示阵发性房颤患者的首选消融策略为肺静脉前庭隔离术,而不是碎裂电位消融术。
关键词:阵发性心房颤动;导管射频消融;肺静脉前庭隔离;碎裂电位
Prospective randomized Comparative study of Pulmonary Vein Antrum Isolation versus Complex Fractionated Electrogram Ablation for Paroxysmal Atrial Fibrillation
Introduction: There are two mayor ablation strategies for paroxysmal atrial fibrillation (PAF), one is pulmonary vein antrum isolation, the other one is mapping and ablation of complex fractionated electrogram (CFE). However, no randomized study comparing the clinical efficacy of PV antrum isolation ablation versus CFEs ablation as a primary strategy in patients with paroxysmal AF has been performed.
Methods: We prospectively studied 118 patients (79 men, age 56.0±11.2 years) with symptomatic paroxysmal AF who underwent circumferential antrum PV isolation or CFE ablation. Patients were then randomly assigned to CFE ablation group and PV antrum isolation group (PVAI) after atrial fibrillation being induced. Patients with inducible AF followed the first step, will cross over the other ablation strategy. Patients who only had CFE ablation with subsequent AF noninducibility were classified into group one (G1), and those with single PVAI which rendered AF noninducible were classified into group two (G2). Cross-over patients who had both ablation strategies were assigned to group three (G3).
Results: All the study patients were randomly assigned to CFE group (58 patients) and PVAI group (60 patients). There was no difference in baseline characteristics including age, gender, left atrial diameter, ejection fraction, structural heart disease and history of AF between both groups. AF became non-inducible in 24 patients (41%) after CFE ablation (G1), which included 2 patients with mitral isthmus dependent flutter, 1 with anterior wall focal AT and 2 with cavo-tricuspid isthmus dependent flutter developed during defragmentation ablation. These ATs were later successfully eliminated by ablation in the same procedure. The remaining 34 patients were cross-over to PVAI and rendered AF non-inducible in 20 patients. Additional cavo-tricuspid isthmus ablation was done in three patients. 14 patients still had inducible AF and one patient need DC cardioversion because of AF persistency. PVAI was successful in 60 patients except one due to cardiac temponade. AF was non-inducible in 35 patients (59%) after PVAI (G2). The acute incidence of AF noninducibility after single PVAI was much higher than that after single CFE ablation (59% vs. 41%, P=0.052). The remaining 24 patients had additional CFE ablation and rendered AF non-inducible in 16 patients. Additional cavo-tricuspid isthmus ablation was done in 9 patients because of clinical atrial flutter documentation or occurrence during the procedure. A focal AT arising from left anterior septal developed during CFE ablation and was successfully ablated. Left accessory pathway was found in one patient and was abolished. After a mean follow up of 22.6±6.4 months, the total success rate of CFE group is much lower than that of PVAI group (57% vs. 73%, P=0.075). Further subgroup analysis revealed that the proportion of AF recurrence patients in G2 is the highest (17.1%), followed by G1 (12.5%), G3 is the lowest (8.6%), but the statistically difference has not been reached (P=0.469). Post ablation AT occurred very commonly in patients who received CFE ablation, with the rate of 50% (12/24) in G1, 22% (13/58) in G3, but only 6% (2/35) in G1 (P<0.001). This makes the total success rate of G1 (38%) dramatically lower than that of G2 (77%)( P=0.002) and G3 (69%) unexpectedly lower than G2 (P=0.395). As to those highly selected patients in G3 who had noninducible AF (S1) and those who still had inducible AF (S2) after ablation, the follow up result of AF free proportion, AT occurrence and total success rate shows no significant difference
Conclusions: Our findings suggest that PVAI, rather than CFE should be the initial ablation approach in patients with paroxysmal AF due to higher ocurrence rate of AT after CFE ablation.
Key Words: paroxysmal atrial fibrillation; catheter ablation; pulmonary vein isolation; complex fractionated electrogram
自1998年Haissaguerre等1开创性的发现房颤起源于肺静脉后,提出了针对致心律失常腔静脉的消融策略;之后,随着房颤机制得的进一步理阐明,消融术式也有了一定的更新,从最初的点消融到节段性肺静脉隔离2,发展至基于肺静脉解剖学消融的治疗策略3;随后,进展为这种术式基础上的隔离所有肺静脉及左房后壁的基质改良4。然而,2004年Nademanee等5, 6另辟蹊径,提出针对房颤维持基质-碎裂电位的导管射频消融术式,研究者认为,碎裂电位区域代表了房颤的维持基质,也是房颤消融的靶点,单纯针对基质消融的术式能够取得良好的效果,但最初的碎裂电位区域只是基于术者的判断,而没有规范化。此后,三维标测系统的自动识别碎裂电位功能被应用到临床,克服了主观观察的缺陷7-12。此外,多项研究提示,碎裂电位具有时空稳定性;这确保碎裂电位标测的准确性及消融的完整性。但是,尚无随机对照研究来评价阵发性房颤的首选消融策略是肺静脉前庭隔离抑或是碎裂电位消融。
方 法
2.1 临床资料
从2007年7月至2008年12月,共前瞻性的连续入选118例抗心律失常药物治疗无效的阵发性房颤患者(男性79例,年龄56.0±11.2岁)。 入选标准:1)年龄在18~75岁之间;2)6个月内房颤至少发作过2次,两次发作间隔大于7天; 3)至少一种I类或III类抗心律失常药物治疗无效的症状性房颤患者;4)自愿并且承诺参加并完成定期随访。 排除标准:1)1年内接受过冠状动脉旁路移植术;2)超声心电图检查提示左心室射血分数<35%;3)显著的瓣膜疾病和/或人工瓣膜置换术后;4)3个月内发生的心肌梗死或者中风; 5)扩张型心肌病失代偿期;6)对对比造影剂过敏;7)1个月内出现过严重的电解质异常;8)有应用华法林或者肝素禁忌症的阵发性房颤患者;9)1年内出现过肺水肿;10)常规经食管超声心动图检测出左心耳及左房附壁血栓。 入选本研究的阵发性房颤患者,左心室射血分数和左心房内径分别为65.0±3.9% 和 35.0±4.4mm。阵发性房颤患者的平均病史为53.1±46.3个月。所有患者术前均签署知情同意书。所采用的临床方案经本院伦理委员会讨论,获得通过后实施。
2.2 一般处理及术前准备
详细询问病史,体格检查后,行十二导心电图检查,术前常规检查动态心电图。所有患者术前均应用华法林抗凝,调整药物剂量达到国际标准化比值2.0~3.0后继续抗凝3周,术前3天停用华法林改用低分子肝素5000IU,皮下注射,一天两次,手术当天停用一次,术前6小时禁食。
2.3 电生理检查
术前停用抗心律失常药物至少5个半衰期,服用胺碘酮者至少停用2个月。术前行经食管超声心动图检查排除左心耳及左心房血栓。局部麻醉后,常规穿刺左锁骨下静脉及左、右股静脉,分别置入10极及4极标测导管至冠状静脉窦和右室心尖部。穿刺房间隔,置入2支SWARTS-SL1长鞘至左心房。穿刺房间隔成功后,常规给予肝素抗凝,并维持部分活化凝血酶原时间(ACT)在250- 300s之间。经多用途导管分别于左前斜45°和右前斜30°造影显示各肺静脉。一根长鞘置入环状标测电极,另一根长鞘置入冷盐水消融导管进入左房进行标测和消融。
2.4 研究设计
入选本研究后,如果患者在术前为窦性心律,从冠状窦近端通过高频burst刺激诱发房颤。诱发参数为5次最短的心房1:1夺获并持续起搏30秒。刺激强度为10mA 脉宽2 ms(Medtronic 5328)。如果房颤持续时间超过1分钟,则认为房颤被诱发。假如基础状态下,房颤不能诱发或不持续,静点异丙肾上腺素直至心率超过基线的30%,并在相同条件下重复刺激。诱发房颤后,所有患者随机进入碎裂电位消融组和肺静脉前庭隔离组。
碎裂电位消融组,消融前房颤必须持续并完成左房及冠状静脉窦的碎裂电位标测。穿刺房间隔成功后,先分别行右侧和左侧肺静脉造影并完成左房模型构建成功,应用EnSite-NavX自带的碎裂电位标测软件进行标测,标测及消融导管的滤波设置为30-500Hz,标测的结果以颜色的形式投影在左心房、肺静脉及冠状静脉窦上。平均碎裂电位标测的参数设置如下:不应期40ms,心房电压敏感度0.1mV,间期10ms,每点采集时间为6秒。碎裂电位标测的上限为120ms,低限为50ms。冷盐水灌注导管消融碎裂电位区域,消融参数设置:冷盐水流速为17-30ml/min,能量35W,温度
肺静脉前庭隔离组者在窦律或者房颤节律下进行消融,方法如前所述4,但采用单Lasso技术,简而言之,穿刺房间隔成功后,分别行右侧和左侧肺静脉造影,左房模型构建成功后,于肺静脉开口外0.5~1
两组患者,消融过程中如房颤转为房性心动过速,依据三维标测结合拖带标测技术确定其机制,并采用相应的消融策略。如为局灶,行局部消融;如为大折返性,确定相应缓慢传导区或关键峡部并行消融。
本研究的设计及消融流程如图1所示。只进行碎裂电位消融后不再诱发房颤的患者进入组1, 只进行肺静脉前庭隔离且术后不再诱发房颤的患者进入组2。 既进行碎裂电位消融又同时进行肺静脉前庭隔离的患者归入组3。如果联合消融术后仍能诱发房颤,静脉推注普罗帕酮转复为窦律,如不能转复,则进行体外直流电复律。 三组患者的临床资料见表1。
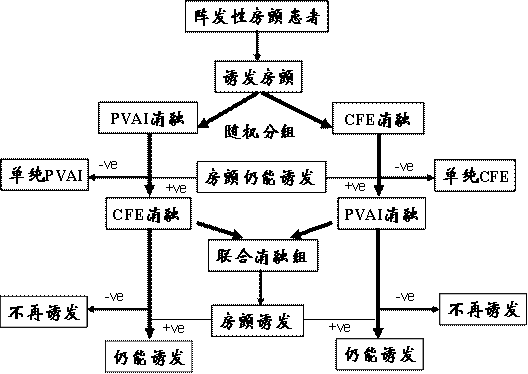
图1:研究设计流程图。 PVAI:肺静脉前庭隔离;CFE:碎裂电位
表1 三组患者临床资料
|
组1(N=24) |
组2(N=35) |
组3(N=58) |
P value | |
|
年龄(岁) |
52.2±13.2 |
57.6±9.1 |
56.4±11.2 |
0.166 |
|
性别(男性) |
17(70.8%) |
23(65.7%) |
39(67.2%) |
0.917 |
|
病史(月) |
52.9±42.2 |
53.5±43.5 |
51.8±46.5 |
0.983 |
|
左房内径(mm) |
34.7±4.2 |
35.5±4.4 |
34.2±3.6 |
0.278 |
|
射血分数(%) |
66.2±4.1 |
65.9±4.7 |
64.5±3.3 |
0.127 |
|
高血压(例) |
5(20.8%) |
10(28.5%) |
12(20.6%) |
0.654 |
|
冠心病(例) |
1 |
3 |
2 |
0.539 |
|
肥心(例) |
0 |
0 |
1 |
- |
|
甲亢(例) |
1 |
1 |
2 |
0. 964 |
冠心病:冠状动脉粥样硬化性心脏病;肥心:肥厚型心肌病;甲亢:甲状腺机能亢进
2.5 消融术后药物治疗及随访
所有患者术后均给予先前无效的抗心律失常药物3个月。术后所有患者均继续使用低分子肝素抗凝5天,第2天加用华法林,持续应用3个月,并定期复查国际标准化比值(INR),维持在2.0~3.0之间。出院前所有患者均做常规体表心电图和动态心电图检查,术后1个月、2个月、3个月、6个月分别再行上述检查。有症状者随时门诊就诊复查心电图。术后3个月复查超声心动图,观察左右心房之间有无分流。
2.6 统计学分析
所有数据均用SPSS 15.0统计软件处理。连续变量用均数±标准差表示, 连续变量的组间比较应用Mann-Whitney t检验,分类变量应用卡方检验,术后随访无房颤复发事件应用Log-rank生存曲线统计,P<0.05表示有统计学差异。
结 果
3.1 三组患者临床特征及分组情况
所有患者随机分为碎裂电位组(58例)及肺静脉前庭隔离组(60例)。两组间的临床基线资料包括性别、年龄、左房内径、左心室射血分数、器质性心脏病及阵发性房颤病程均无统计学差异。
3.2 碎裂电位消融
基础状态下,碎裂电位组患者,14例自发房颤,其余44例患者,通过冠状静脉窦高频burst刺激均能诱发房颤(不应用或应用异丙肾上腺素)。构建左房及肺静脉冠状窦模型后,应用环状电极高密度标测左心房,平均采点108±21个。依据标测结果,碎裂电位的常见分布部位为:左上肺静脉的前庭部位,左房后壁,冠状窦内,右上肺静脉的前庭区域,右下肺静脉的前庭区域,左心房前壁,二尖瓣环后壁,左房顶部及左房侧壁(图2)。完成碎裂电位标测后,三维导航下标测区域行碎裂电位消融。
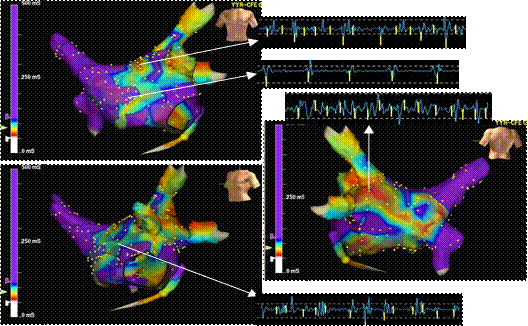
图
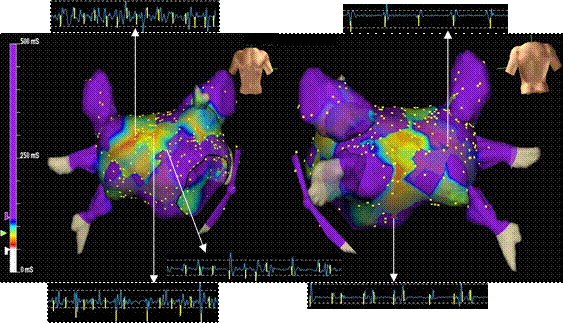
图-2B
图2:EnSite-NavX三维标测系统指导下的碎裂电位标测图。图



图

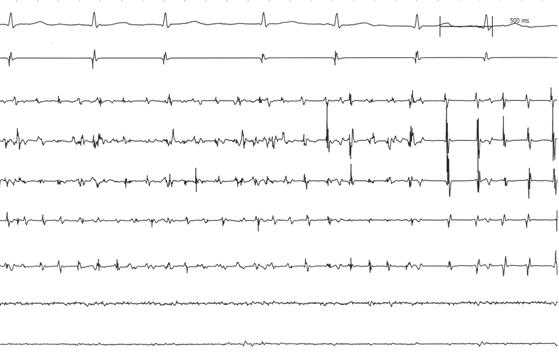

图3B

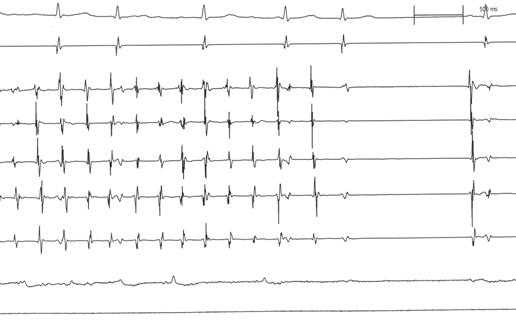

图
图3:碎裂电位消融终止房颤示意图。图
碎裂电位消融术后,24例(41%)患者不再诱发房颤(组1),其中2例患者合并二尖瓣环依赖型房性心动过速,1例合并左房前壁局灶房速,3例合并三尖瓣峡部依赖型心房扑动(图-4)。采用激动标测结合拖带技术消融并终止所有房速。

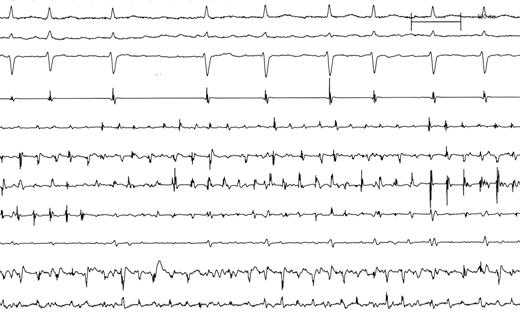

图


 图4B
图4B

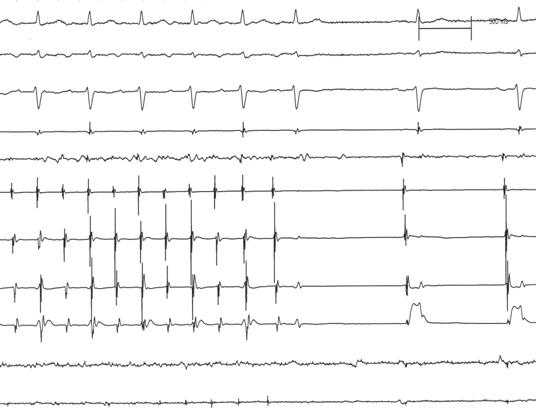
 图
图
图4:碎裂电位消融终止房颤示意图。图4A碎裂电位消融前消融导管位于碎裂电位区域;图4B碎裂电位消融过程中,心房周长转变为三尖瓣峡部依赖型心房扑动,图4C 三尖瓣后位峡部消融终止心动过速。从上至下通道表示体表心电图为I,aVF,V1,腔内电图表示为右室心尖部,冠状窦及消融导管。 碎裂电位消融术后仍能诱发房颤的34例患者,继续进行肺静脉前庭隔离的消融策略,具体方法如前描述,但采用单Lasso技术;联合消融后,20例患者不再诱发房颤(图-4)。此外,3例患者因术后诱发出三尖瓣峡部依赖型心房扑动,而进行三尖瓣后位峡部消融并达到双向阻滞。联合消融后仍能诱发房颤的14 例患者,其中1例因为房颤持续不能自行终止而给予直流电体外电复律。 3.3 肺静脉前庭隔离术 基础状态下,碎裂电位组患者,15例自发发作房颤,其余45例患者,通过冠状静脉窦高频burst刺激均能诱发房颤(不应用或应用异丙肾上腺素)。所有患者均达到隔离所有肺静脉的终点,除了一例术中出现心脏压塞而提前终止手术。隔离术后,35例患者(59%)不再诱发房颤归入组2。组2消融术后不再诱发房颤的比例明显高于组1(59% vs. 41%, P=0.052)。其余24例患者在肺静脉前庭隔离术后仍能诱发房颤,并同时进行碎裂电位消融,消融部位为初始标测的碎裂电位区域。联合消融术后16例患者房颤不再诱发(图-6)。其余6例患者仍能诱发房颤,但均能自行终止或者应用普罗帕酮后终止。其中9例患者术前合并三尖瓣峡部依赖型心房扑动或者术中发生,而同时行三尖瓣后位峡部消融并达到双向阻滞,1例患者诱发出左房前间隔的局灶房速并成功消融,1例患者电生理检查发现合并左侧旁道也成功消融。肺静脉隔离术后进行心房碎裂电位标测,提示碎裂电位面积明显减少(图-5)。
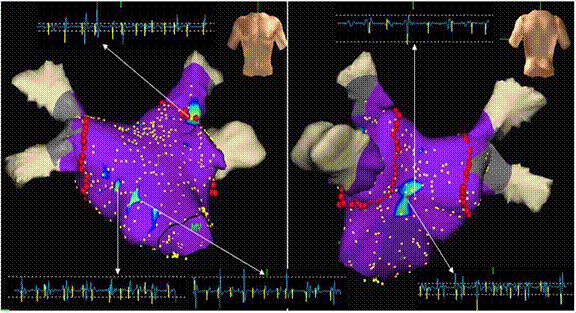
图5:肺静脉前庭隔离术后,行心房碎裂电位标测,显示,碎裂电位的分布区域明显缩小,仅分布于房间隔,左房后壁及右上肺静脉与左心耳交界的前庭部,灰色表示低电压区。
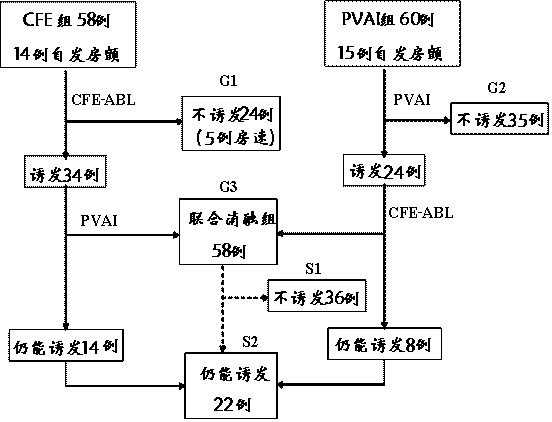
图6:随机分组进入碎裂电位组及肺静脉前庭隔离组的消融线性流程图。肺静脉隔离组中1例因术中发生心脏压塞而未达到消融终点。CFE:碎裂电位;PVAI:肺静脉前庭隔离术;ABL:导管射频消融
3.4 术后随访
术后平均随访22.6±6.4个月,碎裂电位组的总成功率明显低于肺静脉隔离组(57% vs. 73%, P=0.075)(图7)。进一步分组分析提示(图8):组2的房颤复发比例为17.1%,其次是组1(12.5%),组3的比例最低(8.6%),但三组间并无统计学差异(P=0.469)。消融术后房速的发生率在组1中最高达50% (12/24),组3为 22%13/58),组2仅6%(2/35),存在统计学差异(P<0.001)。因此,组1的总成功率明显(38%)低于组2(77%)(P=0.002);此外,令人惊讶的是,联合消融组3(69%)的总成功率也低于组2(P=0.395)。在组3的亚组中,依据联合消融后是否能诱发房颤分为两个亚组:不诱发组(S1)及诱发组(S2);但两个亚组随访的房颤复发率,房速发生率及总成功率均无统计学差异(图9)。Log-rank生存曲线统计显示组2无房性心律失常的事件最高,组1最低,具有统计学差异(图10),空白期内、空白期后房性心律失常复发和平均复发时间情况见表2。
![]()
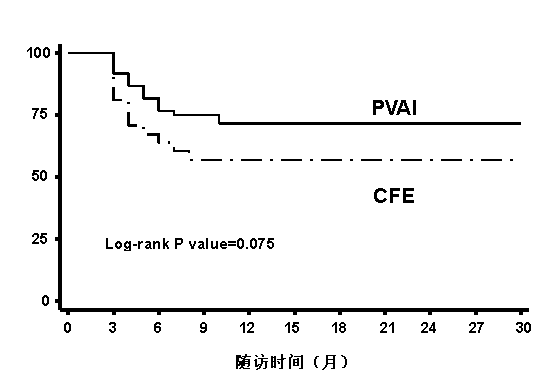

图7:随机分组的意向性治疗生存曲线图,两组之间无统计学差异
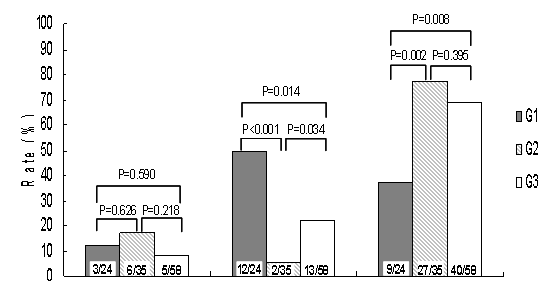 房颤复发 房速发生 总成功率
房颤复发 房速发生 总成功率
图8 三组间的随访房颤复发率,房速发生率及总成功率比较示意图

房颤复发 房速发生 总成功率
图9:组3的亚组(不诱发组及诱发组)两组间的随访房颤复发率,房速发生率及总成功率比较,均无统计学差异
|
|


图10:空白期(3个月)后,未应用抗心律失常药物基础上的无房性心律失常发生的生存曲线三组间的比较具有统计学差异,从上至下为组2,组3及组1。
表2:空白期内、空白期后房性心律失常复发和平均复发时间情况
|
G1 |
G2 |
G3 |
P 值 | |
|
复发房性心律失常例数<3个月 |
7 |
2 |
6 |
0.022 |
|
复发房性心律失常例数(停用抗心律失常药物后)>3个月 |
9 |
27 |
40 |
0.005 |
|
首次复发时间(空白期后) |
5.0±1.4 |
5.0±0.9 |
6.6±2.1 |
0.088 |
3.4 并发症
1例患者术中发生心脏压塞没有达到消融终点,另1例患者发生延迟性心脏压塞,均经心包引流后好转。其他的主要并发症有2例患者出现血胸,引流后好转,2例患者出现右侧股动脉假性动脉瘤,经压迫后治愈。1例患者消融术后1年检查出胃癌。
讨 论
主要发现
本研究有下列几项主要发现:(1)碎裂电位消融术后无诱发的患者随访成功率明显低于肺静脉前庭隔离组术后无诱发者及联合消融组;(2)联合消融组的随访成功率较组2低,但并没有达到统计学差异;(3)碎裂电位消融术后房速的发生非常常见。
阵发性房颤患者肺静脉前庭隔离的有效性
肺静脉前庭隔离治疗阵发性房颤的作用已经众所周知13。通过肺静脉口外的肺静脉左房交界处进行肺静脉隔离,能够有效的治疗阵发性房颤患者。本研究发现,单纯肺静脉前庭隔离术后房颤不再诱发者占59%,这种不再诱发的比例略高于Haissaguerre等14及Oral15等的研究,前者节段性肺静脉隔离术后房颤不再诱发的比例为57%,后者环肺静脉口外线性消融(不验证肺静脉隔离)术后40%患者房颤不再诱发。这组患者的长期随访结果提示房颤复发率为19%,总成功率为77%。肺静脉前庭隔离术的优势有:(1)祛除了肺静脉的触发或者维持因素;(2)破坏了左房后壁的致心律失常基质;(3)肺静脉前庭消融伴随的隐匿性或显现“去迷走”作用16, 17
阵发性房颤患者碎裂电位消融的有效, 性
Konings等18研究发现复杂的心房电位,并将其解释为多重波的碰撞(短的双电位)和传导阻滞(长的双电位)以及旋转字或者缓慢传导部位(碎裂电位)。在此研究基础上,Nademanee及其同事5等认为这一区域是房颤的主要维持部位,并独到的提出针对心房基质的消融策略-碎裂电位消融,来治疗房颤。在他们的开创性研究中,碎裂电位的定义被认为是房颤持续的主要因素,碎裂电位的主要分布区域为房间隔、肺静脉、左心房顶部、左房后间隔部位二尖瓣部位以及冠状窦口,导管射频消融所有碎裂电位区域(人为判断),房颤转复为窦律并不再被诱发。随访1年后110例(91%)的患者无房性心律失常复发(18例患者接受二次消融)。最近,三维标测系统使用的碎裂电位标测软件证明碎裂电位具有时空稳定性,并克服了术者自我观察所带来的缺陷7-12;此外,上述研究结果均提示三维标测的碎裂电位分布区域与Nademanee5的研究结果相一致,这使得碎裂电位消融能够在三维标测系统指导下进行,并且更加客观和便于重复。当前,这种术式作为单独的术式或者作为肺静脉隔离的补充术式应用于阵发性房颤或者持续性房颤患者中10-12, 19,但研究结果迥异。碎裂电位消融治疗房颤,且不再诱发房颤的可能机制如下:首先,部分碎裂电位区域代表着高频激动并触发房颤,或者作为旋转子及缓慢传导区域使房颤得以维持,而导管射频消融这些区域能够使得此部位的碎裂电位变得规整或者房颤终止;此外,碎裂电位的常见分布位置为肺静脉口部及肺静脉前庭,这些部位是触发并维持房颤的关键区域20,消融这些区域能够破坏房颤的基质及祛除房颤的触发因素;第三个可能的机制是碎裂电位的产生可能是自主神经改变的作用,部分研究提示自主神经节分布区域常与碎裂电位分布区域相一致,在这种情况下,导管射频消融碎裂电位区域同时可以损伤心脏神经丛16, 17,亦可使得房颤不再诱发。
然而,临床上碎裂电位消融术式常常作为肺静脉隔离术式的补充,一些研究发现,碎裂电位消融的效果要明显低于预期值,Verma等12的研究提示, 阵发性房颤患者,单纯的肺静脉隔离的效果要明显高于碎裂电位消融。Deisenhofer等10的研究显示肺静脉隔离联合心房碎裂电位消融并不能提高房颤的成功率。Khaykin等研究发现,60例房颤患者,随机分为肺静脉隔离
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#静脉#
53
#随机对照研究#
53
#对照#
64
#消融#
73
#阵发性房颤#
0
#消融治疗#
59