CCR:迪纳西库在临床前药物评估中显示可抑制骨肉瘤的转移
2024-01-26 儿童肿瘤前沿 儿童肿瘤前沿 发表于陕西省
这些细胞系建立对今后临床前评估药物有很大的帮助,比如迪纳西库(Dinaciclib)用于其中一株就展示了有效的转移抑制作用。
骨肉瘤(Osteosarcoma)是一种骨癌,通常在形成骨骼的成骨细胞中发生。它最常发生在儿童、青少年和年轻人身上。骨肉瘤的5年相对生存率为60%。如果癌症在局部阶段被诊断出来,5年相对生存率为77%。不幸的是,骨肉瘤是一种快速转移的肿瘤。在过去的几十年里,骨肉瘤治疗方面的突破很有限, 其部分原因可能是缺乏能够准确表述骨肉瘤转移的模型。
骨肉瘤基因组的特征是多拷贝数改变、染色体碎裂、和非整倍性突变,使其致癌性有着高特异性。过去仅有几株细胞系能表现出稳定的转移型态,因此建立新模型,全面评估转移递级机理在临床药物实验上尤为重要。
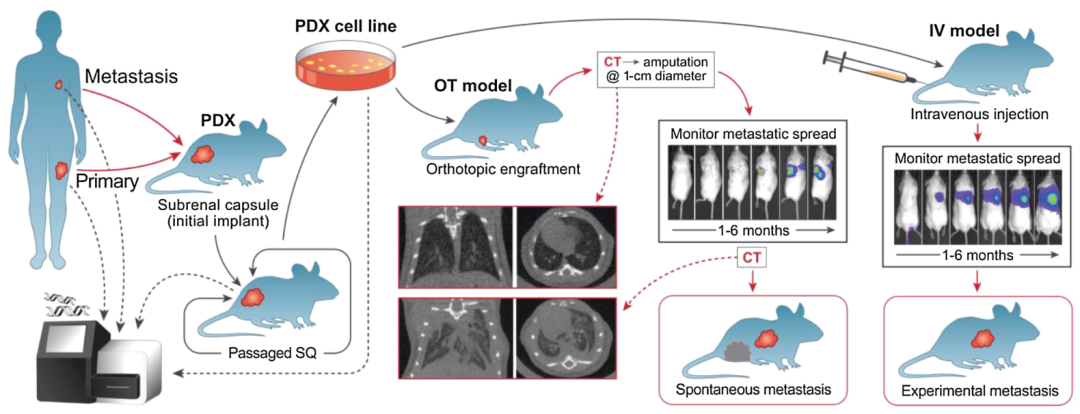
图1. 建模流程图
近日,由加利福尼亚大学旧金山分校儿科 E. Alejandro Sweet-Cordero 团队发表于 Clinical Cancer Research 题为 Osteosarcoma PDX-Derived Cell Line Models for Preclinical Drug Evaluation Demonstrate Metastasis Inhibition by Dinaciclib through a Genome-Targeted Approach 的文章,使用全基因组测序和 RNA 测序对匹配的患者样本、患者来源的异种移植(PDX)和 PDX 来源的细胞系进行了全面评估。Sweet-Cordero团队对八株PDX 衍生细胞系在小鼠体内的表征进行了评估,其中三株在体内表现高扩散,三株中等程度扩散和两株无扩散。这些细胞系建立对今后临床前评估药物有很大的帮助,比如迪纳西库(Dinaciclib)用于其中一株就展示了有效的转移抑制作用。

首先,患者来源的异种移植所衍生细胞系和其患者有着高度的同源性。通过对肿瘤样品和细胞系进行全基因和RNA测序,用无监督层次类聚方法(unsupervised hierarchical clustering),显示患者肿瘤与其对应的衍生细胞系有着高度的相似性,而市场上有的几株细胞系经过去几十年的实验室繁养,已慢慢远离患者肿瘤的基因组,而骨肉瘤又是一种基因繁杂、高拷贝数的肿瘤,因此运用患者来源的异种移植所衍生的细胞系来评估肿瘤抑制剂,才能真实体现肿瘤的转移机制。
另外,患者来源的异种移植所衍生细胞系在转移能力上大为不同,在静脉注射和原位植入模型中,对小鼠肺的肿瘤进行病理分析,不同程度的微转移和远程转移都观察到了;当通过静脉注射这些细胞系在小鼠体内形成最多的是肺转移和骨转移,在肝上也观察到了转移;在小鼠原位肿瘤模型中,通过胫骨旁植入,除了一株细胞系外,其它都能形成原位肿瘤;在小鼠截肢模型中,在七株细胞系里有五株细胞观察到了自发性、定向性转移。
再者,该团队还在小鼠静脉注射和原位植入模型中对市场上已有的细胞系进行了比较。在静脉注射和原位植入模型中,市场上已有的细胞系没有一株能形成骨转移,而骨转移在患者身上却是标志性的特征。
最后,该团队用患者OS152衍生的细胞株在小鼠原位植入模型中测试了迪纳西库,一种细胞周期蛋白依赖性激酶抑制剂。通过腹腔注射迪纳西库,在治疗周期结束时,肿瘤转移负担有了显著的减少。
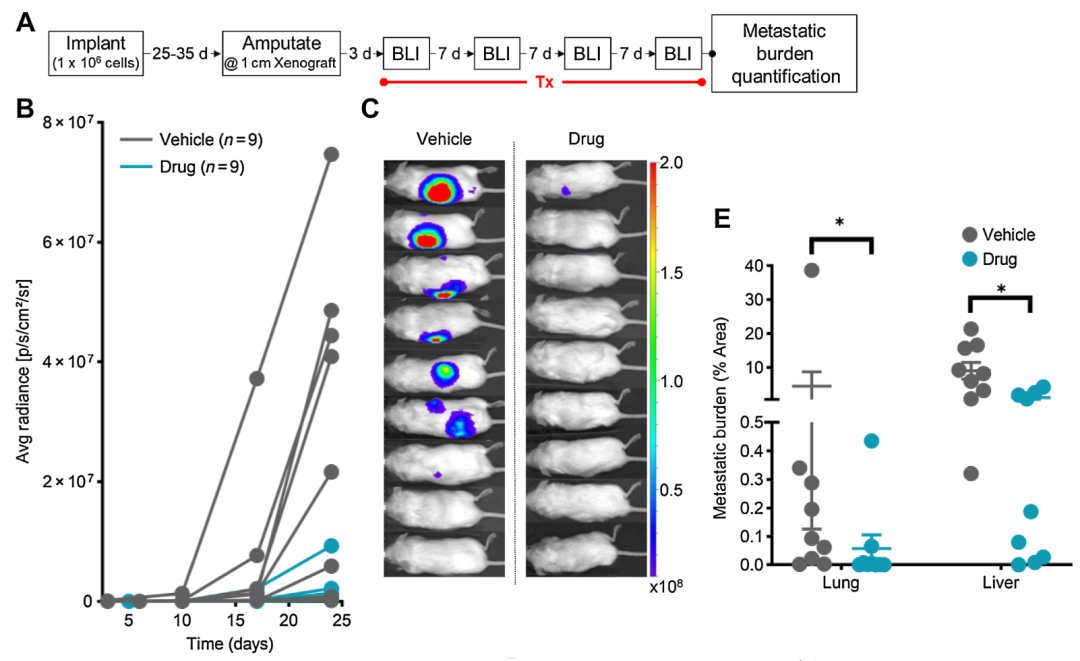
图2. A-实验流程;B-肿瘤生长与时间的线型关系,蓝线-用药组,黑线-对照组;C-小鼠莹光对比图;E-用药组和对照组相比较,在肺和肝转移中显示肿瘤负担的减少
总之,骨肉瘤临床治疗最大挑战是缺乏针对转移机理的了解和充分表达转移表征的模型。Sweet-Cordero团队对八株细胞系在小鼠体内进行了特征分析,并证明它们具有广泛的原位生长和转移进展的型态。在“概念证明”实验中,迪纳西库展示了对肿瘤转移的抑制作用。然而,对患者原位转移与体内转移状态之间的关系,这些细胞系还缺乏清楚的关联。作者们相信这些细胞系的建立能加快对转移机制的了解并在骨肉瘤研究领域有着广泛的应用。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#骨肉瘤#
74
#骨肉瘤# #迪纳西库#
86