初诊至今四年余,肿瘤评价NED!一例直肠癌伴侧方淋巴结转移病例分享
2024-07-30 肿瘤医学论坛 肿瘤医学论坛 发表于上海
该病例是一位64岁的晚期结直肠癌患者,在2010年行结肠癌根治术,2021年复发肝转移。当时,经过MDT讨论,患者被诊断为初治潜在可切除,分子分型显示为RAS和BRAF基因野生型。
01 病例介绍
病例摘要
患者:女,41岁
初诊时间:2019-09-02
主诉:便血伴大便习惯改变1个月
既往及家族史:无特殊
当地医院肠镜:进镜4cm可见环形粘膜隆起突向肠腔,占据肠腔3/4,表面不平,质脆易出血,肠镜勉强通过,进镜20cm可见大量粪便,退镜,病理腺癌。
肛门指诊:距肛缘5cm触及近环周质硬肿物下缘,上极未触及,活动度可,退指指套见血迹。
肿瘤标志物(2019-09-03):CA199至159.9L/ ml 、CA242至64.22IU/ ml。
外院CT:直肠占位伴盆腔内、左侧盆壁和左侧髂血管旁多发肿大淋巴结。
2019-09-04上腹强化 MR :肝右叶后下段异常信号结节考虑血管瘤、肝顶小囊肿。
2019-09-12本院盆腔强化MR:考虑直肠癌,伴直肠系膜、盆腔内及左侧髂脉区多发淋巴结转移。
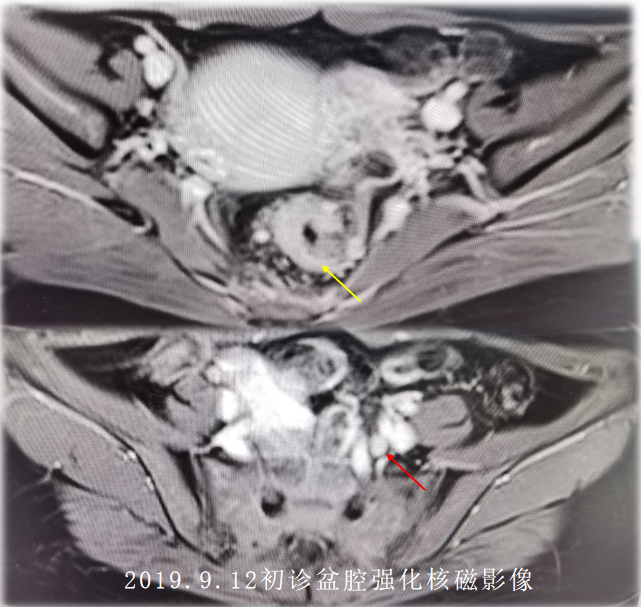
诊断:直肠癌,临床分期:cT3dN2M1a,EMVI(-),MRF(-),非区域淋巴结(髂外动脉旁)阳性。
第一次MDT讨论
问题:先手术?还是先新辅助放化疗?
讨论过程:
1、一点遗憾:目前没有符合循证医学证据的多中心随机对照研究证实优劣。
2、两方争议:
①日本为代表的TME+LLND
依据:LLN视为区域淋巴结,更强调外科手术作用,对术前放化疗持较为保守态度;2019年《大肠癌处理规约》并没有把局部进展期直肠癌的新辅助放化疗作为常规推荐。
②西方欧美国家为代表的新辅助放化疗+TME
依据:LLN转移应该是一种全身性疾病,意味着远处转移;术前新辅助放化疗可以控制LLN的转移不主张做LLND;西方人体质指数较大,增加手术难度和副损伤风险。
3、三方观点:中国的最佳方案:“新辅助放化疗+TME+选择性LLND”
依据:2019年《中国直肠癌侧方淋巴结转移诊疗专家共识》的21条推荐意见。
MDT决策及治疗情况:
1、治疗顺序的选择
①无急症手术指征(出血、穿孔、梗阻)
②先行术前同步放化疗,不加用靶向或免疫治疗(未测MSI)
2019-09-03行第1次XELOX方案化疗;
2019-09-24行放疗(50.4Gy/28f)+同步口服卡培他滨(1.5g*BID)化疗;
2019-11-26行第2次XELOX方案化疗;
2019-12-18行第3次XELOX方案化疗。
初诊4个月时(完成新辅助放化疗后)复查盆腔强化MR:

初诊4个月时(完成新辅助放化疗后)复查上腹强化MR:

初诊4个月时(完成新辅助放化疗后)复查胸部CT:

初诊4个月时(完成新辅助放化疗后)复查肠镜加肿瘤定位:
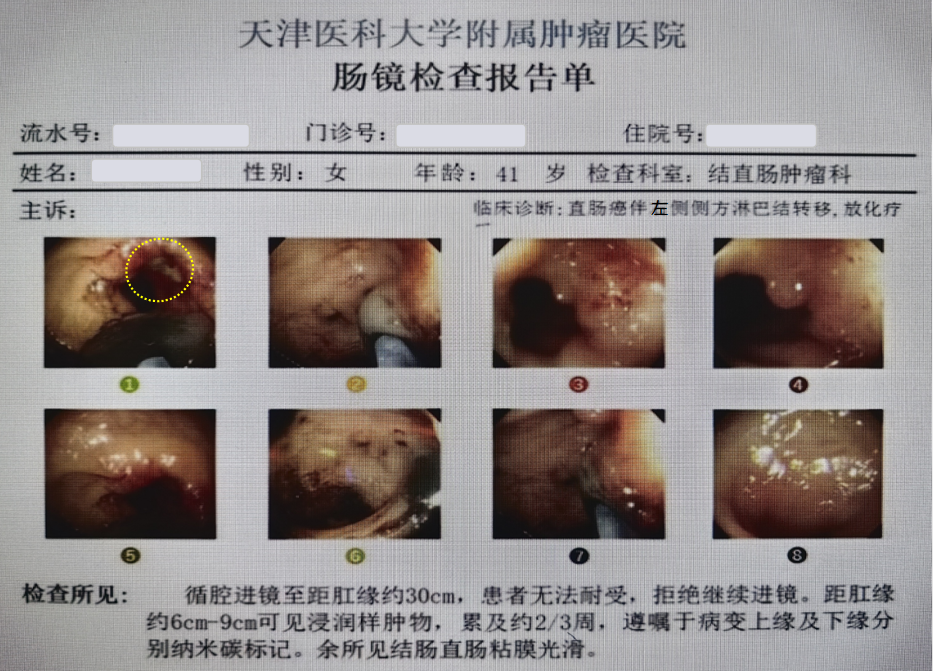
第二次MDT讨论
1、新辅助放化疗效果评估:PR
2、新辅助放化疗是否继续:不继续,拟行手术
3、手术方案主要选择:
①TME+双侧LLND
②TME
③TME+选择性左侧LLND(LD3)(√选择此方案)
4、手术方案其它选择:
①腹腔镜手术
②开腹手术(√选择此方案)
③是/否行回肠预防性造瘘(√选择此方案,行回肠预防性造瘘)
手术情况:

病理报告:

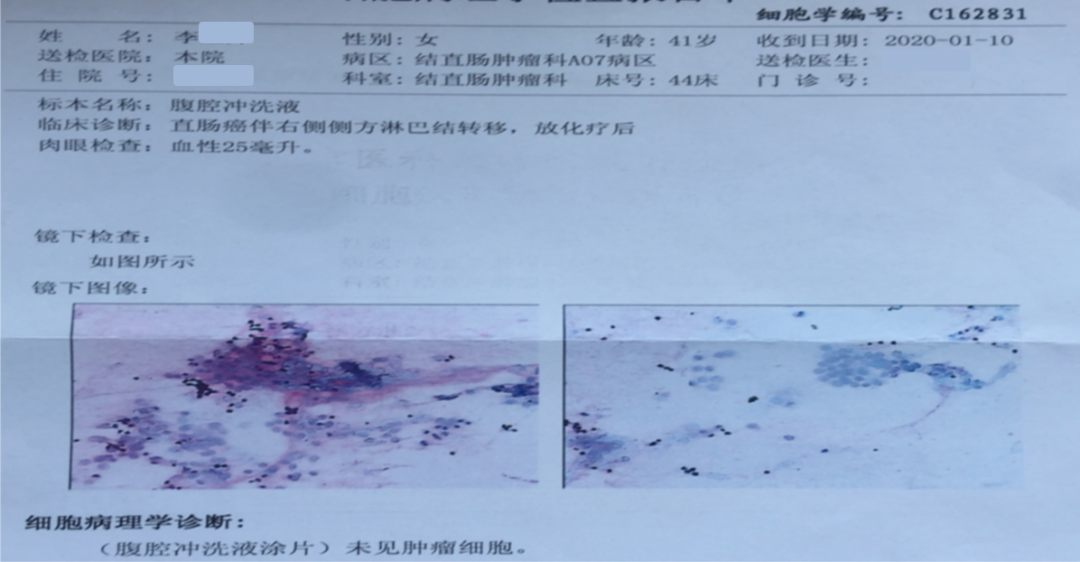
术后化疗及造口还纳:
2020-03-19/04-10/05-05/06-02/06-29开始于我院使用XELOX化疗5周期(加术前3次合计8周期),后2次因血小板减低调减药量延长间隔。
期间定期复查未见异常,2020-07-22复查肠镜如下:
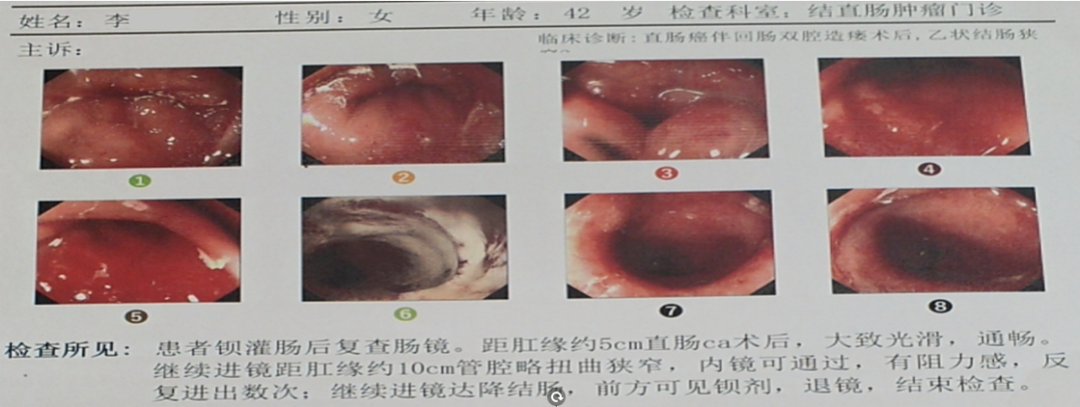
2020-07来院行回肠造口还纳手术,顺利。
术后10个月复查:

术后12个月复查:

术后15个月复查:

术后16个月复查:

术后19个月复查:

右肺中叶结节:2021-04为5×2mm不除外转移,2021-08为7×6mm考虑转移可能性大,故行PET-CT鉴别诊断。
PET-CT显示:双肺纹理清晰,右肺上叶前段及中叶可见多发实性结节影,边界尚清,大者位于中叶,大小约0.8x0.6cm,PET显像可见轻度放射性浓聚,SUVmax为1.5。
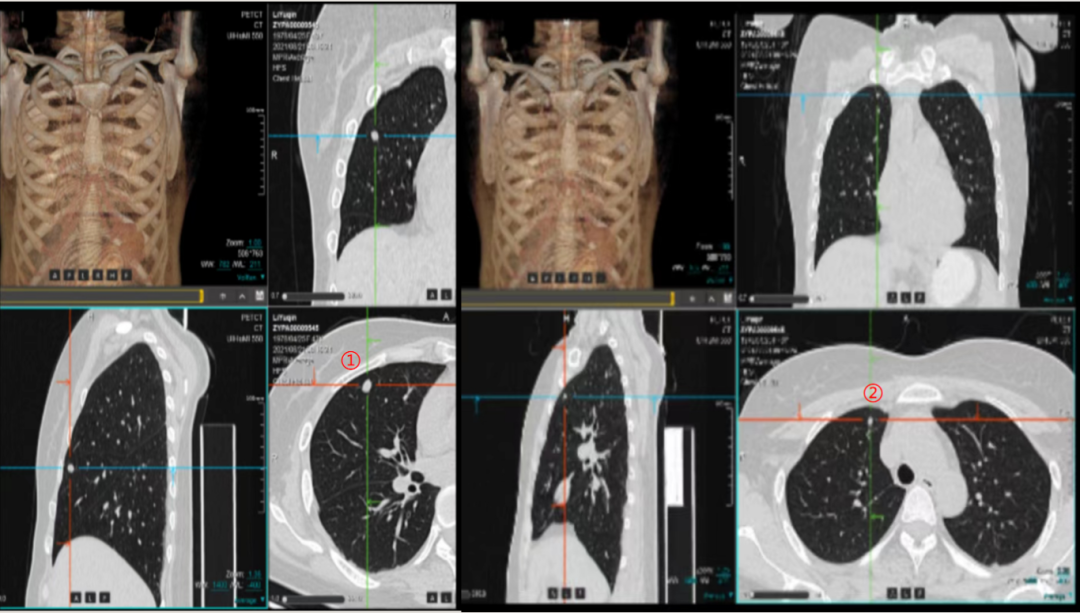
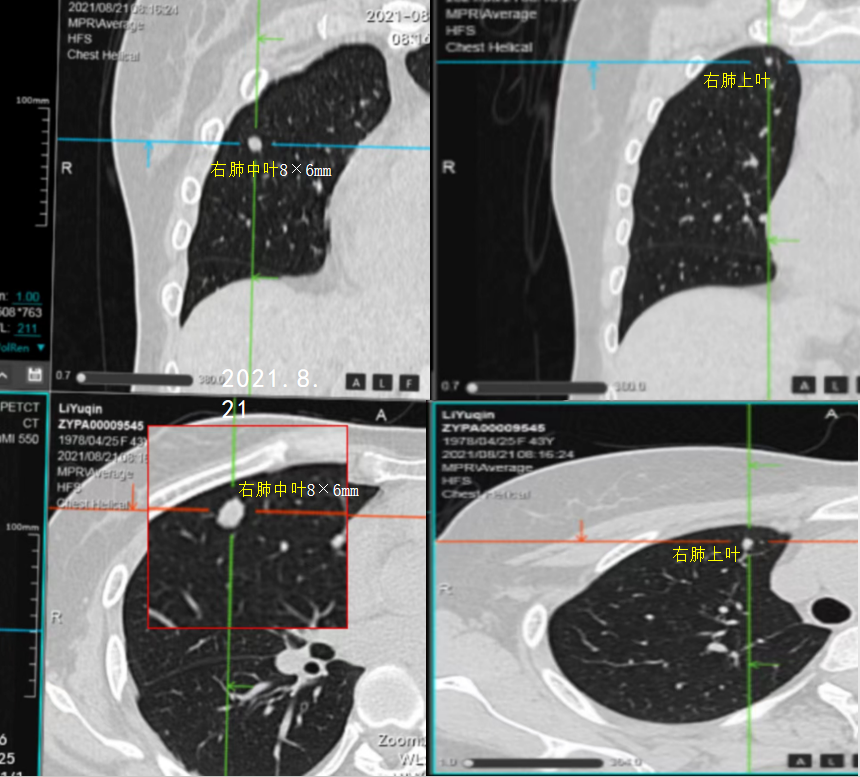
第三次MDT
问题1:术后19个月(停化疗1年余)右肺多发小结节转移是否考虑手术?
1、肺部肿瘤外科:可能存在影像学无法发现转移灶,术后可能再次出现新发肺转移灶,且手术创伤大,不建议直接手术。
2、患者及家属:担心复发转移风险及手术后生活质量,不愿手术,要求综合治疗。
问题2:是否加用靶向或免疫治疗?
①西妥昔单抗
②贝伐珠单抗
③PD-1
患者院外自行基因检测:MSS,TMB-L,KRAS、NRAS、BRAF、PIK3CA、HER2、EGFR、NTRK1\2\3未见突变,ZFHX3缺少突变,APC点突变,POLE缺失突变,NBN缺失突变。
问题3:术后19个月(停化疗1年余)右肺多发小结节转移是否调整化疗方案?
①FOLFOXIRI(3药联合效力强,副反应增大,强力转化首选;患者体质稍弱)
②FOLFIRI(较方案①副反应减轻,患者对伊立替康副作用存在畏惧)
③XELOX(术后辅助化疗8周期)(既往有效,副反应较轻可耐受,曾使用8个周期敏感度可能降低)
④mFOLFOX(√副反应一般较轻,敏感性亦可能降低,患者及家属研究后接受此方案)
结合患者和家属意见的第3次MDT决策:
1、征得知情同意后调整化疗方案为mFOLFOX6;
2、先加用西妥昔单抗(RAS/BRAF野生型、MSI-L),暂不加免疫治疗 ;
当时医院有免费的临床试验mFOLFOX+西妥昔单抗,要求入组条件:肿瘤直径达到1cm;
观察等待期:2021-08-12至2021-10-08,未行化疗等治疗,行强化CT对比:右肺中叶结节(8×6mm)至(9×7mm)。

达到入组临床试验标准后开始晚期一线化疗:
2021-11-25复查CT达到入组标准,于2021-12-02开始入组临床试验mFOLFOX+西妥昔单抗。
因白细胞、血小板减低完成化疗6周期,完成西妥昔单抗治疗10次,后出现低镁血症对症治疗效果欠佳,患者本人不愿继续治疗出组。
疗效评估:2022-03-21复查CT对比2021-11-25 CT:右肺中叶结节直径仍为1.0×0.7cm,病情稳定SD。

2022-03晚期二线化疗尝试1次FOLFIRI无法耐受。
2022-04-19日开始晚期三线化疗:
TAS-102:早晚餐后第1-5天、8-12天用药(第6.7天停药),之后休息16天,每28天一个疗程。
2022-04-19日开始TAS-102化疗,疗效评估为SD,因血小板低停药。
2023-05-16复查:晚期三线停用TAS102后4个月,右肺中叶结节较前增大。

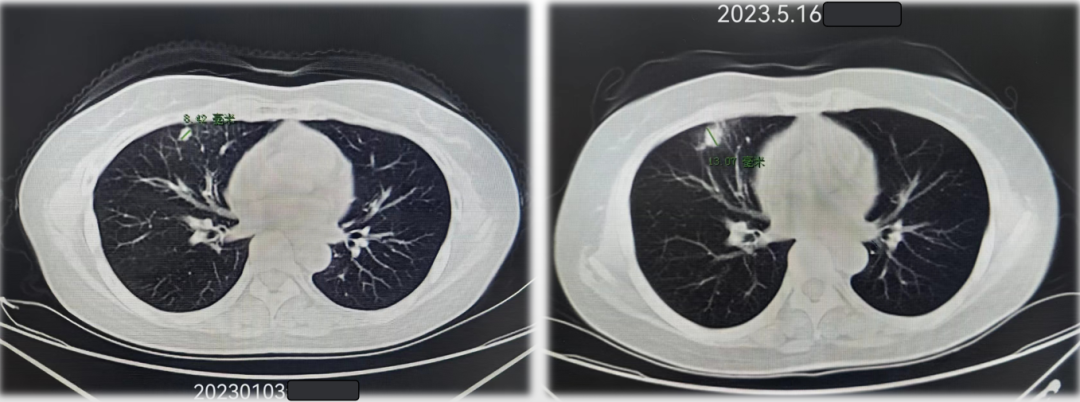
2023-06放疗(PTV/54Gy/3f):
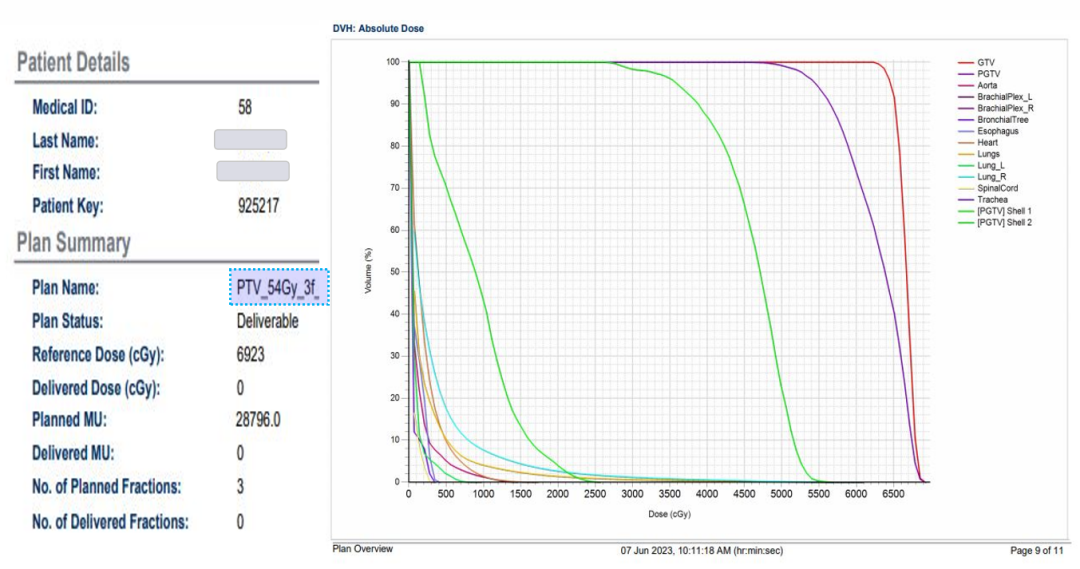
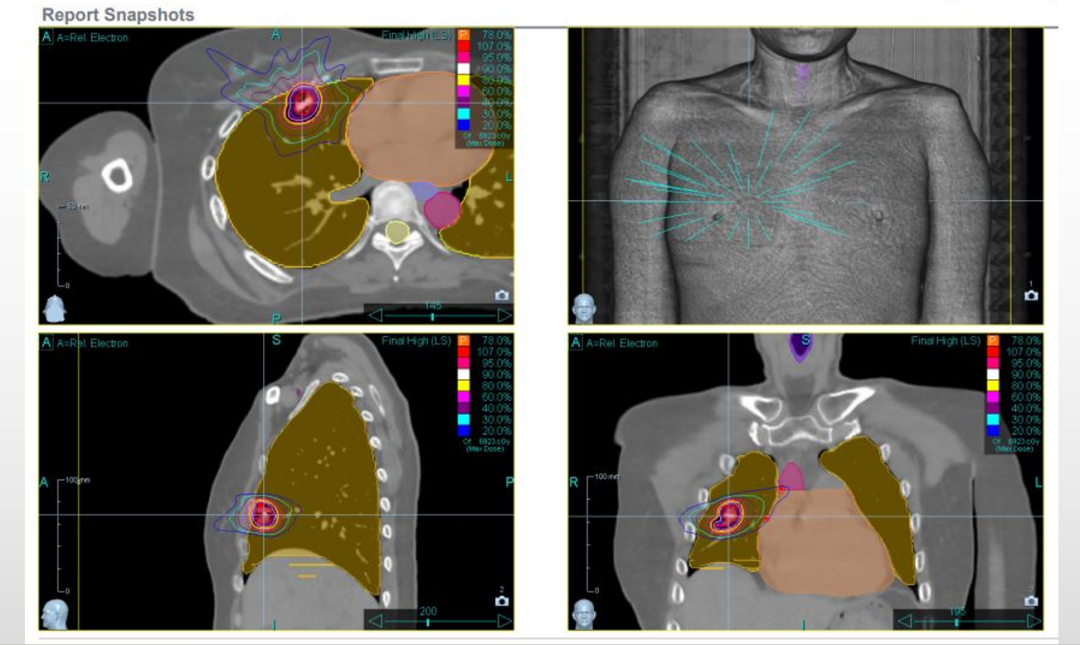
2023-06放疗后定期复查对比:

2024-01-04复查胸部强化CT:
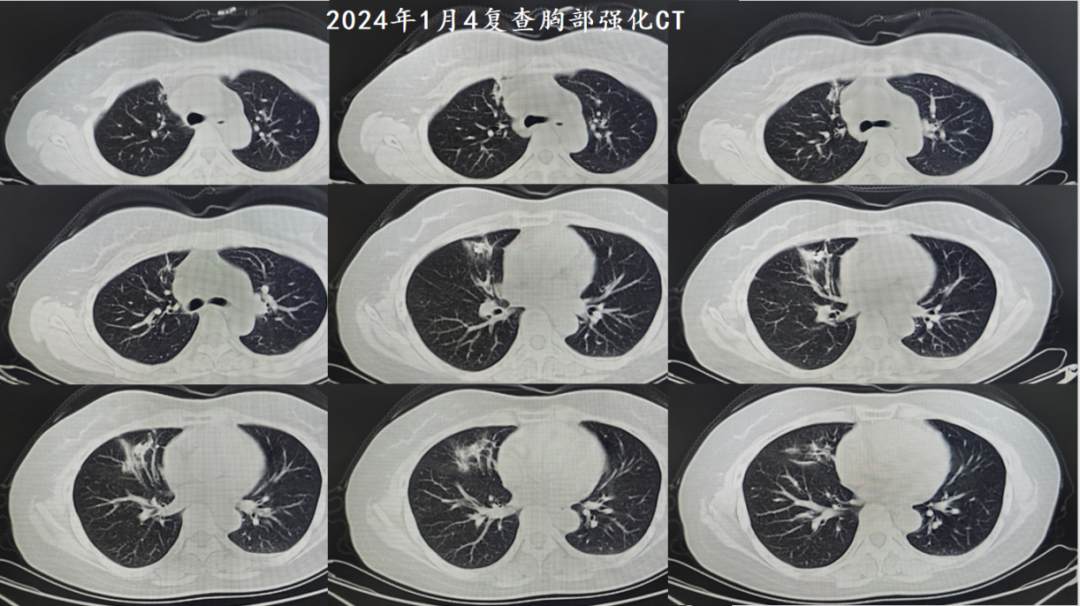
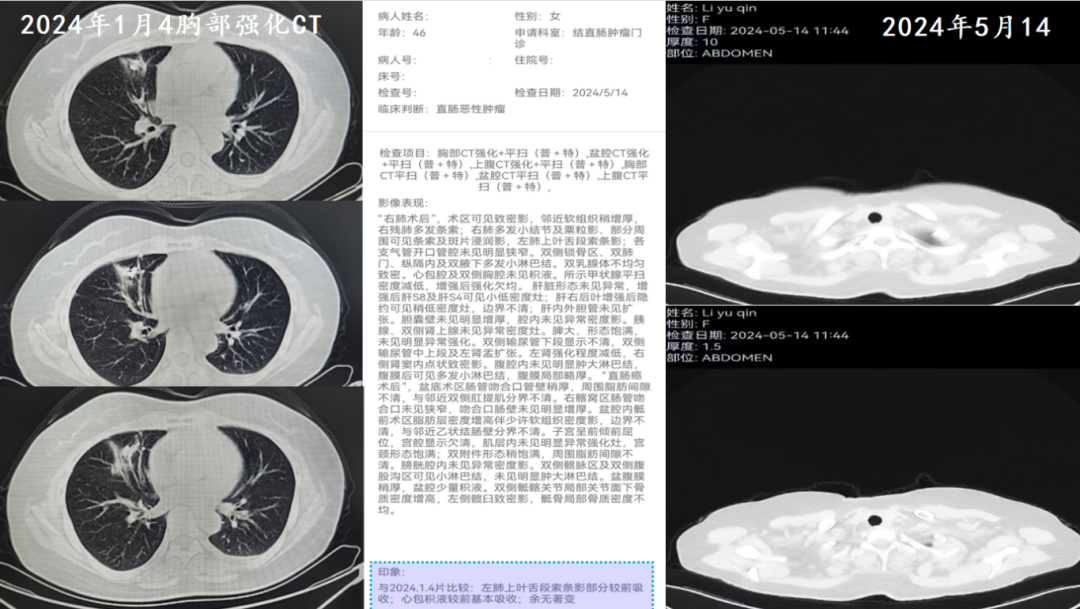
治疗经过小结
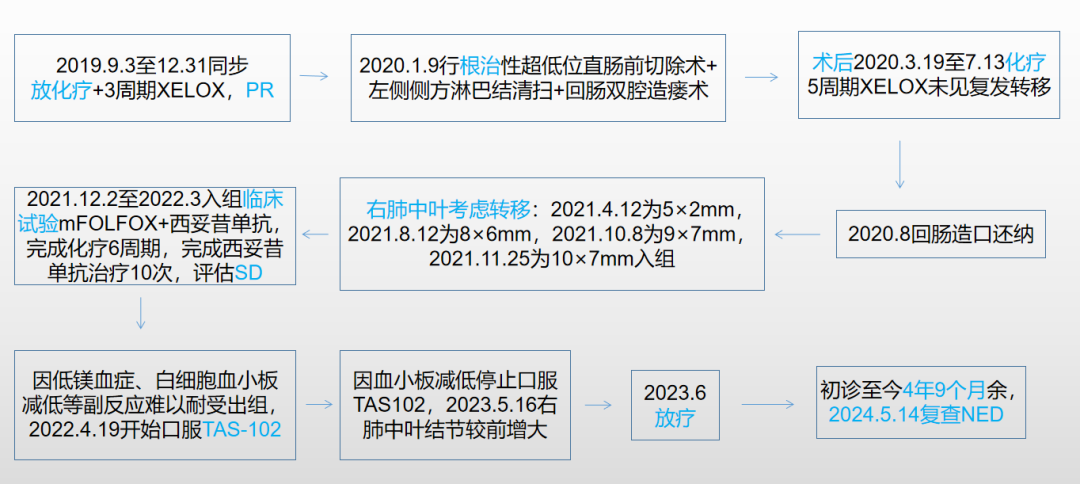
02 病例讨论
问题 1:请根据您的专业谈谈该病例的整个治疗过程,有什么可以优化的地方?对于侧方清扫您持怎样的观点?
天津市人民医院-肛肠外科-宇永军:侧方淋巴结清扫一直是一个备受争议的话题。最初由日本学者提出侧方淋巴结清扫的必要性,而西方欧美学者对此比较抵触,认为一旦发生侧方淋巴结转移,应视为远处转移,所以他们不建议做侧方清扫,而建议做放化疗新辅助来代替侧方清扫。日本学者则认为,只要能够进行侧方清扫,早期即便是在腹膜反折以下也应进行预防性的侧方清扫。所以说两派的观点一直是存在着争议的。而国内对此持有一种中立或者说选择性接收的态度。关于侧方清扫的界定问题,早期我们以0.5厘米作为转移的界定标准,后来提高至0.8厘米,目前普遍接受的是核磁共振成像显示0.7厘米,我们就认为是考虑转移了。
然而,阳性率一直是侧方清扫的一个诟病。很多的中心从中科肿瘤到天津肿瘤再到我们自己的中心,尽管进行了大量侧方清扫手术,但阳性率普遍偏低,文献报道的总体阳性率大约在7%到15%之间,我们做了很多清扫也发现发现实际的阳性率并不高。
但是总的来说,我认为侧方还是非常有意义的。尤其我们这个病人,我们可以看到他从这个手术也好,侧方清扫也好,到后续的这些治疗来说都是非常正确的选择,而且患者最终得到5年的生存获益,这是相当的不容易的。
天津中西医结合医院-胃肠外科一-杨士民:庄教授介绍的病例非常成功,患者自治疗以来已存活近4年9个月。这个病例不仅展示了当前治疗的总体趋势,也反映了目前患者的状况。尽管国家已经实施了大肠筛查,但数据显示,在初次就诊时,有43.8%的患者已经出现了远处转移或腹腔及淋巴结转移。这位患者并非很早期,根据指南应该接受新辅助放化疗,而庄教授也严格遵循了指南进行治疗。
关于侧方淋巴结清扫的问题实际上目前争议也是比较大的。就像宇永军教授所述,日本过去在腹膜反折以下都主张进行侧方淋巴清扫,但鉴于统计数据显示转移率仅为15%左右,且大多数为阴性,目前日本也不再进行预防性清扫,而是采取治疗性清扫。在我们中心,侧方清扫手术做得并不是很多,但是做侧方的时候大部分也是先进行新辅助放化疗。我统计的阳性率相对较低,通常只有2%到3%,这可能与放化疗有很大关系,因为肿瘤可能已经退缩。
关于这个患者的治疗,我有几个问题。首先,新辅助应该做多长时间这个呢?我们中心做的时间稍微长一点,通常进行5到6个周期的新辅助,虽然指南建议通常在两到三个月后进行手术。我认为这个时间可能需要进一步讨论一下,因为延长新辅助时间可能会带来更好的效果,但也存在错过手术时机的风险。另外关于PET-CT的使用,我认为早进行PET-CT检查可能有所帮助,但也不能保证能够,可能结节较小不能发现或无法确诊。此外,患者的后期治疗也用得也非常好,包括基因检测、西妥昔单抗的化疗以及TAS-102的使用。TAS-102是近两年新出的效果比较好的药物,这位患者经过TAS-102治疗后,肿瘤状态达到SD,还是非常幸运的。患者还有一个特殊之处,即经过放化疗后,原发灶为阴性而淋巴结为阳性,这种情况比较少见。此外,我认为射频消融可能也是一个值得考虑的早期治疗手段,可能会带来更好的预后。
总之,这个病例非常成功,遵循了指南标准的治疗方案,并具有一定的创新性。TAS-102为许多结直肠癌患者,无论是转移还是未转移的晚期患者,提供了一个非常好的治疗选择,同时也提高了患者的生活质量。
天津医科大学第二医院-肿瘤科-王丽丽:患者比较年轻,41岁,初诊时为局部晚期直肠癌患者。在天津医科大学肿瘤医院MDT团队的共同努力下,患者接受了同步放化疗,成功降低了肿瘤分期,并随后完成了手术。术后,患者还完成了六个周期的辅助化疗。然而,在术后约19个月,患者出现了肺部结节转移,这些结节在定期监测中明显增大。随后,患者接受了晚期一线治疗,包括西妥昔单抗和mFOLFOX化疗方案,疗效评估为SD。之后,患者采用了TAS-102治疗方案,这个TAS-102药物的使用时间还是挺长的,用药期间病情稳定,但停药四个月后再次复查,肺部肿瘤增大三毫米,评估为病情进展。随后为患者的这个病灶融入了局部放疗,目前病灶基本消失,患者仍在密切随诊治疗阶段。
从这个病例中,我们可以看到,对于晚期肠癌患者,尤其是局部晚期患者,确实需要多学科MDT团队的协作确定何时进行手术、放疗和化疗的介入时机。此外,当肿瘤出现寡进展或寡转移时,局部治疗手段在全身治疗有效的基础上联合使用,可以显著提高患者的生存获益。第三点是关于个性化诊疗的重要性。TAS-102药物在国内上市已有一段时间,无论是在结肠癌还是胃癌中都有应用。与卡培他滨相比,TAS-102在手足综合症、皮疹、骨髓毒性和胃肠道反应方面有显著改善,适合作为比较长期的维持治疗方案。国外一些多中心研究也表明,对于不能耐受三药或两药化疗的高龄患者,TAS-102联合贝伐珠单抗的治疗效果也不错。
从庄教授的病例中,我们看到了外科医生严谨的思维和MDT团队各学科的融会贯通,为患者制定了非常好的指导决策。
03 MDT小结
该病例是一位64岁的晚期结直肠癌患者,在2010年行结肠癌根治术,2021年复发肝转移。当时,经过MDT讨论,患者被诊断为初治潜在可切除,分子分型显示为RAS和BRAF基因野生型。通过西妥昔单抗联合双药化疗的转化治疗,患者达到了显著的疗效。值得称赞的是,该病例在关键治疗节点均有MDT团队的参与。
该病例患者是一位41岁女性,患有直肠癌。手术后,接受了新辅助放化疗并进行了手术,在术后19个月复查发现肺部结节,考虑转移并行PET-CT检查。而后进行mFOLFOX+西妥昔单抗,病情评估SD,因低镁血症、白细胞血小板减低等副反应难以耐受停止,接着使用TAS-102化疗,用药期间疗效良好,停药四个月后右肺中叶结节较前增大,后续进行放疗。令人鼓舞的是,患者初诊至今(2024-06-20)已有4年9个月余,2024-05-14复查NED。这得益于庄教授及MTD 团队制定的治疗计划,为患者制定了非常好的治疗策略,让患者的生存期得以延长。
述评
天津市人民医院 -肿瘤科-阎皓:这个患者初次诊断还是比较晚的,在新辅助治疗以后,能拿到PR的结果,说明情况还是比较好的。但是在辅助治疗完成以后 9 个月出现了一个肺转移病灶,实际上,在这种情况下不好判断它是不是一个真正的寡转移病灶,我们看到 MDT团队也不太确定这是不是只是一个单一病灶。在后续的全身治疗以后,这个病灶仍然是一个孤立性病灶,在给予局部治疗以后,患者目前就达到了NED的状态,也期待后续有更好的消息。
总之,MDT团队的参与给患者的治疗决策带来了一定的帮助,患者生存期的延长得益于庄教授及MDT团队的规范治疗和全程管理。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#直肠癌# #侧方淋巴结转移#
52