JCO:Dara-CVRd诱导联合ASCT和延长巩固可改善超高危NDMM预后
2023-06-26 聊聊血液 聊聊血液 发表于上海
该试验是第一项针对超高危 NDMM 和 PCL 的试验,在随访超过3年的难治性人群中显示大部分可持续缓解。
超高危多发性骨髓瘤
多发性骨髓瘤(MM)的预后已经得到显著改善,但仍有25%的患者会在初始治疗后2年内复发,即使接受移植。这类患者尚无最佳治疗标准,复发后治疗的生存获益也较少。超高危 (UHiR) MM 患者迫切需要早期、预先识别和改进、定制的一线治疗方案来诱导和维持疾病控制。
预测 UHiR NDMM 的分子学标志物包括:(1) 同时出现≥两个独立遗传风险标志物(即“双打击”):典型易位t(4;14) 或t(14;16)/t(14;20) 和拷贝数畸变del(1p)、gain(1q) 或del(17p);(2) 基因表达谱 (GEP) 签名如SKY92,它们独立于双打击,并与肿瘤增殖相关。此外原发性浆细胞白血病 (PCL) 的典型特征为高增殖率和 SOC 治疗后早期复发,类似于UHiRMM。
回顾性探索性分析表明,在更年轻、更fitter的患者中,ASCT 之前(尤其是之后)的强化治疗联合后续巩固和维持治疗(包括达雷妥尤单抗)可改善 UHiR 患者的结局,但尚缺乏UHiR NDMM 或 PCL 患者中获益的前瞻性对照证据。鉴于UHiR/PCL 的罕见性,随机临床试验并不可行,且标准治疗的不良结局使传统试验设计在伦理上颇受质疑;而前瞻性外部对照试验设计可比单臂试验数据提供更多的临床背景,尤其是当关注严格定义的患者组时。
II期OPTIMUM (Myeloma UK nine) 试验是一项 “数字对照臂(digital comparator arm)”试验,使用达雷妥尤单抗、环磷酰胺、硼替佐米、来那度胺和地塞米松 (Dara-CVRd) 强化诱导和巩固方案联合ASCT治疗UHiR NDMM 和 pPCL 患者,并将其方案定义的结果与几乎同时进行的Myeloma XI/XI+(此处称为MyeXI)试验中完全分子学匹配的 UHiR NDMM患者进行比较。试验结果曾发布于2021年ASCO(随访22个月)和2022年ASH大会(随访27.1个月),计划的最终随访(中位41.2个月)结果近日发表于《Journal of Clinical Oncology》。


试验设计
OPTIMUM试验对比了ASCT前后Dara-CVRd的强化治疗与外部标准治疗(来自同期的III期MyeXI试验,包括PI/IMID诱导,ASCT,来那度胺维持治疗);此外进行分子学匹配,可控制潜在的偏倚和内在的不确定性。
OPTIMUM试验纳入根据IMWG标准确诊为症状性 NDMM 并患有 UHiR 疾病的患者。UHiR的确定是基于遗传学【≥2种高危因素:t(4;14)、t(14;16)/t(14;20)、gain (1q)、del(1p)、del(17p】,或存在 MMProfiler SKY92 GEP 签名,或PCL患者(循环浆母细胞>20%)。
患者接受 Dara-CVRd 诱导治疗至最大缓解(或最多6个诱导周期),ASCT,巩固治疗第1部分Dara-VRd 治疗6个周期,巩固治疗第2部分Dara-VR 治疗12个周期, Dara-R 维持治疗直至疾病进展。具体如下图所示。
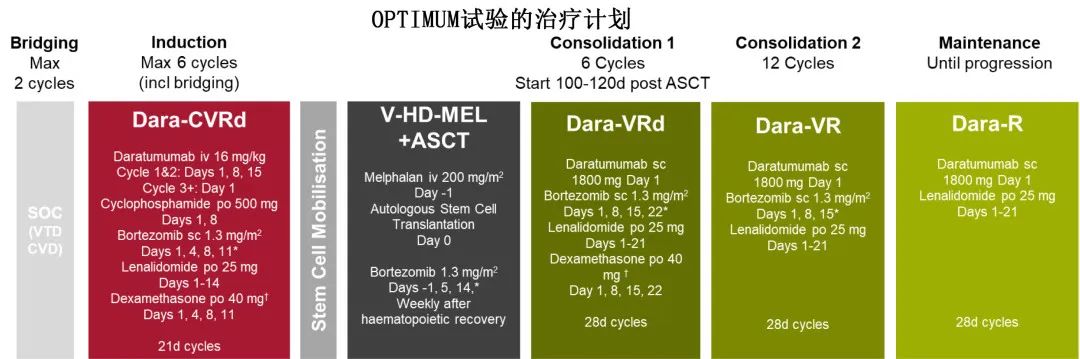
评估疗效的主要终点为根据筛选方案注册后18个月的 PFS (PFS18m);期中无效分析的主要终点为 ASCT 后100天的 MRD 状态和 ASCT 后100天的PFS(或相当于未进行 ASCT 的患者的12个月)。
次要终点包括作为至事件时间终点的PFS(与 MyeXI 的关键探索性比较);安全性和毒性(根据不良事件通用术语标准V4.0分级);MRD缓解;最大缓解(根据 IMWG 标准定义);治疗依从性和OS。所有结局的定义均与 MyeXI匹配。
试验结果
患者流程和基因检测
进行 OPTIMUM 筛查后107例患者提供知情同意书并合格(图1)。
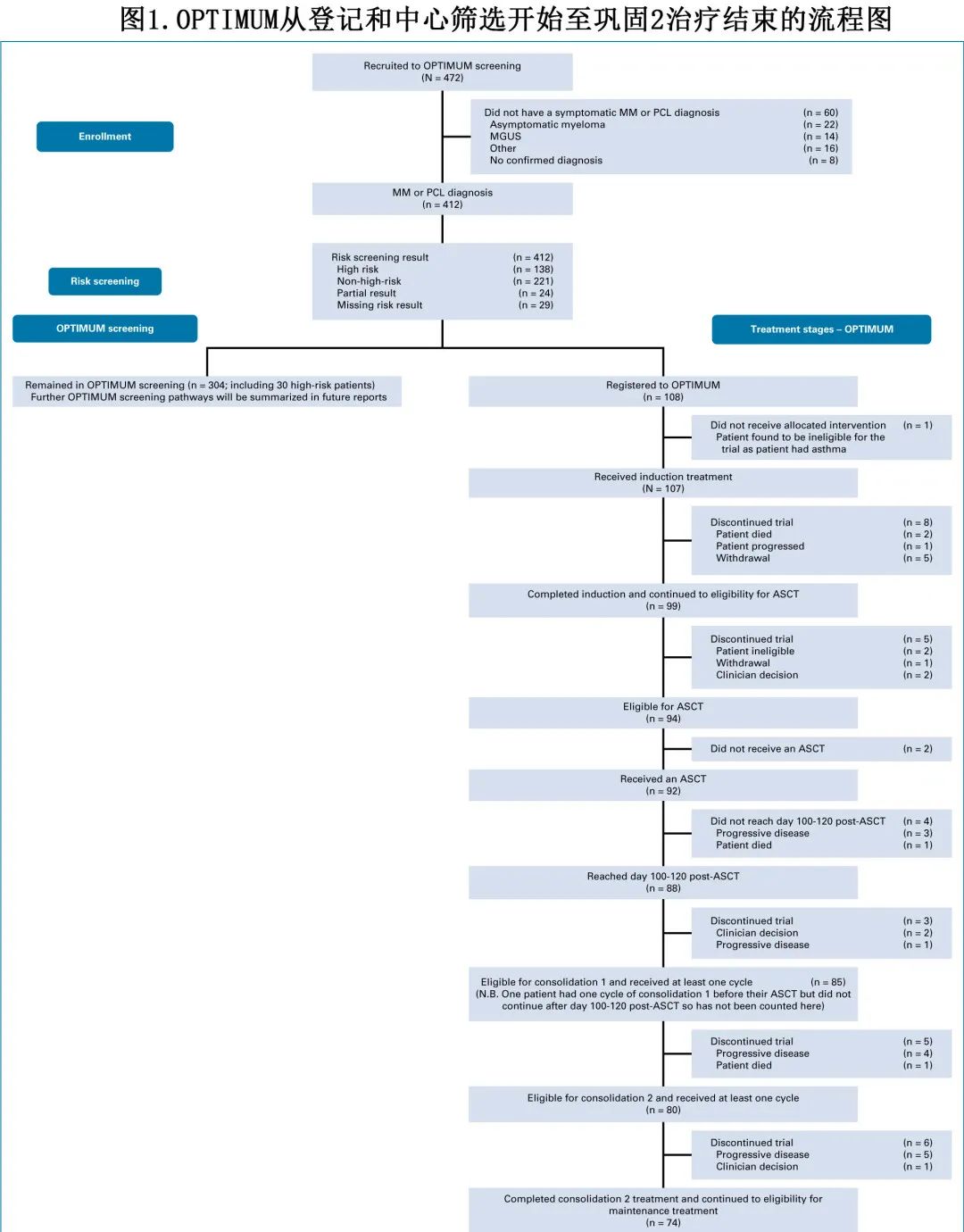
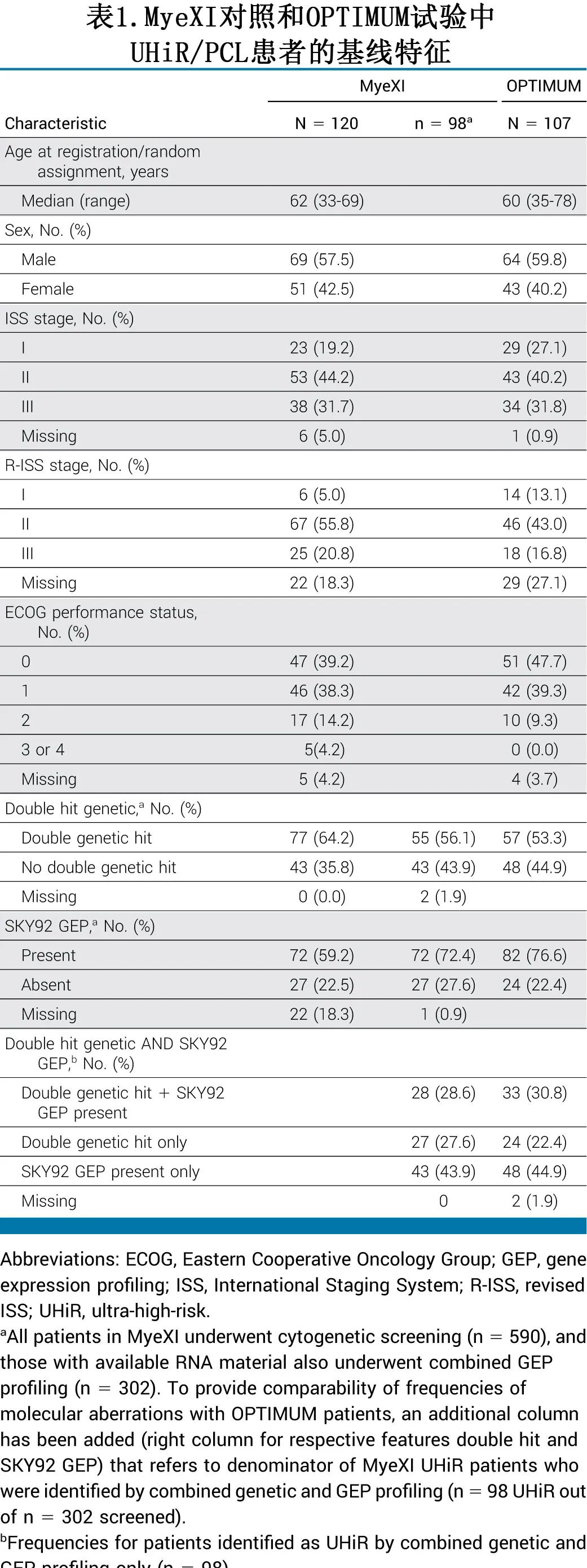
107例患者中,57例 (53%) 为双打击遗传学,82例 (77%) 为SKY92 GEP,33例 (31%) 为双打击和SKY92 GEP(表1)。所有107例 OPTIMUM 患者均接受了至少一次试验治疗,因此被纳入分析中;92例接受了ASCT,85例在 ASCT 后第100-120天接受了巩固1治疗,80例接受了巩固2分析(图1)。
MyeXI数字对照
总共有590例随机分配到 CRD 或 KCRD 的 MyeXI 患者可用于风险分析,其中302例根据 OPTIMUM 进行细胞遗传学和 SKY92 GEP 联合风险分析,另外288例患者仅评估了细胞遗传学信息,因为缺乏用于 GEP 分析的 RNA 材料。分析确定了120例具有 UHiR 特征的患者,并纳入 MyeXI 数字对照中。基线特征总结见表1。
生存分析
103例 OPTIMUM 患者具有可确定的 PFS18m 状态,其中84例患者 (81.7%) 在 OPTIMUM 登记后18个月时存活且无进展,而 MyeXI 中117例可评估患者中有77例 (65.9%)。根据贝叶斯框架,OPTIMUM治疗患者的 PFS18m 优于 MyeXI 治疗患者的概率为99.5%,超过预定义的85%阈值,具有意义的改善(图2A)。
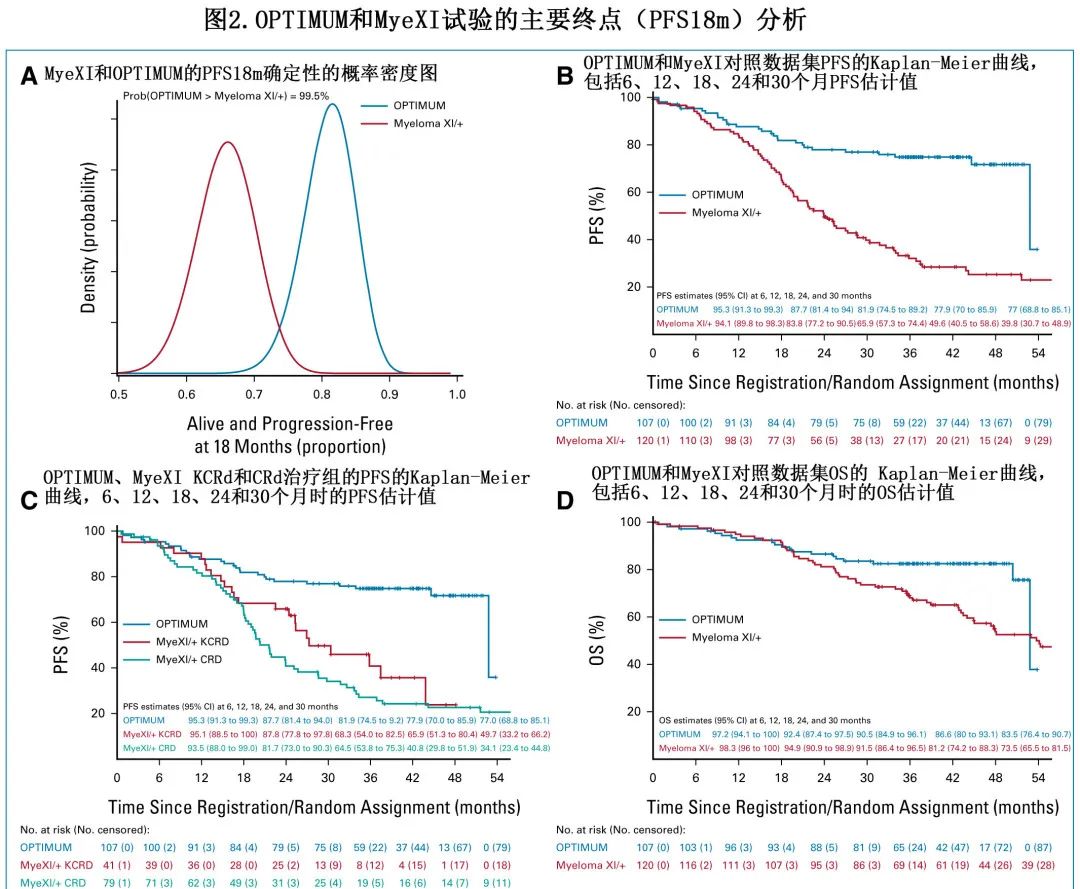
18个月后观察到 PFS 曲线分离增加,继续支持 OPTIMUM 治疗。30个月时OPTIMUM组的 PFS 率估计值为77.0%,而 MyeXI 组为39.8%(图2B),其中 KCRd 组为49.7%,CRd组为34.1%(图2C)。OPTIMUM 和 MyeXI 30个月OS 率估计值分别为83.5%和73.5%(图2D)。
分析时OPTIMUM中的28例患者发生进展事件(24例疾病进展和4例死亡)。中位随访41.2个月,尚未达到中位 PFS 和 OS。
缓解和MRD情况
诱导结束时和 ASCT 后100天内的最大缓解见表2。在巩固治疗1结束时,73例患者达到CR (68.2%),而24例达到VGPR (22.4%),5例达到PR(4.7%)。
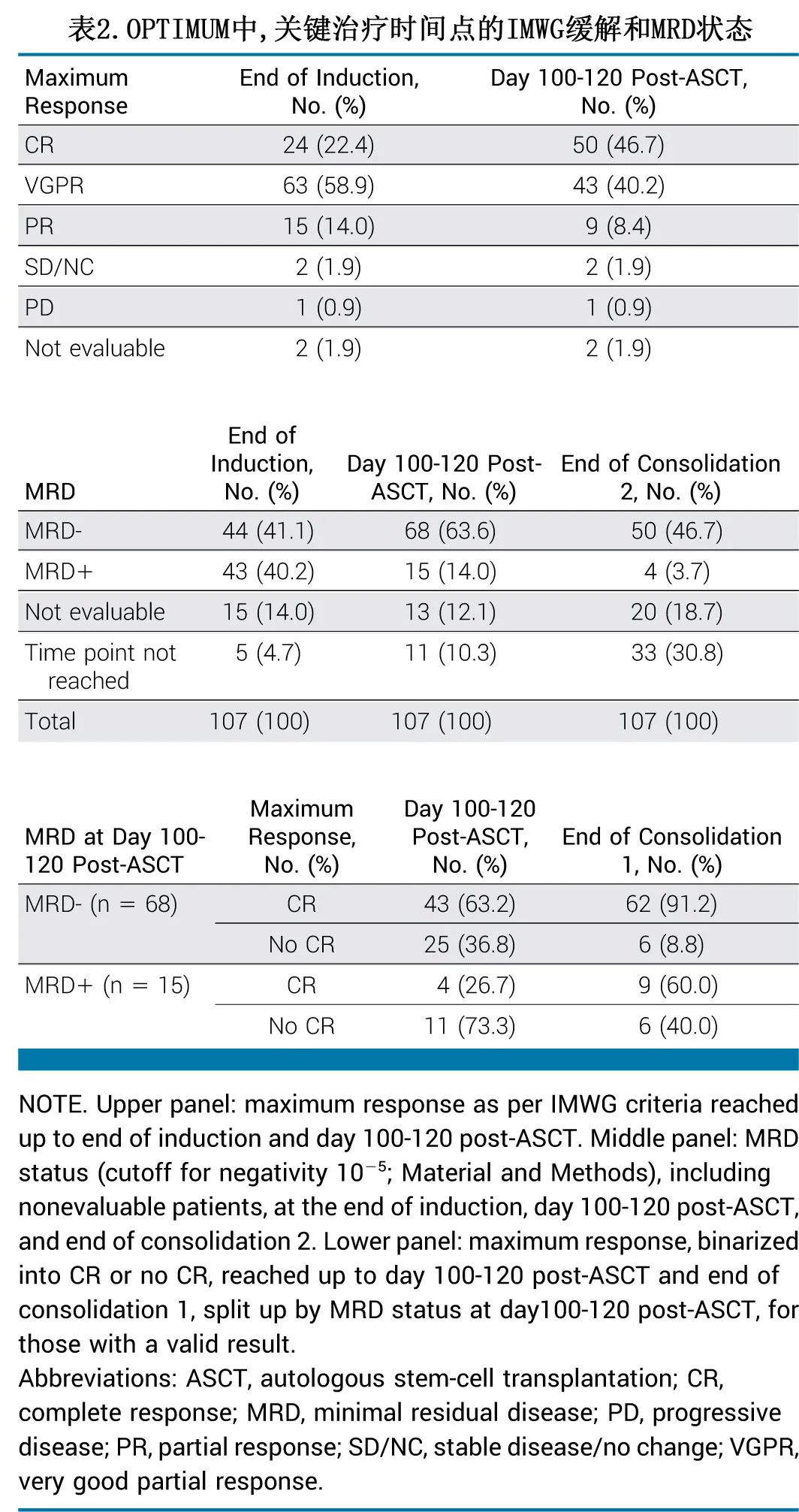
诱导结束时44/107例 (41.1%) 达到 MRD 阴性,并在 ASCT 后100-120天增至68例 (63.6%)(表2)。在第100天 MRD 阴性的68例患者中,43例 (63.2%) 在第100天也为CR, 62例 (91.2%) 在巩固治疗1结束时达到CR。此外,ASCT后100-120天 MRD 阴性的患者中有84.0%在巩固治疗2时仍为 MRD 阴性(不包括巩固治疗2结束时无法评估的18/68例患者)。
安全性和给药
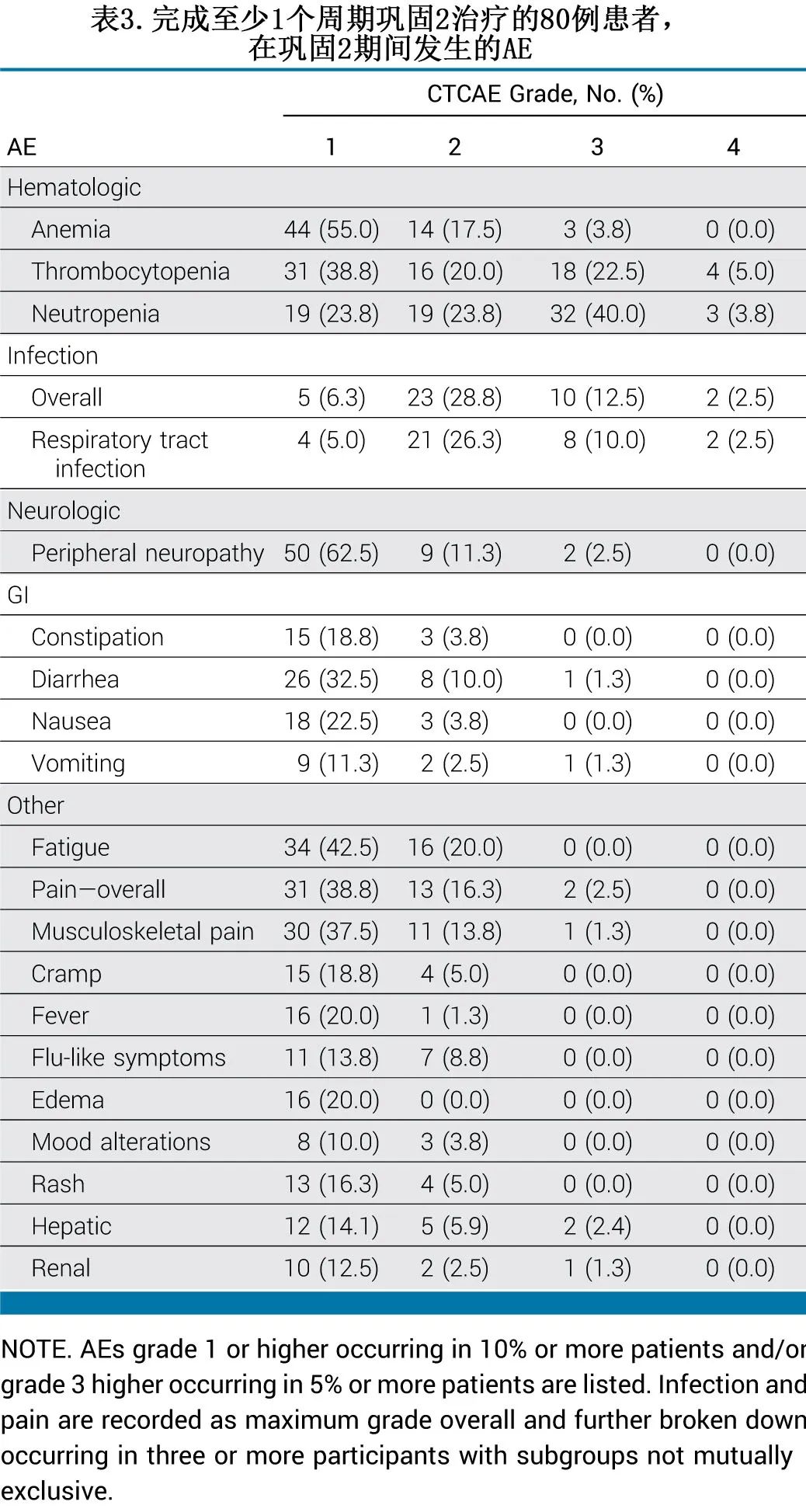
强化 Dara-VRd 巩固2治疗期间的 AE 总结见表3。强化巩固治疗期间发生的主要血液学3/4级 AE 为血小板减少症 (22.5%) 和中性粒细胞减少症 (40.0%) 以及主要非血液学 AE 感染 (12.5%),与诱导和巩固治疗期间观察到的 AE 一致,未出现新信号(表3)。
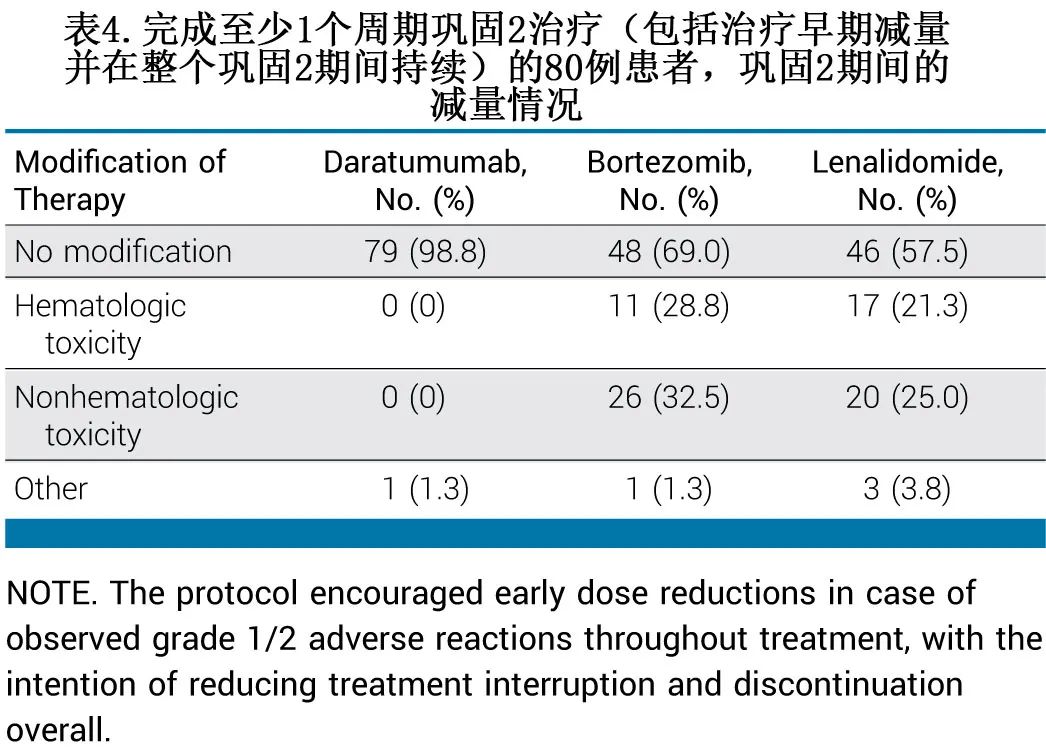
99例患者 (92.5%) 完成了预先计划的诱导治疗,其中5例患者 (4.7%) 在完成一个周期前停止治疗。在开始巩固治疗1的85例患者中,79例 (92.9%) 完成了计划的6个周期治疗。患者在 COVID-19 大流行的第一波期间继续治疗,此时大多数正在接受巩固1或2治疗。巩固治疗2期间的剂量降低信息见表4。在巩固治疗2之前和/或期间,31.0%的患者降低了硼替佐米剂量,42.5%的患者降低了来那度胺剂量,而几乎所有 (98.8%) 患者均以预先计划的剂量给予了Dara。
总结
OPTIMUM试验中103例UHiR 或PCL接受Dara-CVRd 五药诱导治疗,MyeXI试验的 117例UHiR 的患者组成外部对照组,具有与 OPTIMUM 相当的临床和分子特征。根据贝叶斯框架的 PFS18m 比较显示,OPTIMUM 优于 MyeXI 的概率为99.5%。在30个月随访时,OPTIMUM和 MyeXI 的 PFS 分别为77%和39.8%,OS分别为83.5%和73.5%;OPTIMUM超过三年随访仍未达到中位PFS。强化 Dara-CVRd 诱导和 ASCT 可为UHiR/PCL 患者带来ASCT 后的高 MRD 阴性率,且大多数患者通过 Dara-VR(d) 巩固治疗可维持阴性。此外ASCT 后延长 Dara-VRd 巩固治疗的给药率高,毒性有限。
该试验是第一项针对超高危 NDMM 和 PCL 的试验,在随访超过3年的难治性人群中显示大部分可持续缓解。与常规治疗相比,Dara-CVRd诱导和 ASCT 后延长 Dara-VRd 巩固治疗可显著改善UHiR NDMM 患者的PFS,值得进一步评价该策略。
参考文献
Kaiser MF,et al.Daratumumab, Cyclophosphamide, Bortezomib, Lenalidomide, and Dexamethasone as Induction and Extended Consolidation Improves Outcome in Ultra-High-Risk Multiple Myeloma.J Clin Oncol . 2023 Jun 14;JCO2202567. doi: 10.1200/JCO.22.02567.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













