读书报告 | 黑色素瘤获得性耐药的多器官景观
2024-07-20 iCombo iCombo 发表于上海
本研究中产生的基因特征可以应用于许多其他快速尸检队列和正在进行的临床试验,从而调整数据处理技术,建立一个位点特异性的黑色素瘤转移平台,还可以预测药物反应和器官微环境对治疗的影响。
导读
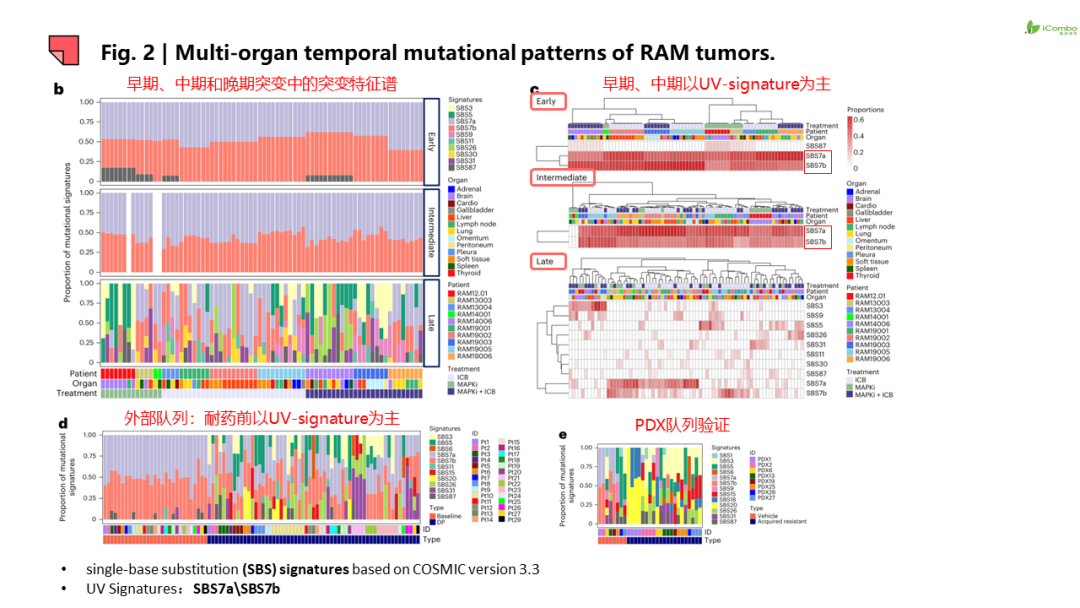
目前尚不清楚MAPK抑制剂(MAPKi)/免疫检查点阻断(ICB)治疗抗性如何改变皮肤型黑色素瘤(CM)突变景观。转移导致大多数癌症相关死亡,而CM是转移性最强的肿瘤之一。然而,由于难以获得患者来源的转移组织,限制了对临床转移和器官特异性演变的理解。临床上对转移灶及其位点特异性宏观环境之间的共适应知之甚少。
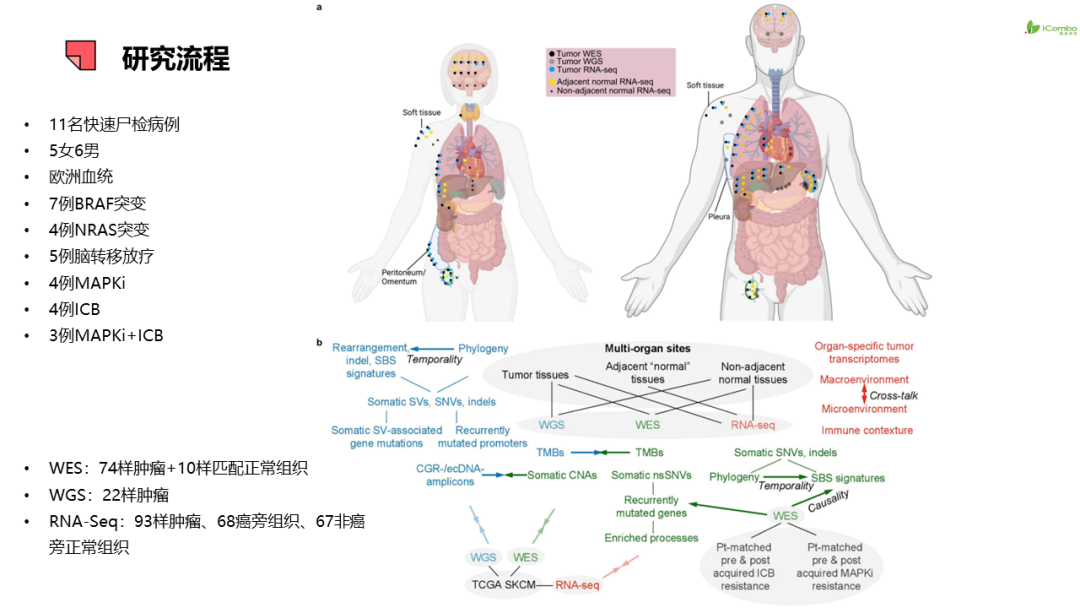
本研究从BRAF-mut或NRAS-mut CM患者中组建了一个快速尸检黑色素瘤(RAM)队列,这些患者接受了MAPKi/ICB治疗并最初对MAPKi/ICB治疗有反应,但后来因疾病进展死亡。该队列包括71个不同的转移性肿瘤,41个代表器官特异性肿瘤宏观环境的肿瘤相邻“正常”(AN)组织和38个肿瘤非相邻正常(NAN)组织。研究者分析了来自肿瘤和患者匹配NAN的WES以及来自子集的WGS。为了剖析不同疗法的贡献,比较分析了来自仅接受MAPKi或仅接受ICB治疗进展的CM患者的纵向肿瘤前和肿瘤后的WES数据。此外,研究者开发了基于肿瘤细胞富集的转录组的器官特异性转移特征,并分析了肿瘤和AN组织之间的配体-受体信号传导。最后对肿瘤、AN和NAN转录组进行去卷积,以破译器官特异性免疫结构。
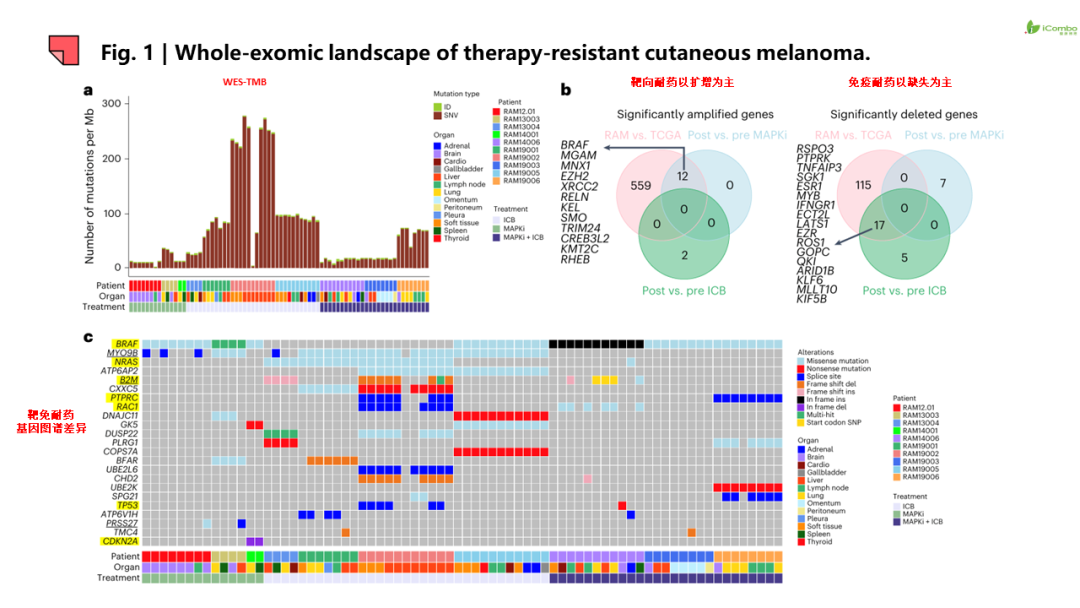
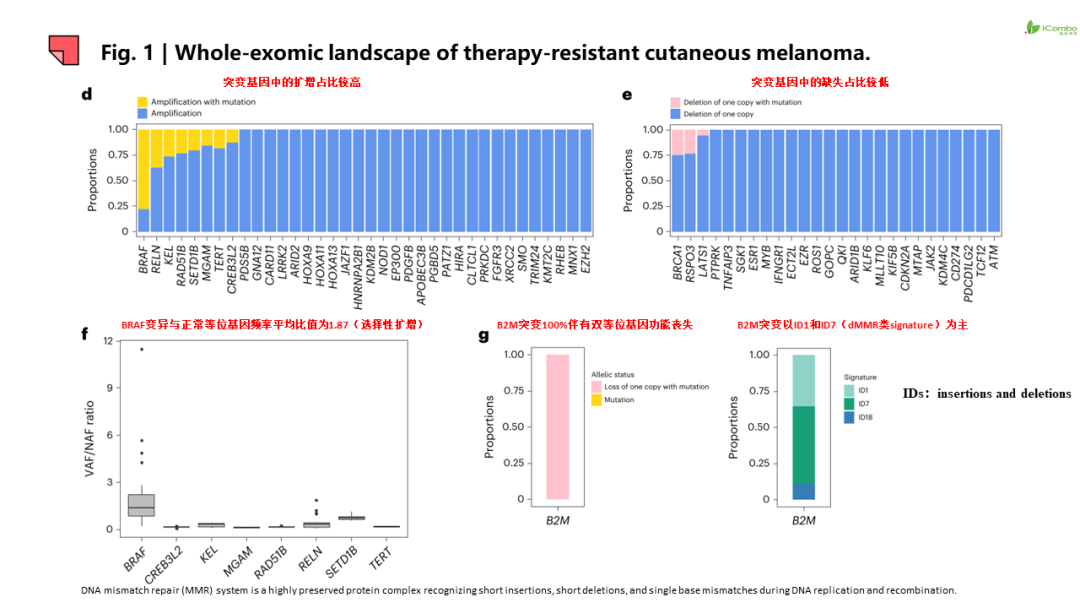
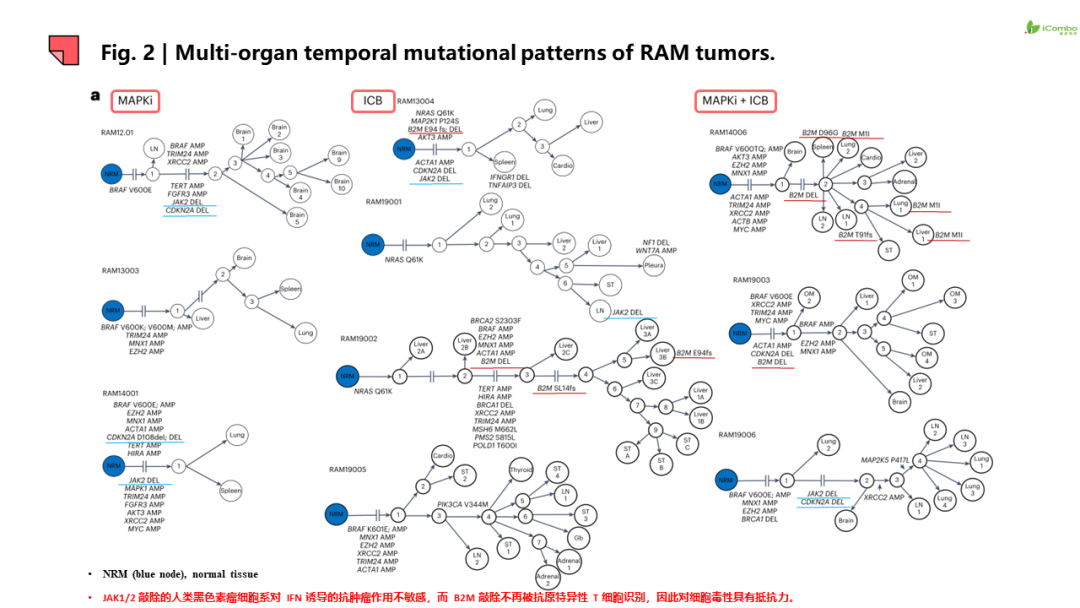
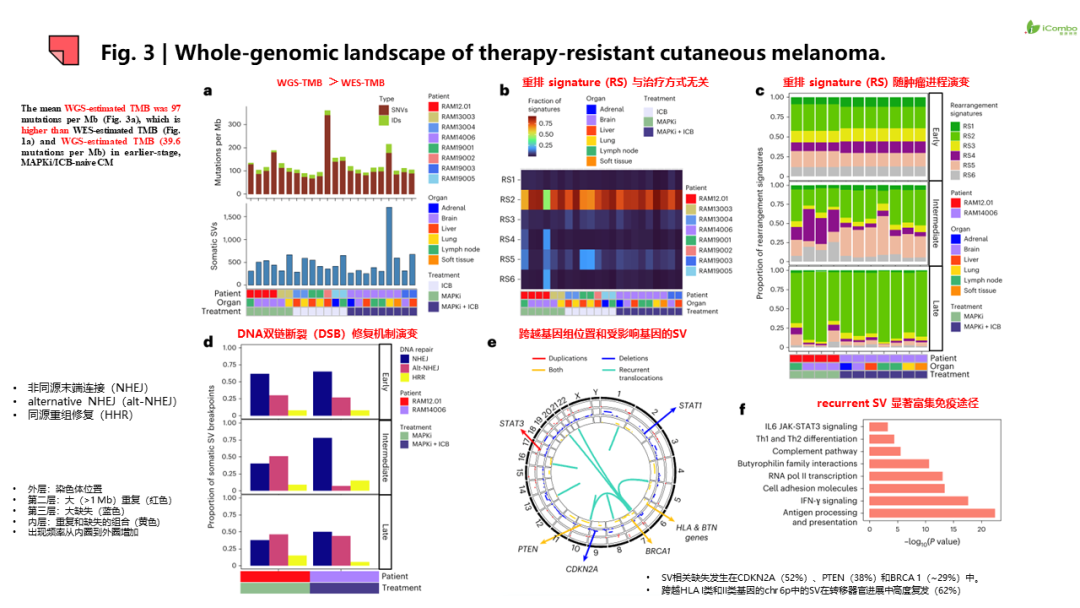
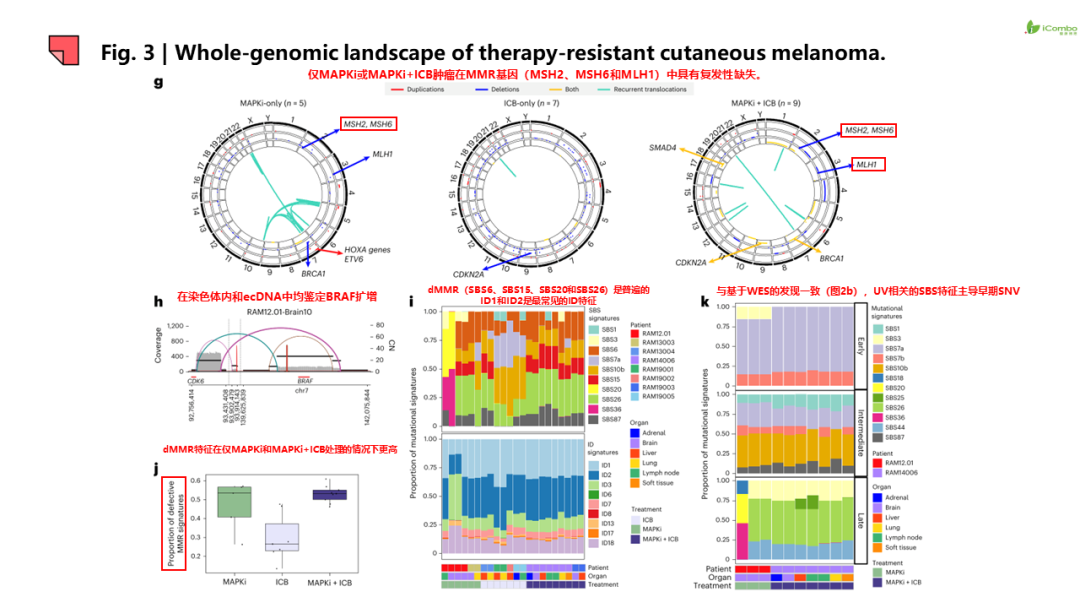
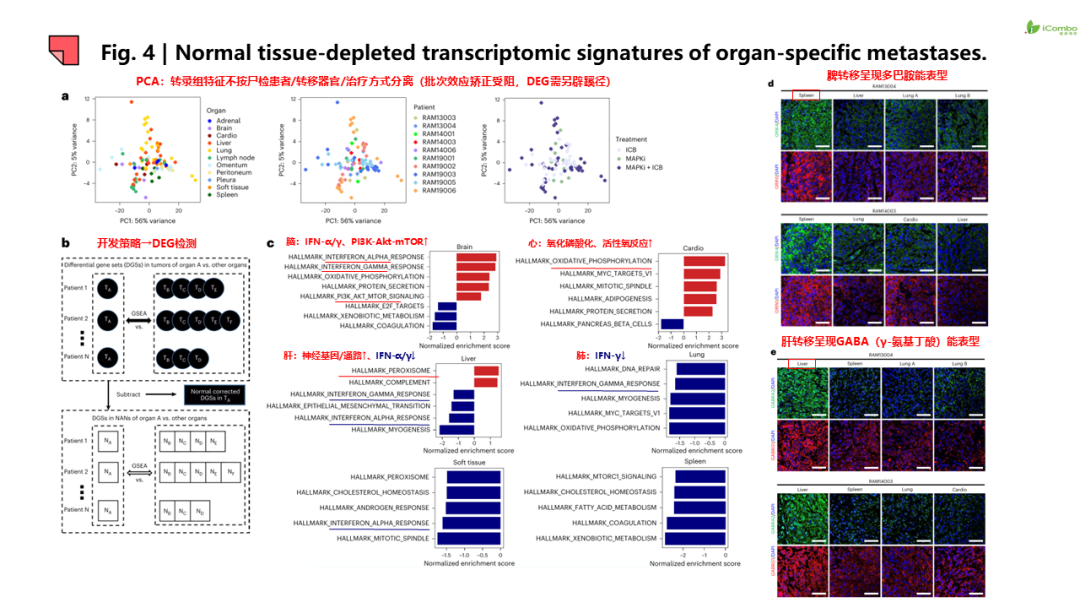
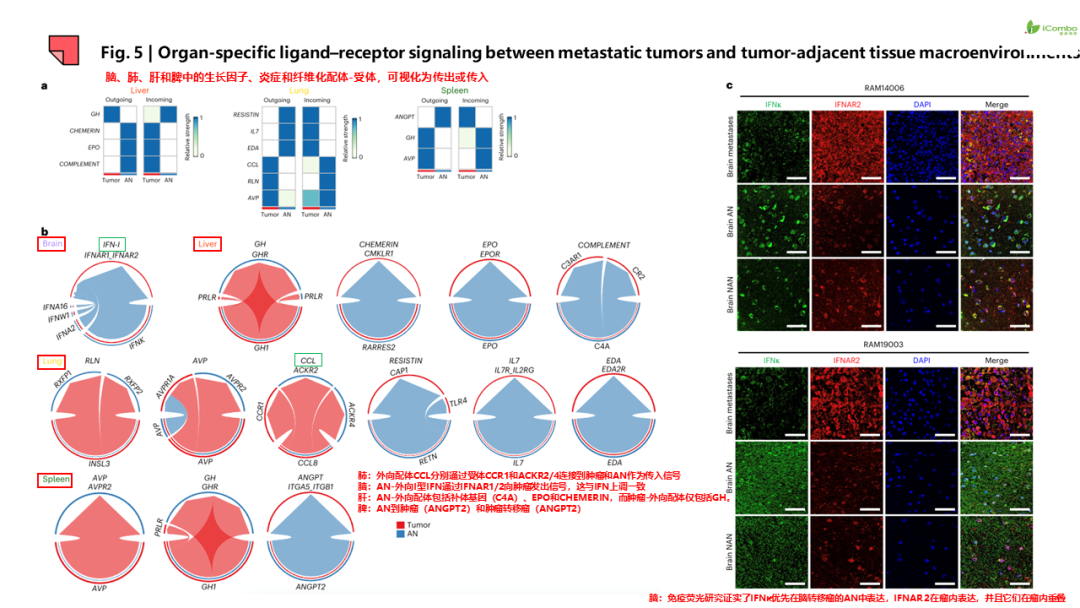
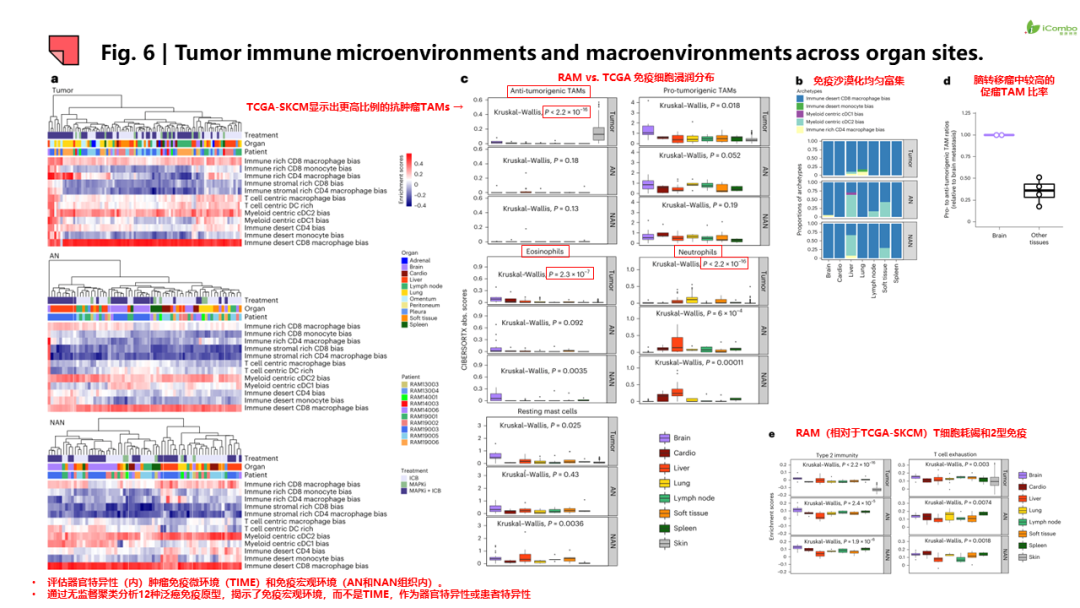
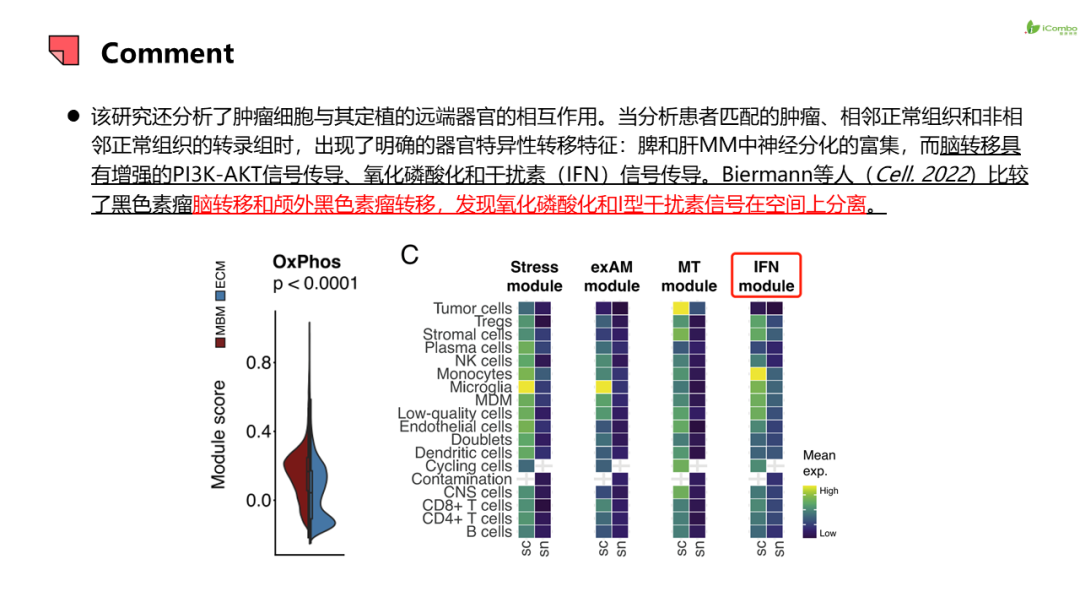
研究结果提示:1.除JAK2和B2M功能丧失和BRAF基因扩增导致ICB或MAPKi耐药外,非同源重组修复机制缺陷也参与ICB或MAPKi耐药。 2.耐药病灶信号特征呈现器官特异性,如脾和肝转移灶中富集神经分化信号,而脑转移灶PI3K-AKT信号传导、氧化磷酸化和干扰素(IFN)信号增强, 脑转移灶表现为“冷肿瘤”,但富集耗竭的CD8+T细胞和巨噬细胞。此外,在转移灶和瘤周正常组织检测到器官特异性配体-受体对。例如,肺转移检测到CCR1配体-受体信号对, 脑转移出现IFNAR1/2信号对等。
本研究中产生的基因特征可以应用于许多其他快速尸检队列和正在进行的临床试验,从而调整数据处理技术,建立一个位点特异性的黑色素瘤转移平台,还可以预测药物反应和器官微环境对治疗的影响,促进临床医生和基础科学研究人员之间的合作(Nat Med. 2023 May;29(5):1123-1134. doi: 10.1038/s41591-023-02304-9)。





本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#黑色素瘤# #MAPK抑制剂# #尸检黑色素瘤#
63