Lancet 子刊:高危淋巴瘤患者的CD30 CAR-T巩固治疗
2024-05-24 儿童肿瘤前沿 儿童肿瘤前沿 发表于上海
这项临床研究的目的是确定作为高复发风险CD30阳性淋巴瘤患者,在自体造血干细胞移植 (HSCT) 后输入抗 CD30 CAR T 细胞作为巩固治疗的安全性。
尽管大多数患有典型霍奇金淋巴瘤的患者经一线治疗都有治愈的可能,但约10-25%的患者属于难治愈型或初始完全缓解后复发。霍奇金淋巴瘤患者的护理标准是第一次复发后进行高剂量化疗,然后进行自体造血干细胞移植(HSCT),用这种方法大约一半接受治疗的患者有治愈可能。最近自体造血干细胞移植后,采用布伦妥昔单抗维多汀(一种CD30抗体偶联物)维持治疗增加了高风险特征患者的无进展生存期, 但存在与治疗相关的毒性,例如神经病变和中性粒细胞减少症。
近日,北卡罗来纳大学莱恩伯格综合癌症中心团队在 The Lancet Haematology 上发表题为Anti-CD30 CAR T cells as consolidation after autologous haematopoietic stem-cell transplantation in patients with high-risk CD30+ lymphoma: a phase 1 study 的文章,基于CD30 CAR-T细胞在CD30阳性淋巴瘤中的高安全性和有希望的活性开展了1期临床试验,这项临床研究的目的是确定作为高复发风险CD30阳性淋巴瘤患者,在自体造血干细胞移植 (HSCT) 后输入抗 CD30 CAR T 细胞作为巩固治疗的安全性。

这项1期剂量递增研究在美国的两个地点进行。年龄3岁及以上、患有典型霍奇金淋巴瘤或非霍奇金淋巴瘤但免疫组织化学显示CD30阳性疾病,且卡诺夫斯基(Karnofsky )评分超过 60%, 计划进行自体造血干细胞移植的患者。如果被认为具有复发高风险,例如原发性难治性疾病或初始治疗后 12个月内复发或移植前挽救治疗开始时,淋巴结外已有癌细胞,则符合进行自体造血干细胞移植的资格。这项临床主要终点是确定最大耐受剂量,该剂量基于接受CAR T细胞输注的患者的剂量限制性毒性发生率。本临床已在ClinicalTrials.gov注册 (NCT02663297),入组工作已完成。
NCT02663297临床研究结果
2016年6月7日至2020年11月30日期间,入组了21名患者,其中18名患者(11名患有霍奇金淋巴瘤,6 名患有T细胞淋巴瘤,1 名患有灰区淋巴瘤),中位数为自体造血干细胞移植后22天(范围 16-44天)输入了抗CD30 CAR T细胞 (3种剂量),没有观察到剂量限制性毒性,因此每平方米2×10⁸ CAR T细胞被确定为最大耐受剂量。一名患者的病情为1级细胞因子释放综合征;最常见的3-4级不良事件是淋巴细胞减少(18例中有2例,11%)和白细胞减少症(18例中的2例,11%;没有出现与治疗相关的死亡;两名患者在治疗后约2年到2.5年出现继发性恶性肿瘤(一名4期非小细胞肺癌和一名睾丸癌症),但这些癌症被诊断与CAR T治疗无关。
输注后中位随访48.2个月 (四分位数范围27.5–60.7)。所有治疗患者 (n=18) 的中位无进展生存期为32.3个月;接受治疗的霍奇金淋巴瘤患者 (n=11) 的中位无进展生存期没有达到;所有接受治疗的患者的中位总生存期尚未达到, 临床流程如图所示:
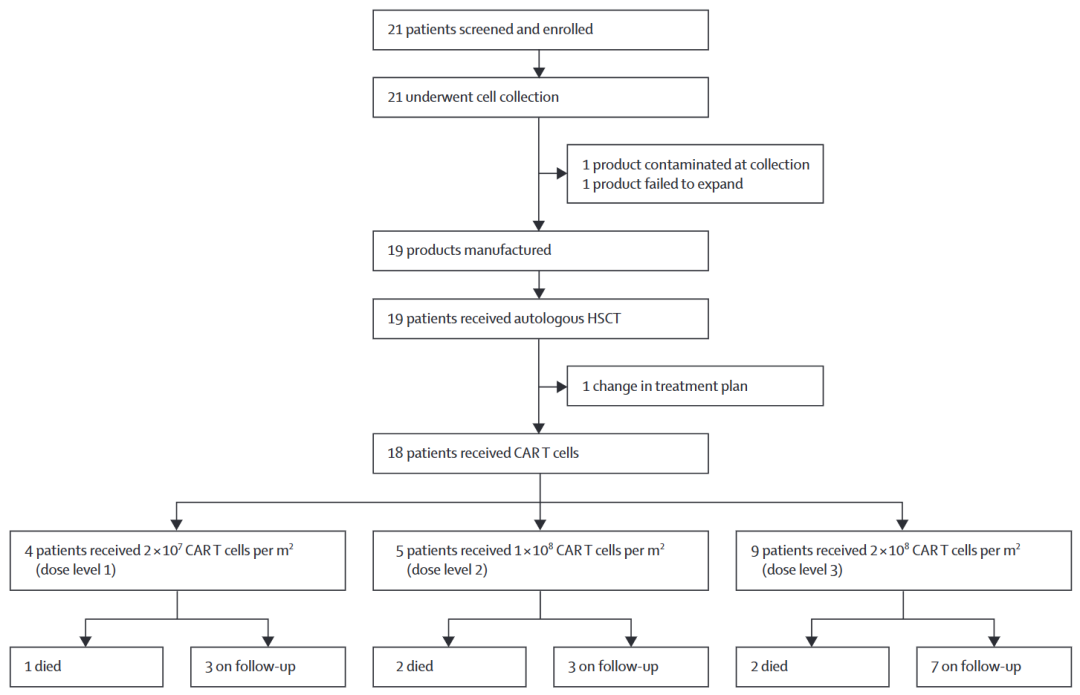
临床结果显示,高剂量化疗和自体造血干细胞移植后,输注抗CD30 CAR T细胞是安全的,因为抗CD30 CAR T细胞并没有出现像其他CAR T细胞疗法的副作用, 例如减小干细胞移植的长期效果或导致长期血细胞减少,并且不会引起高细胞因子释放综合征或其它神经系统毒性。
虽然很难比较不同临床试验的结果,但NCT02663297临床结果优于其它临床试验的地方在于,自体造血干细胞移植后只需单次输注抗CD30 CAR T细胞,相对毒性较小和减小对布伦妥昔单抗维多汀的依赖性,这对于青少年和青壮年人群尤其重要。以往自体移植后,需要使用多周期布伦妥昔单抗维多汀来维持疗效,这对于许多患者来说,具有很大的挑战。例如AETHERA试验中约三分之一的患者由于毒性累积,特别是周围神经病变等原因中止了治疗,在现实世界中的停药率甚至更高。
目前自体造血干细胞移植后采用布伦妥昔单抗维多汀和检查点抑制剂(如PD-1)维持已成为早期疗法, 且HSCT后2年无进展生存率为93% ,这项临床试验也达到了这一结果, 而且为在自体移植前未接受过PD-1抑制剂治疗的患者提供了选择。另外,这一临床试验还招募了六位CD30显性的其他淋巴瘤的患者,不幸的是有五名病情复发,说明抗CD30 CAR T细胞维护疗法并没有克服T细胞淋巴瘤患者不良的预后结果。
这项临床试验局限性在于样本量小和异质的患者群体小,而且治疗前后的活检样本少,不足以评估CD30表达和其他特征, 需要强调的是大多数入组患者能够安全地接受抗CD30 CAR T细胞,证明了这一疗法的可行性,下一临床应该评估这种方法的有效性。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#淋巴瘤# #CAR-T#
69