iPS干细胞治疗糖尿病,竟导致患者出现肿瘤?
2022-07-18 生物世界 生物世界
在 iPSC 来源的β细胞治疗糖尿病后,应更加关注畸胎瘤的形成,因为形成的未成熟畸胎瘤比典型的成熟畸胎瘤更具侵袭性。应在标准临床试验中进一步探索 iPSC 来源细胞治疗糖尿病的安全性和有效性。
2006年,日本京都大学山中伸弥教授在 Cell 期刊发表论文,发现将 Oct3/4、Sox2、Klf4、c-Myc 这四种转录因子通过病毒载体导入成熟体细胞后,可将体细胞转化为诱导多能干细胞(iPSC)。山中伸弥因此获得了2012年诺贝尔生理学或医学奖,也开启了 iPSC 治疗的新时代。
近年来,基于 iPSC 的 CAR-T、CAR-NK 细胞疗法,以及再生医学和抗衰老研究如火如荼。然而,诱导的 iPSC 可能存在细胞过度生长和癌变风险,因此具有潜在致癌性。早在2009年,山中伸弥就曾在 Nature Biotechnology 期刊发表论文,显示胚胎成纤维细胞来源的 iPS 神经干细胞植入小鼠后,具有较高的成瘤风险。
近日,Stem Cells and Development 期刊发表了一篇题为:Distinctive Clinical and Pathologic Features of Immature Teratomas Arising from Induced Pluripotent Stem Cell-Derived Beta Cell Injection in a Diabetes Patient 的论文。
尽管目前有许多基于 iPSC 的细胞疗法的临床试验,但仍不清楚是否会在患者中发生真正的肿瘤。这篇论文报告了第一例 iPSC 来源细胞治疗2型糖尿病后形成未成熟畸胎瘤的临床病例。
与成熟畸胎瘤不同,未成熟畸胎瘤具有复发和转移的潜力,论文作者强调,在使用 iPSC 细胞治疗时,应当更加关注畸胎瘤的形成,并进一步探索治疗的安全性和有效性。

糖尿病是一种以高血糖、胰岛素抵抗和血糖调节缺陷为特征的代谢性疾病,可损害各种器官功能。据WHO预测,到2030年,全球糖尿病患者人数将翻一番,造成严重的社会经济负担。2型糖尿病(T2DM)占所有糖尿病病例的85%-95%,其特征是胰岛素抵抗和胰腺β细胞的胰岛素分泌受损,多数患者需要终生接受胰岛素注射来控制血糖,这常导致不可逆胰腺β细胞损伤并引起严重并发症。
近年来,越来越多的研究开始聚焦于使用人诱导多能干细胞(hiPSC)来源的β细胞来治疗胰岛中不可逆的β细胞损伤,并被认为是治愈糖尿病的有潜力的方法。
然而,iPSC 的致瘤性一定程度上阻碍了其临床应用,在体外和体内 iPSC 实验模型中,已检测到其存在广泛的基因组不稳定性,包括染色体畸变、拷贝数变异和单核苷酸变异等,小鼠模型实验也观察到了存在致瘤性,此外,还有少数临床试验病例报道了 iPSC 来源的细胞在移植后形成肿瘤或肿瘤样病变。但目前还没有 iPSC 治疗2型糖尿病后导致患者出现肿瘤的病例报道。
这篇论文报道了一例2型糖尿病患者在接受 iPSC 来源细胞治疗后形成未成熟畸胎瘤的病例。
该2型糖尿病患者接受移植的β细胞是由自体 iPSC 分化而来,2020年6月,该患者在北京的某家医院接受了自体 iPSC 来源的β细胞的注射,病历显示,该患者血液中分离的体细胞被重编程为 iPSC,然后再分化为胰岛β细胞,在扩增后通过左上臂的三角肌注射到患者体内。到治疗后2个月,患者的血糖调节和胰岛素水平并没有改善,反而在注射位置出现肿块以及腋窝淋巴结肿大。
此后,这名患者来到了云南省肿瘤医院接受了治疗(该患者的iPSC治疗并非在云南省肿瘤医院进行)。
磁共振成像(MRI)扫描提示,该肿瘤为良性或中间性肿瘤。2020年8月,患者接受了肿瘤切除手术,病理诊断显示是未成熟畸胎瘤。PET-CT 检查显示存在同侧腋窝和颈部淋巴结转移。经过两个周期的常规化疗后,患者的肿瘤出现进展。此后患者接受了颈部和腋窝手术区的辅助放疗,并结合化疗。到2021年10月,PET-CT 显示患者没有出现肿瘤复发或远端转移。
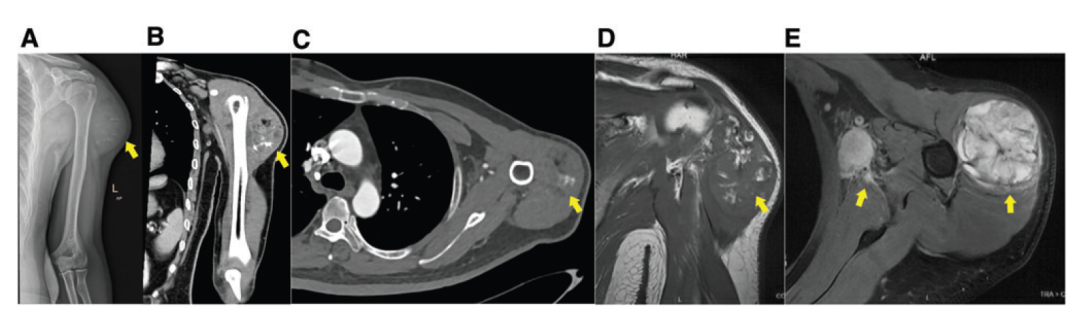
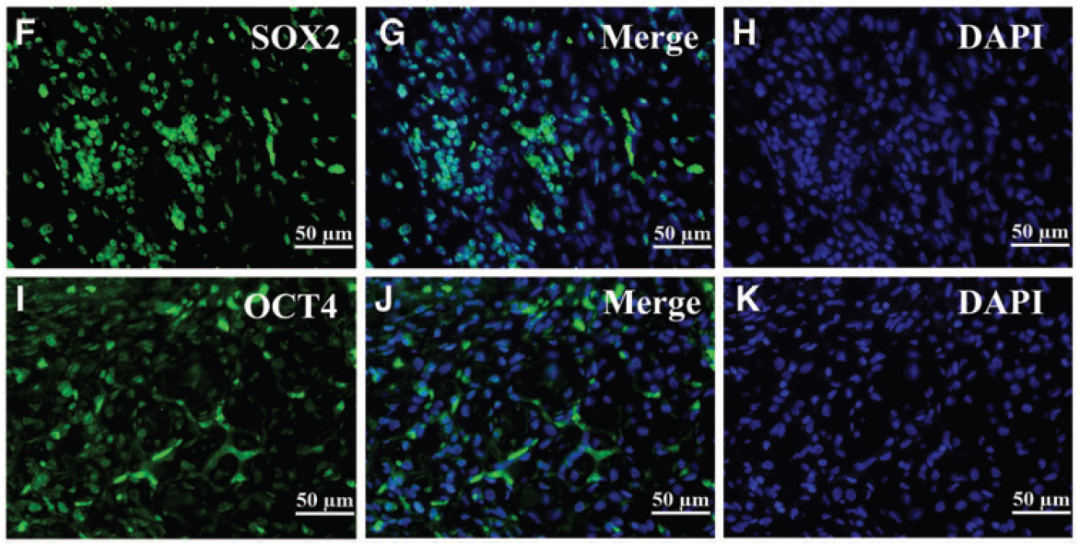
为了确定畸胎瘤中是否存在胰岛β细胞,通过免疫荧光测定检测诱导的 iPSC 的关键标志物 OCT4 和 SOX2 基因表达,二者在细胞核或细胞质中均呈阳性。然而,对肿瘤细胞中胰岛素的免疫组织化学染色呈阴性。
OCT4 和 SOX2 阳性,表明注射后的细胞并未完全分化。而胰岛素阴性表明这些细胞没有产生胰岛素分泌功能,这说明 iPSC 在体外诱导的状态不代表在体内植入后的状态。
对患者的肿瘤组织进行的高通量测序显示,患者肿瘤细胞中存在 ABCB4、CDC73、CROT、DNMT3A、HCK、KMT2D、MSH2、MSH6、NCOR2、PRDM1、PREX2、RPS6KB2、TRAF7、ZFHX3、ZNF703 和 ZRSR2 这16个基因的错义或移码突变。
iPSC 来源的细胞疗法已经在临床试验中显示了对癌症、神经图形学疾病以及糖尿病的疗效。与其他干细胞疗法相比,iPSC 细胞具有更易获取、扩增迅速、免疫原性低、无伦理问题等显著优势。然而,基于 iPSC 的细胞治疗具有致瘤性的潜在风险,这是其在推广到临床过程中面临的一大障碍。
越来越多的证据表明,iPSC 的重编程会带来潜在致瘤性风险,例如病毒载体带来的基因插入、转录因子的长期过表达等等。
2022年4月,Altos Labs 公司在 Nature Aging 发表的一项研究显示【2】,通过瞬时表达重编程因子(Oct4、Sox2、Klf4 和 c-Myc)对衰老小鼠进行体内重编程,恢复了衰老细胞的年轻表观遗传特征,并延长了早衰小鼠模型寿命。这提示了我们,瞬时诱导方案效果良好,且没有观察到致瘤性等潜在副作用。
最后,论文作者总结道,在 iPSC 来源的β细胞治疗糖尿病后,应更加关注畸胎瘤的形成,因为形成的未成熟畸胎瘤比典型的成熟畸胎瘤更具侵袭性。应在标准临床试验中进一步探索 iPSC 来源细胞治疗糖尿病的安全性和有效性。
论文链接:
1.https://www.liebertpub.com/doi/10.1089/scd.2021.0255
2.https://www.nature.com/articles/s43587-022-00183-2
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#iPS#
79