南通大学Nano Letters:双响应仿生纳米材料的声动力学和铜死亡作用可在癌症治疗中实现精确的线粒体干预
2024-06-22 BioMed科技 BioMed科技 发表于上海
该研究开创了一种精确的声动力学铜死亡的仿生方法,有望彻底改变癌症治疗。
声动力疗法(SDT)与铜死亡联合用于癌症靶向治疗是肿瘤学的一个重大进展。在此,南通大学Binyi Li等人提出了一种双响应治疗系统“CytoNano”,它结合了与氮化铜纳米颗粒和富氧全氟碳融合的阳离子脂质体(Lip@Cu3N/PFC-O2),这些成分全部包裹在中性粒细胞膜和酸响应性羧甲基纤维素的仿生涂层中。CytoNano利用中性粒细胞和酸响应材料的模拟细胞性质,实现肿瘤及其酸性微环境的精确靶向,增强Lip@Cu3N/PFC-O2的癌症细胞摄取和线粒体定位。因此,它在保护健康组织的同时,增强了Cu3N驱动的SDT和铜死亡的治疗效果。此外,CytoNano的超声响应性增强了肿瘤内的氧合,克服了生理障碍,并启动了声动力学-铜死亡的联合效应,诱导多种细胞死亡途径。因此,该研究开创了一种精确的声动力学铜死亡的仿生方法,有望彻底改变癌症治疗。相关工作以“The Convergence of Sonodynamic Therapy and Cuproptosis in the Dual-Responsive Biomimetic CytoNano for Precision Mitochondrial Intervention in Cancer Treatment”为题发表在Nano Letters。

【文章要点】
为了充分利用SDT和铜死亡结合的协同潜力,精确靶向癌症细胞内的特定细胞器,尤其是线粒体至关重要。SDT和铜死亡都会显著影响线粒体功能,使这些细胞器成为治疗干预的主要靶点。具体而言,铜死亡与线粒体呼吸和硫辛酸途径密切相关,硫辛酸途径导致氧化应激的启动,最终导致细胞死亡。同时,SDT对超声刺激响应产生ROS,进一步诱导氧化应激。SDT和铜死亡在线粒体紊乱方面的趋同突出了线粒体靶向递送策略提高治疗效果的潜力。为此,作者提出了一种名为CytoNano的双响应仿生纳米复合材料系统。该系统包括中性粒细胞膜和羧甲基纤维素(CMCS)外层,能够包封阳离子脂质体,而该脂质体融合有氮化铜纳米颗粒和富氧全氟化碳(Lip@Cu3N/PFC-O2)(图1)。
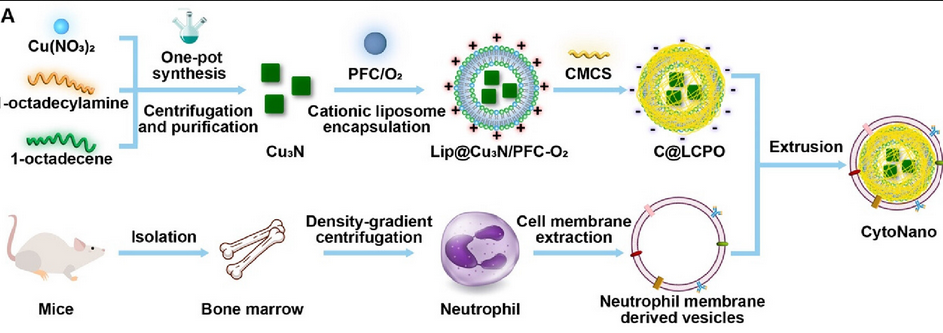
图1 CytoNano的设计和合成
CytoNano巧妙地将中性粒细胞的细胞特性与CMCS的酸响应特性相结合,增强了系统循环、肿瘤靶向性和细胞内递送功效。更重要的是,阳离子纳米复合物的正电荷促进其在带负电荷的线粒体膜上的积累,优化线粒体定位。掺入的Cu3N作为一种多功能治疗剂,同时诱导铜死亡和激活SDT。此外,PFC-O2成分有效缓解肿瘤缺氧,从而提高铜死亡和SDT的治疗效果,显著提高整体治疗效果(图2)。
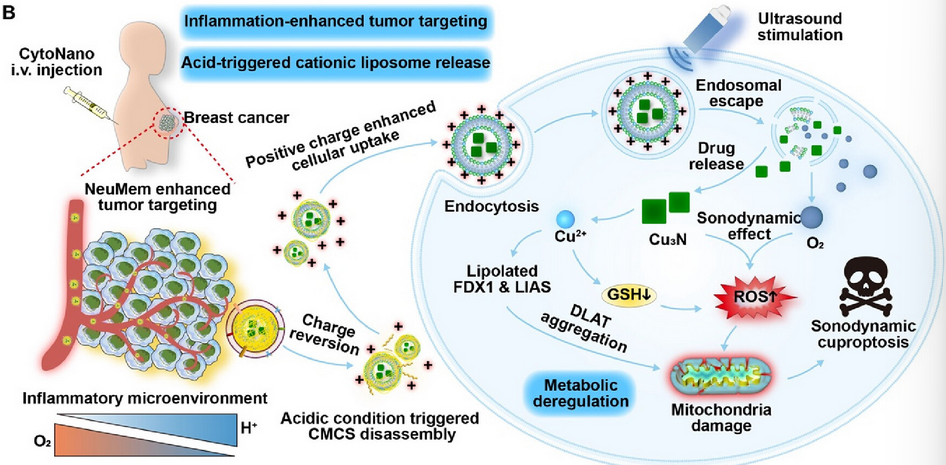
图2 由声动力学铜死亡触发的协同抗癌机制
原文链接:
https://pubs.acs.org/doi/10.1021/acs.nanolett.4c01864
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#癌症治疗# #铜死亡# #声动力疗法#
53