Science:生命中心施一公研究组报道酵母剪接体催化第二步剪接反应激活状态的三维结构
2016-12-17 生命科学联合中心 生命科学联合中心
2016年12月16日,生命中心施一公研究组于《科学》(Science)杂志就剪接体的结构与机理研究再发长文(Research Article),题为《酵母剪接体处于第二步催化激活状态下的结构》(Structure of a Yeast Step II Catalytically Activated Spliceosome),报道了酿酒酵母(Saccharomyces cerevisiae)剪
2016年12月16日,生命中心施一公研究组于《科学》(Science)杂志就剪接体的结构与机理研究再发长文(Research Article),题为《酵母剪接体处于第二步催化激活状态下的结构》(Structure of a Yeast Step II Catalytically Activated Spliceosome),报道了酿酒酵母(Saccharomyces cerevisiae)剪接体在即将开始第二步剪接反应前的工作状态下的三维结构,阐明了剪接体在第一步剪接反应完成后通过构象变化起始第二步反应的激活机制,从而进一步揭示了前体信使RNA剪接反应(pre-mRNA splicing,以下简称RNA剪接)的分子机理。这是继上半年发文后进一步研究的结果(上半年文章见:施一公在《科学》同一期发表两篇论文,这是第二次!)
由于真核生物中的基因编码区中存在不翻译成蛋白质的序列(称为内含子),染色体DNA转录出来的前体mRNA(pre-mRNA)并不直接参与蛋白质翻译,而是需要先将其中的内含子片段去除,才能进入核糖体进行蛋白质合成。内含子的去除需要通过两步转酯反应来实现:首先,位于内含子序列中下游被称为分支点(branch point sequence)的序列中有一个高度保守的腺嘌呤核苷酸(A),其2’羟基亲核攻击内含子5’末端的鸟嘌呤(G),于是第一步反应发生,形成套索结构;然后,5’外显子末端暴露出的3’-OH向内含子3’末端的鸟嘌呤发起攻击,第二步反应发生,两个外显子连在一起。通过这两步反应,前体信使RNA中数量、长度不等的内含子被剔除,剩下的外显子按照特异顺序连接起来从而形成成熟的信使RNA(mRNA)(图1)。
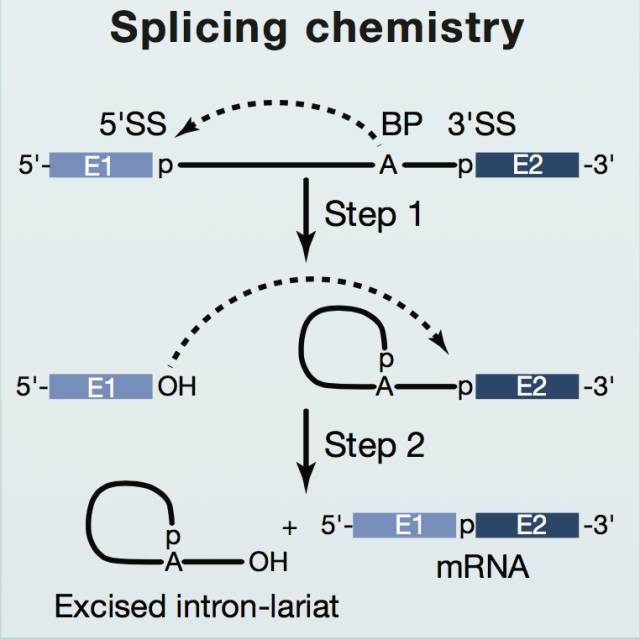
图1 基因剪接反应示意图(图片来源:《Cell》)
这两步化学反应在细胞内是由一个庞大、复杂而动态的分子机器——剪接体催化完成的。对于每一个内含子来说,为了调控反应的各个基团在适当时机呈现合适的构象从而发挥其活性,剪接体各组分按照高度精确的顺序结合和解离,组装成一系列具有不同构象的分子机器,统称为剪接体。根据它们在RNA剪接过程中的生化性质,这些剪接体又被区分为B、Bact、B*、C、P、ILS等若干状态。获取剪接体在组装、激活、催化反应过程中各个状态的结构是最基础也是最富挑战性的结构生物学难题之一。

图2 C* complex三维结构示意图
原始出处:
相关论文链接:
Chuangye Yan,Yigong Sh,et al. Structure of a yeast spliceosome at 3.6-angstrom resolution. Science. 20 Aug 2015.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#第二步剪接反应#
44
#三维结构#
55
#剪接体#
52
#SCIE#
62
#应激#
59
期望下一个中国诺贝尔奖!
80
一公就是不得了
80