JARG:有一就有二?全球第二例人类胚胎基因编辑现身中国
2016-12-29 生物探索 生物探索
导读 最近,中国科研人员发表了一项有关人类胚胎基因编辑方面的研究,让全球科学家的神经再一次被挑动。该研究由广州医科大学附属第三医院范勇领导的研究团队完成。虽然论文发表在一般人不熟悉、影响因子不超过2的学术杂志——《辅助生殖与遗传学期刊》上,但却引来国际顶级学术期刊以及媒体的关注。最近,中国科研人员发表了一项有关人类胚胎基因编辑方面的研究,让全球科学家的神经再一次被挑动。该研究由广州医科大学附属
导读 最近,中国科研人员发表了一项有关人类胚胎基因编辑方面的研究,让全球科学家的神经再一次被挑动。该研究由广州医科大学附属第三医院范勇领导的研究团队完成。虽然论文发表在一般人不熟悉、影响因子不超过2的学术杂志——《辅助生殖与遗传学期刊》上,但却引来国际顶级学术期刊以及媒体的关注。
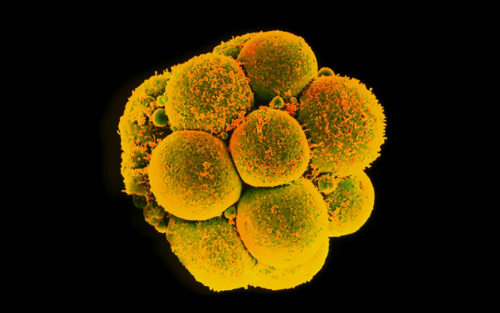
最近,中国科研人员发表了一项有关人类胚胎基因编辑方面的研究,让全球科学家的神经再一次被挑动。该研究由广州医科大学附属第三医院范勇领导的研究团队完成。虽然论文发表在一般人不熟悉、影响因子不超过2的学术杂志——《辅助生殖与遗传学期刊》(Journal of Assisted Reproduction and Genetics)上,但却引来国际顶级学术期刊以及媒体的关注,如Nature、Science、MIT Technology Review等。

发表在《辅助生殖与遗传学期刊》的论文截图
人类胚胎基因编辑再现,存在诸多技术瓶颈
根据研究者介绍,他们进行此项研究的目的是对CRISPR技术在早期人类胚胎的精准基因编辑方面的应用进行评估并制定原则,从而为未来遗传性疾病的治疗提供了可能。

广州医科大学附属第三医院研究员 范勇
从2014年4月至9月,研究者从87名志愿者那里收集了213枚三原核受精卵,即原本不能正常发育的人类胚胎细胞。研究者通过基因编辑技术CRISPR,对这些受精卵中的基因ccr5进行编辑,结果发现26个人体胚胎细胞中,仅有4个细胞的基因成功被修饰,基因编辑的脱靶问题突出,表明该技术存在大量瓶颈。此次实验的所有胚胎在三天后均被销毁。研究者之所以选择该基因,是因为部分人群如果携带有ccr5突变基因,那么他们则拥有抵抗HIV病毒的能力,该突变基因能改变CCR5蛋白,使其能够阻止HIV病毒对人体免疫细胞的入侵。
如同去年中山大学出现的全球首个人类胚胎细胞基因修饰的研究一样,这项研究一经发表,就引起Nature等权威学术杂志的关注。只不过经历了去年一年的激烈讨论之后,研究者以及公众现在更加理性地看待此类研究。

人类胚胎基因编辑再现,存在诸多技术瓶颈
根据研究者介绍,他们进行此项研究的目的是对CRISPR技术在早期人类胚胎的精准基因编辑方面的应用进行评估并制定原则,从而为未来遗传性疾病的治疗提供了可能。

广州医科大学附属第三医院研究员 范勇
从2014年4月至9月,研究者从87名志愿者那里收集了213枚三原核受精卵,即原本不能正常发育的人类胚胎细胞。研究者通过基因编辑技术CRISPR,对这些受精卵中的基因ccr5进行编辑,结果发现26个人体胚胎细胞中,仅有4个细胞的基因成功被修饰,基因编辑的脱靶问题突出,表明该技术存在大量瓶颈。此次实验的所有胚胎在三天后均被销毁。研究者之所以选择该基因,是因为部分人群如果携带有ccr5突变基因,那么他们则拥有抵抗HIV病毒的能力,该突变基因能改变CCR5蛋白,使其能够阻止HIV病毒对人体免疫细胞的入侵。
如同去年中山大学出现的全球首个人类胚胎细胞基因修饰的研究一样,这项研究一经发表,就引起Nature等权威学术杂志的关注。只不过经历了去年一年的激烈讨论之后,研究者以及公众现在更加理性地看待此类研究。

平日爱八卦的英国媒体《每日邮报》严肃了一回,同样也关注此项研究,截图自Daily Mail
中外同行学者的评价
来自波士顿儿童医院的George Daley表示,这项研究推动了CRISPR技术未来对人类细胞精准编辑的应用,但并未提供太多的证据,此前已有研究者对这方面论证过。CRISPR技术成为潜在的具有应用价值的技术,仍需很长的一段时间。
来自埃默里大学的神经生物学家Xiao-Jiang Li认为,这项研究强调,“我们对细胞的精准编辑仍存在大量的技术瓶颈。事实上,此类实验可先在非人灵长类动物身上进行,然后再来对人类细胞进行有效的编辑。”
《知识分子》也在第一时间联系了国内这一领域权威学者。一位不愿透露姓名的学者认为,去年中山大学的人类胚胎基因修饰研究,得到了国际权威的认可,但后续的类似工作,意义不大。“我不大主张编辑人类胚胎,除非在技术上或者科学上有很大进步,如果是完全可预见的结果,其实意义不大了。”
此外,前述学者认为,这项研究“选择的基因也有问题,即便是最后的基因编辑能用于人类,也没有必要选一个可能感染疾病的靶点来进行操作。因为目前尚没有中国人的数据,证明ccr基因突变不会影响健康。即便是欧洲有此突变的人群,也很难说哪方面会不会受到了影响。”
另外一位研究者向《知识分子》表示,这篇文章的意义有限,未对疾病治疗、预防以及药物的研发有直接作用,这可能是其不能发表在主流期刊的原因。但文章比较吸引眼球。
基因编辑技术的伦理讨论
2015年4月,中山大学学者黄军就发表在《蛋白质与细胞》(Protein and Cell)上的人类胚胎基因修饰研究,引发全球科学同行以及公众的激烈讨论。该研究亦成为当年12月份在华盛顿召开的“国际人类基因编辑大会”(International Summit on Human Gene Editing)的导火索之一。黄军就也因该项研究入选Nature杂志2015年十大科学人物。
此次大会汇集了来自美国、欧洲、日韩以及中国这一领域的权威学者。会议达成了一个共识:On Human Gene Editing: International Summit Statement,阐述了目前基因编辑技术的基础研究与未来的可能应用,并划清伦理禁区。大会达成一个共识:当前利用CRISPR技术对人类胚胎细胞基因进行修饰,是“不负责任”(irresponsible)的举动。虽然该共识不具备法律效应,但它对目前这一领域的科学家形成强而有力的约束。
令人感到忧虑的是,人类胚胎细胞基因编辑或许不会是目前仅有的两项研究。根据Nature的报道,很多科学家已经将类似的研究论文投递出去,广州医科大学的这篇文章只不过是它们其中的一篇而已。
尽管中国科学院是去年人类基因编辑大会的三方组织者之一,积极参与推动基因编辑伦理规范的讨论以及制定,但是中国更多的正在进行的有关人类生殖细胞基因编辑研究工作尚没有明确的伦理规范。显然,相关的研究工作不仅考验着人类的伦理底线,同时从某种程度上说,不规范的研究活动也会使得其他学者正常利用基因编辑技术进行研究或应用受到阻碍。
中外同行学者的评价
来自波士顿儿童医院的George Daley表示,这项研究推动了CRISPR技术未来对人类细胞精准编辑的应用,但并未提供太多的证据,此前已有研究者对这方面论证过。CRISPR技术成为潜在的具有应用价值的技术,仍需很长的一段时间。
来自埃默里大学的神经生物学家Xiao-Jiang Li认为,这项研究强调,“我们对细胞的精准编辑仍存在大量的技术瓶颈。事实上,此类实验可先在非人灵长类动物身上进行,然后再来对人类细胞进行有效的编辑。”
《知识分子》也在第一时间联系了国内这一领域权威学者。一位不愿透露姓名的学者认为,去年中山大学的人类胚胎基因修饰研究,得到了国际权威的认可,但后续的类似工作,意义不大。“我不大主张编辑人类胚胎,除非在技术上或者科学上有很大进步,如果是完全可预见的结果,其实意义不大了。”
此外,前述学者认为,这项研究“选择的基因也有问题,即便是最后的基因编辑能用于人类,也没有必要选一个可能感染疾病的靶点来进行操作。因为目前尚没有中国人的数据,证明ccr基因突变不会影响健康。即便是欧洲有此突变的人群,也很难说哪方面会不会受到了影响。”
另外一位研究者向《知识分子》表示,这篇文章的意义有限,未对疾病治疗、预防以及药物的研发有直接作用,这可能是其不能发表在主流期刊的原因。但文章比较吸引眼球。
基因编辑技术的伦理讨论
2015年4月,中山大学学者黄军就发表在《蛋白质与细胞》(Protein and Cell)上的人类胚胎基因修饰研究,引发全球科学同行以及公众的激烈讨论。该研究亦成为当年12月份在华盛顿召开的“国际人类基因编辑大会”(International Summit on Human Gene Editing)的导火索之一。黄军就也因该项研究入选Nature杂志2015年十大科学人物。
此次大会汇集了来自美国、欧洲、日韩以及中国这一领域的权威学者。会议达成了一个共识:On Human Gene Editing: International Summit Statement,阐述了目前基因编辑技术的基础研究与未来的可能应用,并划清伦理禁区。大会达成一个共识:当前利用CRISPR技术对人类胚胎细胞基因进行修饰,是“不负责任”(irresponsible)的举动。虽然该共识不具备法律效应,但它对目前这一领域的科学家形成强而有力的约束。
令人感到忧虑的是,人类胚胎细胞基因编辑或许不会是目前仅有的两项研究。根据Nature的报道,很多科学家已经将类似的研究论文投递出去,广州医科大学的这篇文章只不过是它们其中的一篇而已。
尽管中国科学院是去年人类基因编辑大会的三方组织者之一,积极参与推动基因编辑伦理规范的讨论以及制定,但是中国更多的正在进行的有关人类生殖细胞基因编辑研究工作尚没有明确的伦理规范。显然,相关的研究工作不仅考验着人类的伦理底线,同时从某种程度上说,不规范的研究活动也会使得其他学者正常利用基因编辑技术进行研究或应用受到阻碍。
原始出处:
Xiangjin Kang. Introducing precise genetic modifications into human 3PN embryos by CRISPR/Cas-mediated genome editing. Journal of Assisted Reproduction and Genetics.May 2016.
Xiangjin Kang. Introducing precise genetic modifications into human 3PN embryos by CRISPR/Cas-mediated genome editing. Journal of Assisted Reproduction and Genetics.May 2016.
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#胚胎基因#
55
#胚胎#
55