国家药监局全新批准12款药品,3个首仿、2个首家通过一致性评价
2021-02-01 医谷网 医谷网
1月29日,药监局发布《2021年01月29日药品批准证明文件待领取信息》,内容显示12个药品获批,包括替格瑞洛、地氯雷他定、他达拉非、利伐沙班......
1月29日,药监局发布《2021年01月29日药品批准证明文件待领取信息》,内容显示12个药品获批,包括替格瑞洛、地氯雷他定、他达拉非、利伐沙班......
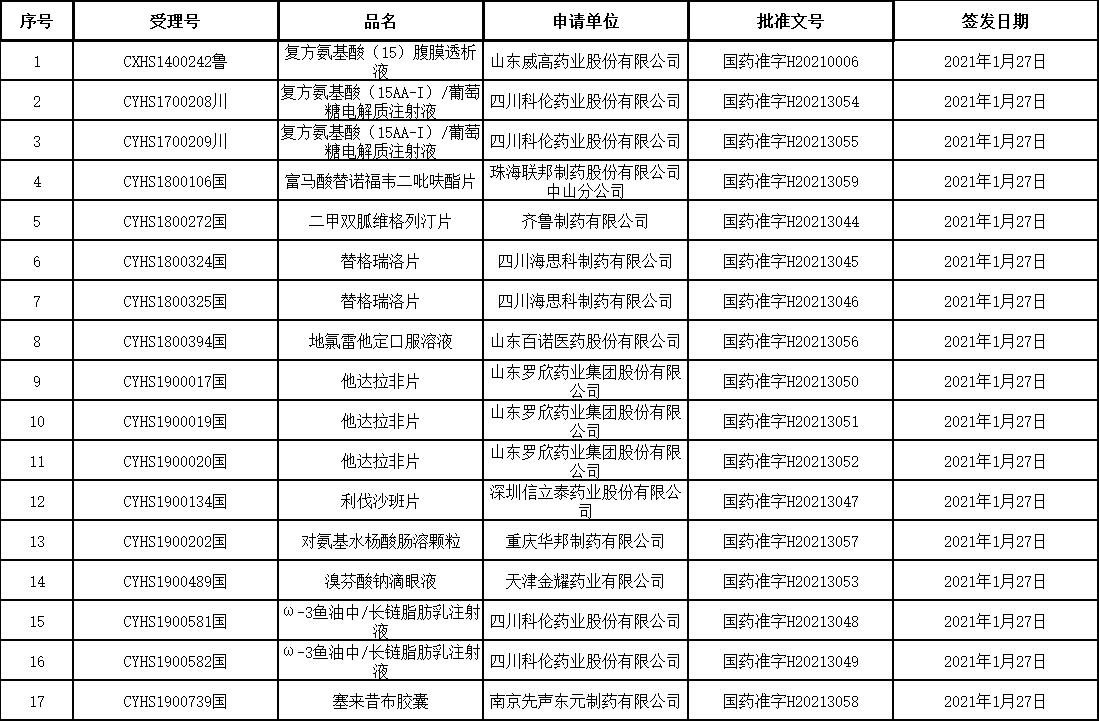
替格瑞洛片
由四川海思科制药有限公司旗下全资子公司海思科制药(眉山)有限公司研发生产,是一种新型的环戊基三唑嘧啶类(CPTP)口服抗血小板药物,它能够可逆性阻断血小板P2Y12受体。替格瑞洛是第一个证实可以显着降低急性冠状动脉综合征患者心血管死亡和总病死率的口服抗血小板药物,同时显着降低心血管事件风险,而不增加出血。该产品目前国内除原研厂家上市外,另有深圳信立泰药业股份有限公司等8家药企上市。
据米内网数据显示,替格瑞洛在城市公立及县级公立医院2019年销售额超过15亿元,2020年上半年销售额近9亿元。
地氯雷他定口服溶液
地氯雷他定(Desloratadine)最早由大日本住友(DainipponSumitomo)和默沙东(MerckSharpDohme,MSD)联合研发,于2001年1月15日获欧洲药物管理局(EMA)批准上市,于2001年12月21日获美国食品药品管理局(FDA)批准上市。由默沙东在英国上市销售(商品名:Neoclarityn)。该药用于季节性过敏性鼻炎,常年性(非季节性)过敏性鼻炎症状的缓解,也可用于与慢性特发性荨麻疹相关的瘙痒和荨麻疹症状性的治疗。
目前国产地氯雷他定制剂主要为片剂,其次还有糖浆、胶囊、干混悬剂等。暂无口服溶液剂型。除了山东百诺制药有限公司还有1企业进行了仿制药上市申请,为恩瑞特药业。
他达拉非片
他达拉非是一种选择性、可逆性的磷酸二酯酶5(PDE5)抑制剂,用于解决男性勃起功能障碍问题,具有起效快,药效持续时间长的特点,且不受高脂饮食和酒精摄入影响。此外,他达拉非还有前列腺增生和肺动脉高压两个可增加的适应症。
他达拉非最早由美国礼来公司研制开发,2004年作为治疗男性勃起功能障(ED)的药物在美国上市,商品名为“CIALIS”(希爱力),并于2005年在国内获批上市。此后,礼来公司又向FDA申请了关于治疗肺动脉高压(PAH)和治疗良性前列腺增生(BPH)的两项适应症,并获得批准。
据药智数据企业版医院销售数据显示,2018年国内样本医院他达拉非片医院销售额为1177.33万元,其中主要市场份额被原研礼来的“希爱力”占据。据医谷目前国产已上市的他达拉非片除刚刚获批的山东罗欣药业外,还有齐鲁制药、南京正大天晴、长春海悦、天士力、恒瑞医药获批。
利伐沙班片
利伐沙班广泛用于静脉血栓栓塞性疾病的预防与治疗,以及非瓣膜性房颤的卒中预防。与同类药物华法林相比,利伐沙班具有起效迅速,疗效可预测,颅内出血发生率低,无需常规凝血监测和常规调整剂量等优势。
利伐沙班原研由拜耳/强生联合开发,商品名为Xarelto。利伐沙班最早于2008/9获得欧盟批准上市,上市之后很快取代了华法林在欧洲的市场。2009/3,利伐沙班在国内获批上市,商品名为拜瑞妥。
国内此前有正大天晴、石药欧意和扬子江的利伐沙班片视同通过一致性评价。正在申请/视同申请利伐沙班片一致性评价的企业还有齐鲁制药、华海药业等在内的20余家企业。
塞来昔布胶囊
塞来昔布作为新一代非甾体抗炎镇痛药,通过选择性抑制环氧化酶-2 (COX-2)来抑制前列腺素生成,达到抗炎症、镇痛的效果。其原研为辉瑞,于 2002 年在美国上市,由 GD SEARLE LLC 公司持有,商品名为西乐葆。国内于 2012 年获 NMPA 批准上市,目前获批适应症包括骨关节炎(OA)、类风湿关节炎(RA)、两岁及以上患者的幼年型类风湿关节炎(JRA)、强制性脊柱炎(AS)等。
据Insight 数据库显示,目前国内除了辉瑞的塞来昔布胶囊(商品名:西乐葆)获批进口外,另有包括恒瑞、石药等 6 家企业已相继获批。
除以上获批药品外,科伦药业的复方氨基酸(15AA-Ⅱ)/葡萄糖(10%)电解质注射液、山东百诺医药的地氯雷他定口服溶液、重庆华邦制药的对氨基水杨酸肠溶颗粒是获批的3个首仿药物,齐鲁制药的二甲双胍维格列汀片和天津金耀药业的溴芬酸钠滴眼液是2个首家通过一致性评价。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#首仿#
173
#一致性#
91
#药监局#
79
#国家药监局#
80
#评价#
103
不错
266