癌症转移重大发现:K离子,氧气,T细胞和免疫抑制密切关联
2016-10-06 MedSci MedSci原创
美国国家癌症研究中心终身研究员Nicholas P. Restifo博士,他在癌症免疫基础研究方面获得了不少重要成果。他们研究组刚刚发现了肺脏中抗癌免疫反应受到抑制的机制。这一机制与氧气抑制T细胞的抗癌活性有关。采用遗传方法或药物来抑制免疫细胞的氧感应能力可以阻止肺转移。这一研究成果公布在Cell杂志上。同时,还发现细胞外K离子浓度对T细胞受体(TCR)驱动的AKT-mTOR磷酸化的作用,从而抑制
美国国家癌症研究中心终身研究员Nicholas P. Restifo博士,他在癌症免疫基础研究方面获得了不少重要成果。他们研究组刚刚发现了肺脏中抗癌免疫反应受到抑制的机制。这一机制与氧气抑制T细胞的抗癌活性有关。采用遗传方法或药物来抑制免疫细胞的氧感应能力可以阻止肺转移。这一研究成果公布在Cell杂志上。同时,还发现细胞外K离子浓度对T细胞受体(TCR)驱动的AKT-mTOR磷酸化的作用,从而抑制了T细胞效应功能(T cell effector function),文章发表在最新一期Nature上。
转移是大多数癌症死亡的原因。长期以来人们都猜测,癌症转移过程要求扩散癌细胞与细胞环境之间的合作。一个关键的环境组件就是局部的免疫系统,它可以发挥作用击退入侵癌细胞。
研究人员发现T细胞包含一组氧感应蛋白,它们发挥作用限制了肺脏中的炎症。这项新研究表明,氧气也抑制了T细胞的抗癌活性,由此使得扩散至肺脏的癌细胞能够躲避免疫攻击,建立转移灶。
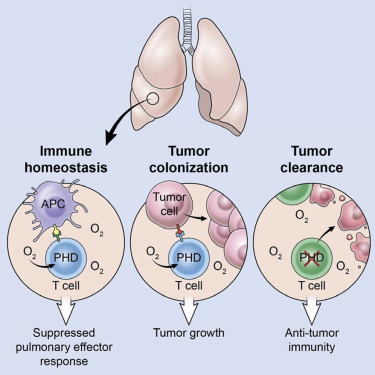
研究小组发现,称作为脯氨酸羟化酶(prolyl hydroxylase domain ,PHD)的氧感应蛋白,在T细胞内发挥作用阻止了对频繁进入肺脏的无害粒子产生过于强烈的免疫反应。这一保护机制也使得循环癌细胞能够在肺脏中找到立脚点。具体说来,研究人员发现PHD蛋白促进了调控T细胞发育,这类T细胞可以抑制免疫系统其它组件的活性。他们还发现PHD蛋白限制了炎症T细胞发育,抑制了它们生成一些癌症杀伤分子的能力。
为了测试PHD蛋白是否在肺脏中促进了肿瘤细胞生长,研究人员利用了T细胞缺失PHD蛋白的一种“基因敲除”小鼠品系。给这些PHD基因敲除小鼠以及未被改变的正常小鼠注入黑色素瘤细胞。令人惊讶地是,尽管正常小鼠肺脏中显示大量的癌性黑色素瘤细胞, T细胞缺失PHD蛋白的小鼠肺脏中几乎没有黑色露的迹象。
鉴于他们发现PHD蛋白抑制了肺脏中的炎症免疫反应,研究人员想知道抑制PHD是否可以提高过继细胞转移的疗效——这种免疫疗法利用了患者自身T细胞识别和攻击癌症的能力。在过继细胞转移中,研究人员从患者肿瘤组织中提取出T细胞,在实验室将它们扩增到极大的数量,随后与一种T细胞生长因子一起通过静脉注入患者体内,希望这些细胞将返回癌症部位并消除它。
在这些实验中,研究小组在存在一种叫做dimethyloxaloylglycine (DMOG)的药物的情况下扩增了抗肿瘤T细胞,DMOG可阻断PHD蛋白的活性。在实验室中,药物处理提高了T细胞的杀癌性能,当给予已建立转移癌的小鼠时,药物处理的这些T细胞比未经处理的T细胞更好地消除了癌症。其他的研究也曾发现DMOG处理可提高人类T细胞的杀癌性能。Restifo小组正在研究将这些结果应用到一些人类过继细胞转移免疫治疗临床试验中。
Restifo 说:“过继细胞转移免疫治疗为操控从患者体内提取的自身T细胞提供了一个独特的机会。尽管我们的研究结果是在小鼠中获得,我们渴望能够测试采用药物、遗传学方法来破坏T细胞中的氧感应机器或调控环境氧气,是否将提高人体中T细胞介导的免疫疗法对癌症的疗效。”
在细胞外K离子的研究中发现通过升高细胞外K离子浓度能产生抑制效应,与膜电位无关。通过过表达钾通道Kv1.3能促进T细胞效应功能,从而在体外和体外增强肿瘤清除能力和动物生存。这些研究表明,离子通道类靶点药物可能成为肿瘤治疗新的策略。
原始出处:
Eil R, Vodnala SK, Clever D, Klebanoff CA, Sukumar M, Pan JH, Palmer DC, Gros A, Yamamoto TN, Patel SJ, Guittard GC, Yu Z, Carbonaro V, Okkenhaug K, Schrump DS, Linehan WM, Roychoudhuri R, Restifo NP. Ionic immune suppression within the tumour microenvironment limits T cell effector function. Nature. 2016 Sep 14;537(7621):539-543.
Clever D, Roychoudhuri R, Constantinides MG, Askenase MH, Sukumar M, Klebanoff CA, Eil RL, Hickman HD, Yu Z, Pan JH, Palmer DC, Phan AT, Goulding J, Gattinoni L, Goldrath AW, Belkaid Y, Restifo NP. Oxygen Sensing by T Cells Establishes an Immunologically Tolerant Metastatic Niche. Cell. 2016 Aug 25;166(5):1117-1131.e14.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#重大发现#
0
继续关注!
75
谢谢分享!
89
好文章,受益
95
文章很好,继续关注
79
#癌症转移#
66
了解一下!
101
学习了,分享一下!
65
阅读了谢谢。
69