肿瘤微环境的异质性:不是一首简单的小情歌
2016-09-07 VTALK 肺癌前沿 vitalk
Influence of tumour micro-environment heterogeneity on therapeutic response肿瘤微环境的异质性 Melissa R. Junttila & Frederic J. de Sauvage Nature 2013 肿瘤的生成,与新生肿瘤细胞,与细胞外的基团,肿瘤血管和免疫细胞的共同进化密切

肿瘤的生成,与新生肿瘤细胞,与细胞外的基团,肿瘤血管和免疫细胞的共同进化密切相关。肿瘤的成功繁殖生长并最终发生转移,并不是单独被基因水平的改变所决定的,而同样受到肿瘤微环境的调控影响,后者将决定具有某种基因改变的肿瘤细胞是否得以优势选择而增殖生长。在这种情况下,将肿瘤看成是完整独立的“器官”,而不仅仅是转化的上皮细胞团块,来进行研究和分析,就变得至关重要。即便在同一个病灶中,肿瘤的表型也在发生着戏剧性的动态变化,支持肿瘤结构的基质细胞,生长因子的组成,血管供应,和免疫细胞之间的“交互协作”,处在动态的变化状态。肿瘤微环境的异质性将对治疗疗效和耐药发生产生巨大的影响。免疫细胞的浸润牵涉到多种细胞的参与,这些细胞群可能具有促进肿瘤生成或抗肿瘤的作用。同时他们的活动状态和在肿瘤团块中的位置也在发生着动态的变化;血管网络可以随着起源器官,成熟程度(外膜细胞的覆盖范围),间质压力和功能性改变而发生异质性。肿瘤相关成纤维细胞根据活化状态,在组织中的位置,压力反应和起源也在发生着显著的影响
来自Genetech Molecular biology的Melissa R.Junttila 博士和 Frederic J.de Sauvage.在《Nature》上发表了一篇review,简要阐述了肿瘤细胞的微环境组成部分是如何共建肿瘤异质性,肿瘤中的基质细胞如何导致耐药的发生,以及在对抗肿瘤微环境肿瘤学家们所作出的努力和面临的挑战。Origin and influence of micro-environment heterogeneity 肿瘤微环境异质性的起源
CAF:肿瘤相关成纤维细胞
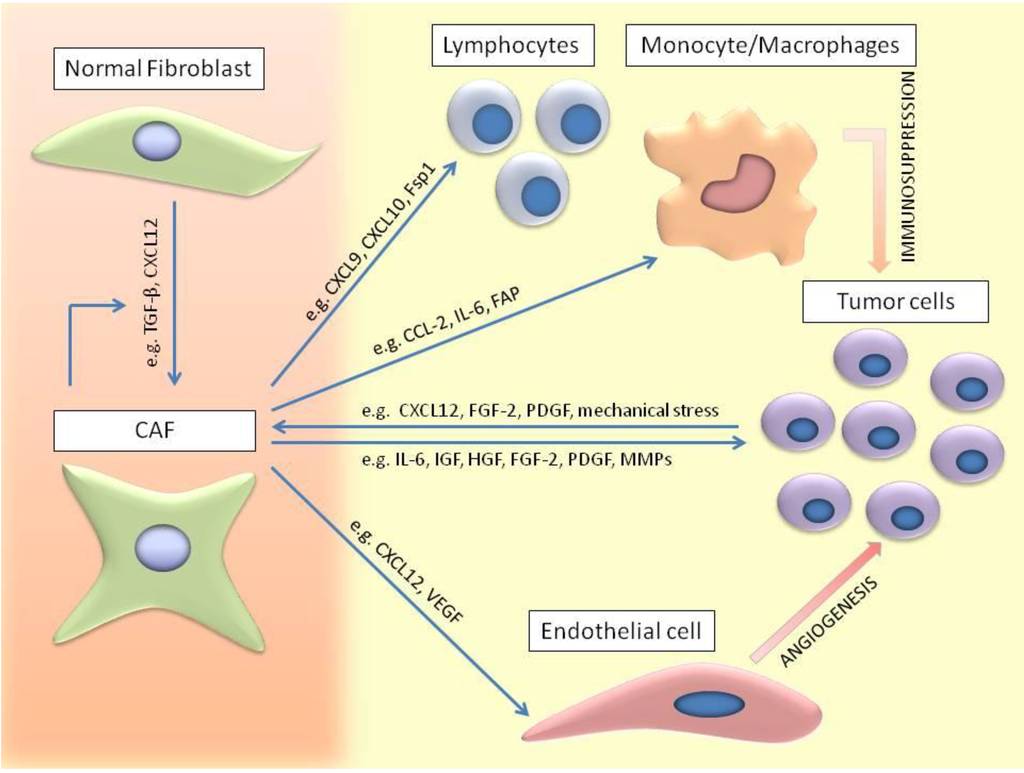
正常的成纤维细胞阻碍肿瘤的生成,但CAF(肿瘤相关性成纤维细胞)则能够显著的促进肿瘤生长,与前者相比,CAFs具有过度分芽增殖,细胞外团块增生和独特的细胞因子分泌的特点(基质细胞衍生因子SDF1;血管生长因子 VEGF;PDGF;和HGF)。
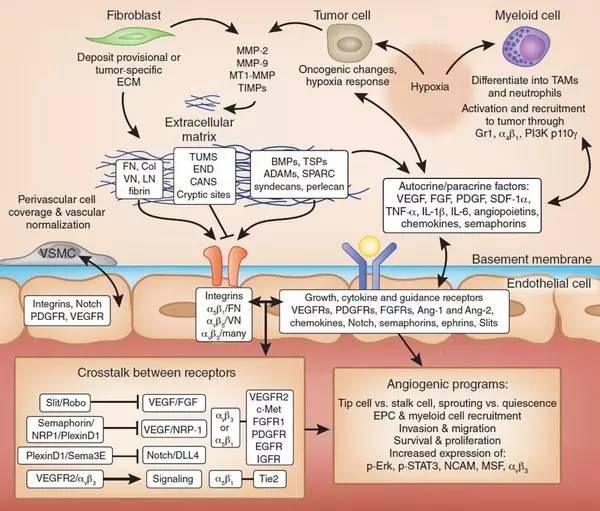
血管
免疫细胞
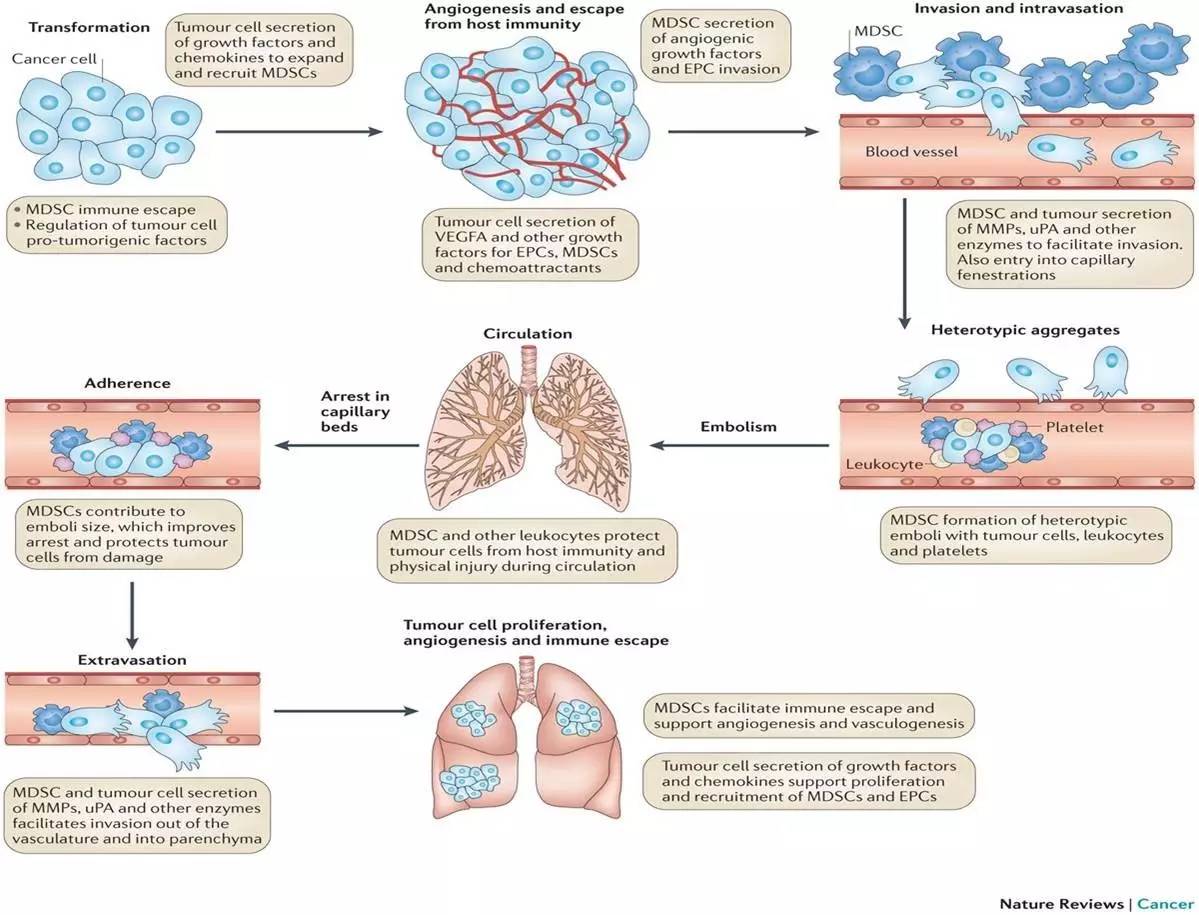 T细胞的活化与checkpoint信号通路的激活和抑制有关。直接抑制T细胞作用的方式,是通过上调CTLA-4,PD1配体与受体的相互作用实现。间接抑制T细胞作用,则是通过培育一个肿瘤抑制的微环境,MDSC(myeloid derived suppressor cell population)在其中扮演重要角色。肿瘤招募免疫抑制细胞,不仅仅抑制了免疫反应,而且通过释放促进血管生成的因子(VEGFA,bFGF等),来诱导血管生成。MDSC能够直接抑制NK细胞的功能,并促进免疫抑制T细胞的数量。
T细胞的活化与checkpoint信号通路的激活和抑制有关。直接抑制T细胞作用的方式,是通过上调CTLA-4,PD1配体与受体的相互作用实现。间接抑制T细胞作用,则是通过培育一个肿瘤抑制的微环境,MDSC(myeloid derived suppressor cell population)在其中扮演重要角色。肿瘤招募免疫抑制细胞,不仅仅抑制了免疫反应,而且通过释放促进血管生成的因子(VEGFA,bFGF等),来诱导血管生成。MDSC能够直接抑制NK细胞的功能,并促进免疫抑制T细胞的数量。尽管已经有针对non tumor cell的治疗(如贝伐珠单抗抗血管治疗,和免疫治疗)已经取得了很好的临床数据,,但是将对肿瘤微环境的理解应用于临床实践仍然面临巨大的挑战。这些挑战包括,直接分析人体肿瘤基质中的细胞成分,到应用对人体肿瘤的异质性的观察来建立preclinical model,并阐明这种异质性与疗效,药物反应和耐药的关系。
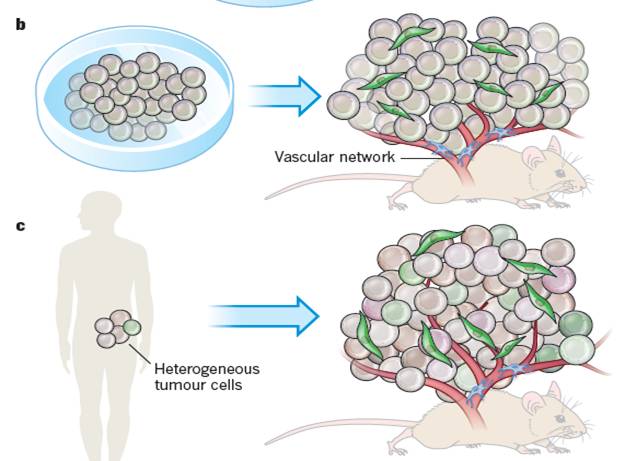
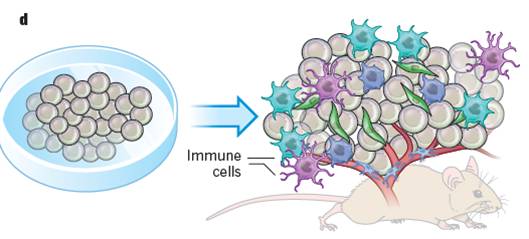
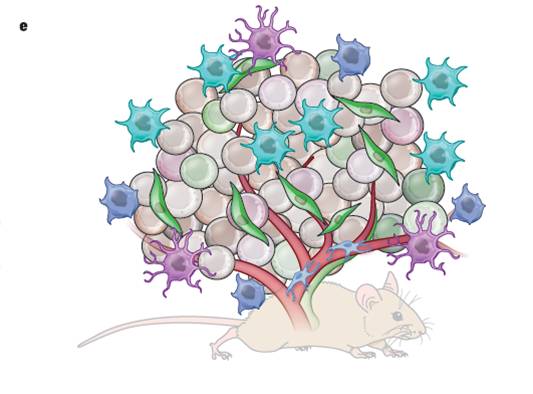
对肿瘤微环境异质性的深入了解,将有可能帮助肿瘤学家发现新的治疗策略,以获得更好和更长的肿瘤缓解;但显然,这不是一首简单的小情歌
内容转载于微信号:VTALK (在微信中查找viTALK101)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













学习学习。。。
100
继续学习
92
继续关注
83
继续关注
103