柳叶刀子刊:剑桥大学科研团队发表基于真实世界的AI模型,可提前6年预测阿尔茨海默病
2024-08-07 测序中国 测序中国 发表于上海
研究团队开发了一个稳健且可解释的预测预后模型(PPM),可准确预测个体从认知正常或轻度认知障碍(MCI)阶段进展为AD的风险及速度,准确率达81.66%、敏感性82.38%、特异性80.94%。
随着人口老龄化趋势的不断加剧,痴呆症给全球医疗保健领域带来了巨大挑战,影响全球约5500多万人,并造成了巨大的经济负担;其中,阿尔茨海默病(AD)是痴呆症的主要病因,占综病例的60-80%。已有研究表明,早期准确的诊断和干预对于减缓AD疾病进展和改善患者生活质量至关重要,但现有标准记忆测试缺乏敏感性,尤其是在疾病的早期阶段,更具特异性的PET或腰椎穿刺检测价格昂贵,大多数患者无法获得。因此,目前亟需有效的早期痴呆症诊断和预后工具。
近年来,基于机器学习(ML)算法的人工智能(AI)模型在早期痴呆症预测中显示出巨大潜力,可通过分析大规模、多模态数据来识别早期疾病标志物,并对患者进行精准分层。但由于代表人群局限性、缺乏标准化的疾病评估方法以及无法预测个体化的健康轨迹,这些ML模型在实际临床应用受到严重限制。
为克服上述挑战,英国剑桥大学心理学系的科研人员在eClinicalMedicine上发表题为“Robust and interpretable AI-guided marker for early dementia prediction in real-world clinical settings”的文章。研究团队开发了一个稳健且可解释的预测预后模型(PPM),可准确预测个体从认知正常或轻度认知障碍(MCI)阶段进展为AD的风险及速度,准确率达81.66%、敏感性82.38%、特异性80.94%。此外,PPM还能从研究数据泛化到真实世界患者数据,其预测结果可通过纵向临床结果得到验证,同时具备可扩展性和临床普适性。综上,PPM模型超越了传统的二元分类方法,有望为痴呆症的早期诊断、个性化治疗及医疗资源的高效分配提供有力支持。

文章发表在eClinicalMedicine
PPM模型的构建与训练
研究团队使用美国阿尔茨海默病神经影像学计划(ADNI)研究队列410名个体(样本内验证)的认知测试和结构性MRI扫描(显示灰质萎缩)数据来训练、构建PPM模型;并使用另外609名来自ADNI队列个体的现实世界数据,以及来自多个记忆诊所900名参与者的独立数据集对PPM模型进行样本外验证,包括英国NHS记忆诊所脑结构与功能定量MRI(QMIN-MC)、新加坡国立大学记忆老化与认知中心数据集(MACC)。
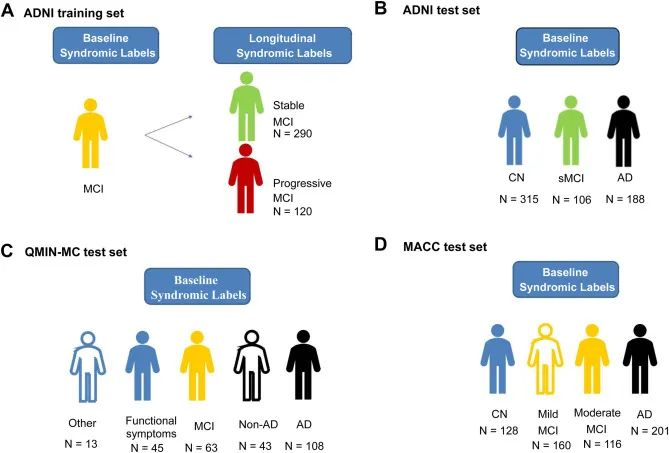
图1. 用于PPM训练和验证的队列数据概述
研究团队首先利用ADNI队列的基线数据(即首次评估)对PPM进行了训练,并特别使用了ACE-R 记忆量、MMSE量表和灰质密度(GM密度)等数据类型(图1)。结果显示,PPM在预测MCI患者是否会进展为AD方面表现出色,可以81.66%的准确率区分稳定型MCI患者(sMCI,3年内持续接受MCI诊断的个体)和进展型患者MCI(pMCI,3年内进展为AD的个体),AUC为0.84、敏感性为82.38%、特异性为80.94%。
PPM度量张量分析显示,与MMSE和GM密度相比,ACE-R记忆量是最具区分度的特征;ACE-R记忆量、MMSE和GM密度之间存在正交互作用,这为交互多模态特征在准确区分sMCI和pMCI方面的作用提供了证据。有趣的是,如果结构性MRI数据不可用,当从多个互补的认知测试中获取的记忆性能数据可用时,PPM依旧能保持良好分类性能。
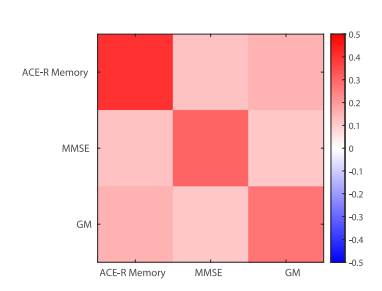
图2. sMCI与pMCI分类的PPM度量张量
PPM的个性化预后预测
为超越传统二元分类(sMCI vs pMCI),预测个体未来的认知衰退风险,研究团队使用标量投影法生成了PPM衍生的个体化AI引导多模态标志物(预测预后指数),帮助临床医生理解和解释每个患者的风险因素和预测结果。利用GMLVQ分类器集成,研究团队发现预后指数在区分不同疾病阶段(AD、MCI、CN)的群体中表现出色,准确率达到81.40%。
此外,PPM衍生的预后指数在预测认知健康轨迹方面具有临床相关性:通过分析个体患者数据,PPM能够识别出关键的认知和脑结构特征,这些特征与疾病进展风险密切相关。特别地,增加GM密度可提高PPM在预测早期或症状前阶段患者未来认知能力下降的敏感性。上述结果表明,这种个性化预测能力使得PPM在临床实践中具有重要的应用价值,有助于制定针对性的干预措施。
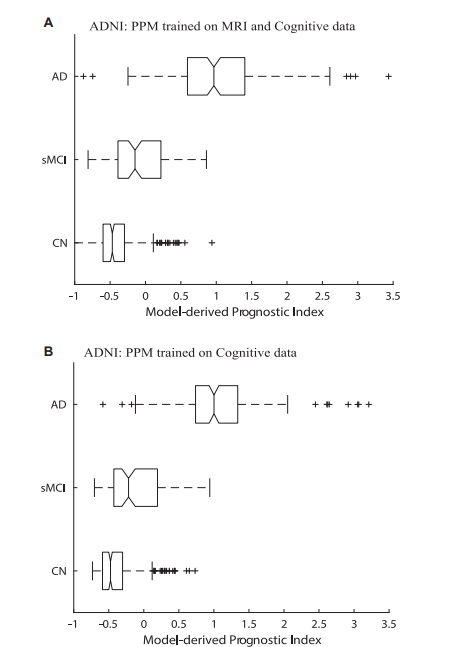
图3. ADNI验证集的PPM衍生预后指数
PPM在真实世界数据中的验证
为评估PPM的互操作性和临床适用性,研究团队使用来自现实世界患者队列的QMIN-MC、MACC数据进行测试,使用基线数据为每个个体提取PPM衍生的预后指数,测试了其是否与临床诊断相关(图4)。结果显示,在QMIN-MC、MACC队列中,PPM衍生的预后指数在不同诊断组别间存在显著差异;经过认知和MRI数据训练的PPM能够准确区分AD患者与其他组别,以及不同程度的MCI患者。这一结果证实了PPM模型在真实世界临床数据中的有效性,能够根据首次评估的非侵入性数据对患者进行精准分层,并预测未来的认知健康状况,为临床诊断和治疗提供了有力的支持。
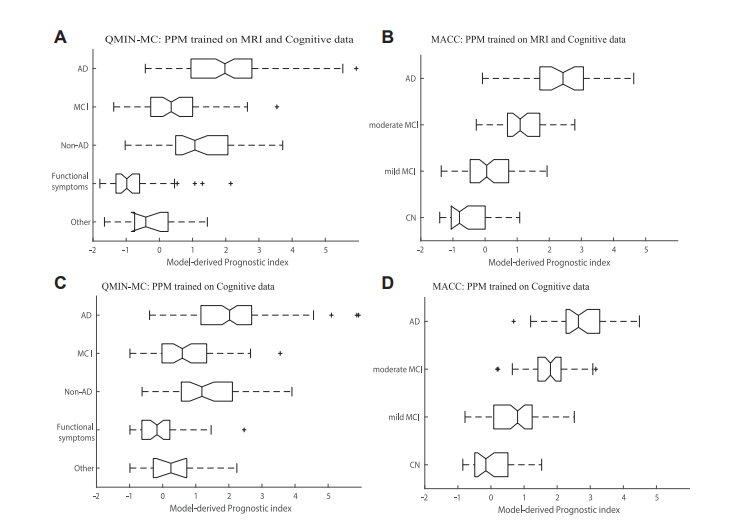
图4. 临床测试数据的PPM衍生预后指数
研究团队还开发了一种基于PPM衍生预后指数对个体进行分层的方法,使用多项逻辑回归来捕捉预后指数与认知能力下降率的关系,以确定疾病进展的不同可能性,将患者分为三类:①症状保持稳定(PPM指数<0);症状快速进展(PPM指数>1);③症状缓慢进展(PPM指数介于0和1之间)。
在ADNI数据中,大部分认知正常个体被归为稳定,而多数AD患者被预测为进展;QMIN-MC 和MACC数据中也观察到类似的分层效果,且部分被诊断为MCI的患者被PPM预测为稳定,这可能有助于减少早期痴呆的误诊。
PPM衍生的预测与标准临床评估和统计方法的比较
为进一步验证PPM的临床有效性,研究团队将其与常规临床评估、简单机器学习模型(逻辑回归)和传统统计方法(多元回归)进行比较(图5)。结果表明,PPM比上述诊断方法具有更高的准确性和灵敏度。这些结果证实了PPM在预测未来认知健康方面的优越性能和临床应用潜力,其可比标准临床评估更准确地预测患者未来认知能力的下降。
PPM衍生预后预测的纵向验证
研究团队测试了根据基线(即首次评估)患者数据,使用PPM衍生的预后指数(即稳定、缓慢进展和快速进展)进行的分层是否与未来的临床结果(即临床诊断表明转为AD的纵向数据)一致。研究团队使用了超过6年的MACC纵向数据,并进行了生存分析(图5)。
结果显示,被PPM预测为稳定的个体很少(0.5%)转化为AD,而被预测为缓慢进展和快速进展的个体在3年内的AD转化率分别为18.9%、41.4%,表明在基线时依据PPM进行分层能更精确预测转化风险,基于临床诊断的标准分层相比,其准确率高出约三倍。Cox风险模型证实,与标准临床标志物(灰质萎缩、认知能力下降)相比,PPM衍生的预后指数能更精确预测患者的AD转化风险。Kaplan-Meier生存分析显示,稳定组整体具有"不转化为AD"的优势,而快速进展组具有更高的转化为AD的风险。
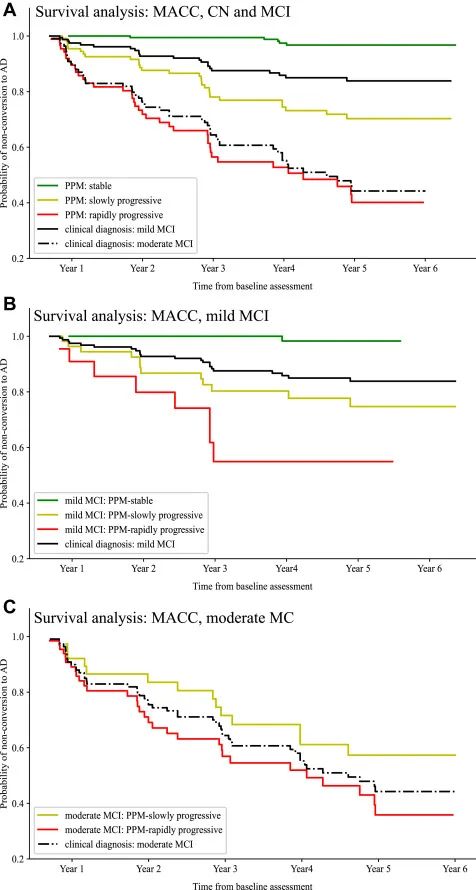
图5. MACC数据的生存分析
综上所述,研究团队构建稳健且可解释的预测预后模型——PPM来弥合AI和临床转化之间的差距;并使用真实世界、常规收集的、非侵入性和低成本(认知测试、结构性MRI)的患者数据,验证其临床效用。研究证明,PPM展现出了优异的泛化能力和临床实用性,能够稳健地预测MCI的患者是保持稳定还是进展为AD,从而提供未来认知能力下降的个体化预后指标。相较标准临床标志物或临床诊断,这种PPM衍生的多模态标志物可更精确地预测AD转化。将该AI指导工具用于真实世界临床环境中可减少减少侵入性和高成本诊断测试的需求,并减少痴呆早期阶段的误诊,改善患者福祉。
参考文献:
Liz Yuanxi Lee j, Delshad Vaghari. et al. Robust and interpretable AI-guided marker for early dementia prediction in real-world clinical settings. eClinical Medicine(2024).
https://doi.org/10.1016/j.eclinm.2024.102725
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#阿尔茨海默病# #预后模型#
67