利用CRISPR/Cas9系统治疗HBV感染取得突破性进展
2016-07-27 佚名 生物谷
乙型肝炎病毒(HBV),简称乙肝病毒,是一种DNA病毒,属于嗜肝DNA病毒科(Hepadnavividae),可导致肝硬化和肝癌的发生,给全球带来严重的疾病负担。据世界卫生组织(WHO)报道,全球有20多亿人曾受到过乙型肝炎病毒(HBV)感染,大约3.5亿至4亿人罹患慢性乙肝病毒(HBV)感染,在亚洲和非洲发病率尤其高。我国的乙肝病毒感染率约60%-70%;乙肝表面抗原携带率约占总人口的7.1
乙型肝炎病毒(HBV),简称乙肝病毒,是一种DNA病毒,属于嗜肝DNA病毒科(Hepadnavividae),可导致肝硬化和肝癌的发生,给全球带来严重的疾病负担。据世界卫生组织(WHO)报道,全球有20多亿人曾受到过乙型肝炎病毒(HBV)感染,大约3.5亿至4亿人罹患慢性乙肝病毒(HBV)感染,在亚洲和非洲发病率尤其高。我国的乙肝病毒感染率约60%-70%;乙肝表面抗原携带率约占总人口的7.18%,以此计算,全国约有9300万人携带乙肝病毒,其中慢性乙型肝炎患者约2000万例。
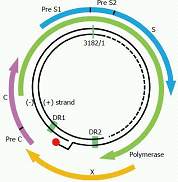
尽管现有的抗病毒药物可以控制乙型肝炎病毒,但却不能完全清除它。因此,一旦停止治疗患者肝脏中的HBV会重新活化。这是因为cccDNA “匿藏”在细胞核中。
细胞外的乙型肝炎病毒DNA是一种松弛环状的双链DNA(relaxed circularDNA,rcDNA)分子。HBV的基因组(rcDNA)进入到细胞核后,rcDNA在病毒蛋白和宿主细胞因子的帮助下修复成共价闭合环状DNA(cccDNA)。cccDNA是乙肝病毒前基因组RNA复制的原始模板。
只要还存在于肝细胞中,乙肝病毒cccDNA的复制就不会停止,并与病毒蛋白装配成新的完整HBV病毒颗粒,以芽生的方式再感染健康的肝细胞,而这是导致乙肝复发的根本原因。因此,尽管每个肝细胞内只有约5~50个cccDNA拷贝,但是只要这些cccDNA池稳定,就可以使得病毒的持续感染延续,因而清除肝细胞内的cccDNA是乙肝彻底治愈所必需的。
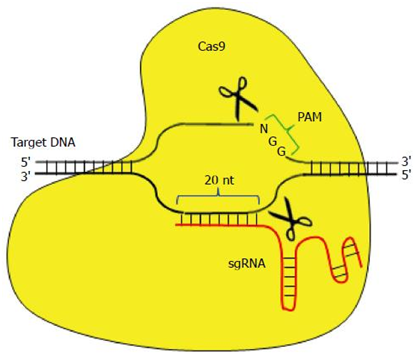
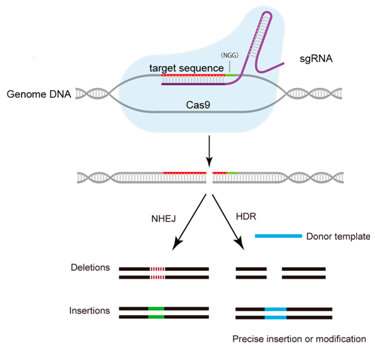
CRISPR/Cas9系统靶向结合特异性的DNA序列,诱导靶DNA双链发生精确切割。在哺乳动物细胞中,这样的切割能够被一种被称作非同源末端连接(non-homologous end-joining, NHEJ)的紧急修复系统快速地修复。NHEJ是高效的,但是并不很准确,因而经常导致一些DNA碱基在修复位点上插入或剔除。鉴于每次读取DNA时是按密码子(每个密码子由连续的三个碱基组成)读取的,在关键位点上发生的这些小的DNA序列变化经常破坏相应的基因和它的蛋白产物的功能。基于此,世界各地的研究人员尝试利用CRISPR/Cas9系统治疗HBV感染,并且取得重大进展。
为了让读者更好地了解CRISPR/Cas9在治疗HBV感染上取得的进展,小编在http://www.ncbi.nlm.nih.gov/pubmed网站上以CRISPR和(HBV or (Hepatitis B Virus))为关键词,除去不相关的检索结果和综述论文类型的检索结果,获得11项相关的检索结果。接下来,小编对这11项检索结果,进行如下解读。
1. Sci Rep:利用CRISPR/Cas9系统高效地抑制HBV
Scientific Reports, 02 June 2015, doi:10.1038/srep10833
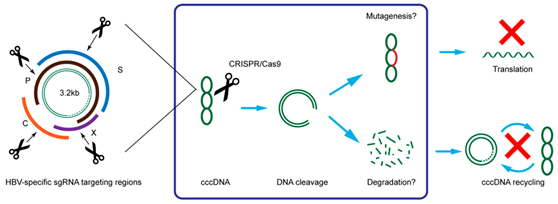
在一项新研究中,麻省理工学院的研究人员利用CRISPR/Cas9 系统,对受到HBV感染的哺乳动物肝细胞进行基因组编辑,从中删除了乙肝病毒(HBV)DNA。他们靶向切割了HBV病毒共价闭合环状DNA(cccDNA)中的一些特异性位点。
在这项研究中,Vyas Ramanan和同事们设计了24条单向导RNA(sgRNA)来靶向从在线病毒序列信息资源库中鉴别出的一些HBV基因组位点。经过初筛测试后,研究小组将三种最有效的sgRNA和Cas9蛋白插入到慢病毒载体中,然后将它们转导进将HBV DNA整合到宿主基因组的人类肝细胞内。
通过利用包含整合性HBV基因组DNA的稳定转染细胞系展开实验,研究人员观察到HBV总DNA和cccDNA逐渐减少,在36天时cccDNA下降了92%。他们还观察到HBV病毒基因表达和复制水平显著减少。
如今,Ramanan计划在人类肝脏嵌合小鼠模型中测试这一方法,以评估和优化传递方法和给药方法,及更好地了解需要除去多少的cccDNA才能到达人类功能性的治愈。
2. Mol Ther Nucleic Acids:利用CRISPR/Cas9抑制HBV感染
Molecular Therapy Nucleic Acids, 2014 December; 3(12): e216, doi:10.1038/mtna.2014.68
在一项新的研究中,为了研究源自传染性HBV的cccDNA是否能够被直接靶向摧毁,来自美国福克斯蔡斯癌症中心(Fox Chase Cancer Cente)的研究人员在表达HBV受体---钠离子-牛磺胆酸共转运蛋白(sodium taurocholate cotransporting polypeptide, NTCP)---的人HepG2中使用CRISPR/Cas9基因编辑系统。他们测试了不同的HIV特异性的向导RNA(gRNA),并证实它们能够高达8倍地抑制HBV感染。这种抑制是HBV cccDNA发生突变和缺失---类似于Cas9切割染色体DNA和随后基于NHEJ介导的DNA修复时观察到的情形---所导致的。α干扰素(IFN-α)并不对CRISPR/Cas9系统的抗病毒活性产生可衡量的影响,这提示着Cas9和NHEJ活性并不受这种细胞因子(即IFN-α)诱导的先天免疫反应的影响。
3. Mol Ther:利用CRISPR/Cas9让HBV cccDNA功能性灭活
Molecular Therapy, online publication 21 June 2016; doi: 10.1038/mt.2016.94
在一项新的研究中,通过采用下一代测序(NGS)技术,来自美国福克斯蔡斯癌症中心(Fox Chase Cancer Cente)的 Christoph Seeger、Ji A Sohn和同事们确定了在Cas9切割和基于非同源末端连接(NHEJ)的修复后,HBV cccDNA所发生的完整突变谱。他们发现,90%以上的乙肝病毒DNA都能被Cas9切割。此外,研究结果还表明,在Cas9切割后对HBV DNA进行基因编辑的效率是在对被HBV感染的细胞进行α干扰素(IFN-α)处理后发生的APOBEC蛋白介导的胞嘧啶脱氨基作用的1500倍以上。研究还发现,以前用来检测DNA胞嘧啶脱氨基作用的3D-PCR方法方法高估了发生基因编辑的HBV DNA的数量和频率。
总之,研究人员证实CRISPR/Cas9系统是迄今为止在功能上让HBV cccDNA失活和提供一种慢性乙肝治愈疗法的最好途径。
4. Gene Ther:我国科学家利用CRISPR破坏乙肝病毒
Gene Therapy, 2015, 22, 404–412; doi:10.1038/gt.2015.2; published online 5 February 2015
2015年2月5日,来自我国军事医学科学院放射与辐射医学院研究所、第四军医大学西京医院、日本京都大学和华中农业大学兽医学院等处的研究人员,在Nature旗下Gene Therapy期刊上发表一项最新的研究成果,题为“Harnessing the clustered regularly interspaced short palindromic repeat (CRISPR)/CRISPR-associated Cas9 system to disrupt the hepatitis B virus”。 在这项研究中,研究人员研究靶向乙肝表面抗原(HBsAg)编码区的CRISPR/Cas9系统,在体外培养的肝细胞中和活的小鼠体内的效果。结果表明,CRISPR/Cas9可在体内和体外抑制HBV复制和表达,可能是治疗HBV感染的一种新策略。
5. Mol Ther Nucleic Acids:利用CRISPR/Cas9系统在体内促进肝内HBV模板清除
Molecular Therapy Nucleic Acids, 2014, 3, e186; doi:10.1038/mtna.2014.38
在当前的抗病毒治疗下,HBV cccDNA持续存在是根治慢性乙肝的一大障碍。治愈慢性乙肝需要新的策略来特异性地破坏HBV cccDNA。为了研究CRISPR/Cas9系统是否能够切割HBV基因组,来自中国国立台湾大学的研究人员设计出8种针对A基因型HBV的gRNA。利用这些HBV特异性的gRNA,CRISPR/Cas9系统显著性地降低感染上HBV表达载体的Huh7细胞中的乙肝核心抗原(HBcAg)和乙肝表面抗原(HBsAg)产生。在这8种筛选出的gRNA中,他们鉴定出两种有效的gRNA。有趣的是,其中的一种靶向保守性HBV序列的gRNA在不同基因型的HBV中都能发挥作用。
利用一种流体动力学-HBV持续存在小鼠模型,研究人员进一步证实这种CRISPR/Cas9系统能够切割肝内含有HBV基因组的质粒,促进它在体内被清除,从而导致血液中的HBsAg水平下降。
这些数据提示着CRISPR/Cas9系统能够在体外和体内破坏HBV表达模板,并且表明它有潜力根除持续性HBV感染。
6. Virus Res:利用CRISPR/Cas9系统在体内和体外诱导抗HBV效应
Virus Research, Volume 217, 2 June 2016, Pages 125–132, doi:10.1016/j.virusres.2016.04.003
在一项新的研究中,来自中国同济大学生命科学与技术学院的研究人员利用CRISPR/Cas9系统靶向剔除HBV基因组中的保守性区域。通过让核酸内切酶Cas9携带HBV S基因和X基因的同源序列,他们构建出pCas9。通过利用pCas9开展实验,他们证实pCas9-2能够更好抵抗HBV产生,而且在Huh7和HepG2细胞之间没有显著差异。
在M-TgHBV的HBV感染小鼠模型中,注射pCas9会降低血液中的HBsAg水平和肝脏中的HBcAg水平。
总之,这种人工构建的CRISPR/Cas9系统能够诱导抗HBV效应,而且有潜力作为一种新的疗法治疗慢性HBV感染。
7. Sci Rep:利用CRISPR/Cas9系统破坏HBV S基因和X基因保守性序列
Scientific Reports, 2015 Sep 3;5:13734. doi: 10.1038/srep13734
为了在治疗上应用于人体,人工设计出的核酸内切酶Cas9应当能够识别不同基因型的HBV,同时产生最小的脱靶效应。
针对此,在一项新的研究中,德国研究人员鉴定出HBV基因组的S区域和X区域在不同基因型中都保守的HBV序列,而且能够利用一种Cas9酶特异性地和高效地靶向切割这些保守性序列。这一方法不仅破坏报告细胞系中的游离HBV cccDNA和HBV在染色体上的整合靶位点,而且也破坏慢性感染和新感染的肝癌细胞系中的HBV复制。
这些数据提示着将CRISPR/Cas9系统作为旨在治愈HBV感染的新策略具有可行性。
8. World J Gastroenterol:利用双gRNA指导的CRISPR/Cas9系统高效地抑制HBV复制
World Journal of Gastroenterology, 2015 Aug 28; 21(32):9554-65, doi:10.3748/wjg.v21.i32.9554
为了筛选和研究有效地抵抗A、B、C和D基因型HBV的gRNA,来自中国北京大学医学部的研究人员总共设计出15种gRNA(分别记为gRNA-1,gRNA-2,…,gRNA-15)。他们从中选择了11种靶向HBV基因组调节区域的双gRNA组合。他们研究了每种gRNA和这11种双RNA组合抑制A、B、C和D基因型HBV复制的效率。
研究人员证实所有的gRNA能够显著地抑制体外细胞培养物中的HBsAg或HBeAg产生,所有双RNA组合能够高效地抑制A、B、C和D基因型HBV中的HBsAg或HBeAg产生,而且当与单个gRNA相比时,双RNA组合抑制HBsAg或HBeAg产生的效率显著增加。
再者,通过利用PCR直接测序,研究人员证实这些双gRNA组合能够通过移除这两种使用的gRNA的切割位点之间的序列片段,特异性地破坏HBV表达模板。最为重要的是,gRNA-5和gRNA-12的双gRNA组合不仅能够高效地抑制HBsAg和/或HBeAg产生,而且也破坏HepAD38细胞中的HBV cccDNA池。
这些结果提示着CRISPR/Cas9系统能够高效地破坏HBV表达模板(A、B、C和D基因型HBV),而且没有明显的细胞毒性。
9. J Gen Virol:利用CRISPR/Cas9系统抑制不同基因型HBV复制
Journal of General Virology, 2015 Aug;96(8):2252-61, doi:10.1099/vir.0.000159
为了研究利用CRISPR/Cas9系统是否可能破坏HBV DNA模板,来自中国武汉大学的研究人员设计出8种靶向不同基因型HBV的保守区域的gRNA,而且这些gRNA能够在体外和体内显著地抑制HBV复制。再者,这种HBV特异性的gRNA/Cas9系统能够抑制不同基因型HBV在细胞中的复制,而且利用单个gRNA/Cas9系统能够显著降低HBV DNA,而且利用不同的gRNA/Cas9系统组合能够清除HBV DNA。
10. Antiviral Res:利用CRISPR/Cas9系统高效抑制HBV复制
Antiviral Research, Volume 118, June 2015, Pages 110–117, doi:10.1016/j.antiviral.2015.03.015
作为一种新的基因组编辑工具,CRISPR/ Cas9系统能够被用来准确地和高效地改造和修饰基因组DNA。
在一项新的研究中,来自中国苏州大学的研究人员合成出4种靶向HBV基因组保守区域的单向导RNA(sgRNA)。在Huh7细胞和HBV复制性细胞HepG2.2.15中,CRISPR/ Cas9系统降低HBV产生。他们进一步证实CRISPR/Cas9的直接切割和这种切割介导的突变发生于转染细胞的HBV cccDNA中。
在携带HBV cccDNA的小鼠模型中,通过快速地尾静脉注射含sgRNA-Cas9的质粒导致较低水平的HBV cccDNA和HBV蛋白产生。
总之,这种CRISPR/Cas9系统能够准确地和高效地靶向HBV cccDNA和抑制HBV复制。它有可能被用来治疗慢性HBV感染。
11. Virology:利用CRISPR/Cas9系统抑制HBV DNA积累
Virology, Volume 476, February 2015, Pages 196–205, doi:10.1016/j.virol.2014.12.001
在一项新的研究中,来自美国杜克大学和埃默里大学的研究人员通过对细菌Cas9基因和单向导RNA(sgRNA)进行慢病毒转导,观察到在体外的HBV慢性感染和新感染的模型中,HBV DNA产生受到高效抑制。HBV特异性的Cas9/sgRNA组合降低总HBV DNA水平高达1000倍左右和降低HBV cccDNA水平高达10倍左右,而且也通过突变让残留的绝大多数HBV DNA失活。
总之,这些数据提供概念验证表明CRISPR/Cas9系统有潜力有效地剔除慢性HBV感染者体内的HBV cccDNA池。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#HBV#
41
great~~~~
99
#CRISPR#
60
#CRISPR/Cas9#
0
#Cas9#
51
#HBV感染#
58
#系统治疗#
67
#Cas#
58
#RISPR/Cas9#
86