建议收藏!局部晚期鼻咽癌五大治疗方法
2022-12-08 放疗前沿 网络 发表于上海
鼻咽癌在全世界的发病率并不高,其高发区主要在东南亚和中国南方。鼻咽癌大部分属于低分化或未分化鳞状细胞癌,其恶性程度较高,易出现远处转移。
鼻咽癌在全世界的发病率并不高,其高发区主要在东南亚和中国南方。我国有世界上约 80% 的鼻咽癌患者,尤其是 广东、广西、福建、江西等省发病率较高,部分地区可高达( 15 ~ 50) /10 万,其中约 75% 患者诊断时即为晚期。
鼻咽癌大部分属于低分化或未分化鳞状细胞癌,其恶性程度较高,易出现远处转移。随着诊治技术的推广及改进,鼻咽癌患者的生存率得到了很大提高,但局部复发及远处转移仍然是目前鼻咽癌治疗失败的主要原因。
临床表现
鼻咽癌的发病位置具有一定的隐蔽性,在疾病早期,其临床症状并不明显,所以难以及时发现,鼻咽内部的淋巴管较为丰富,在这样的条件下,极易发生癌细胞转移的情况。
症状包括鼻塞、面颊或鼻区肿胀,还可有流涕、涕血、发热、复视、视物模糊、头痛、眼球突出、颅神经麻痹等。鼻咽癌早期的临床症状大部分表现为出血,有的患者在擤鼻过程中鼻涕中出现血丝,有的患者在吸鼻子后痰中出现血丝,随着疾病的发展,患者将会出现不同程度的耳鸣、耳内闭塞以及听力减退。
检查
鼻内镜检查
显示鼻黏膜坏死、溃疡出血、表面常有恶臭的干痂或脓痂。晚期T/NK细胞型患者常发生鼻骨、鼻甲、鼻中隔或硬腭广泛骨质破坏。甚至面部严重变形。
影像学检查
①早期表现为咽隐窝闭塞,咽侧壁小的软组织隆起,鼻咽腔不对称;
②肿瘤可侵犯翼内肌,使之粗大、模糊,与周围脂肪间隙消失;
③进一步发展可侵犯翼内板、翼外板、眶壁、上颌窦后壁及颅底等邻近结构,表现为骨质破坏侵蚀;
④ 强扫描肿块有不同程度强化;
⑤常伴颈部淋巴结转移及远处转移。
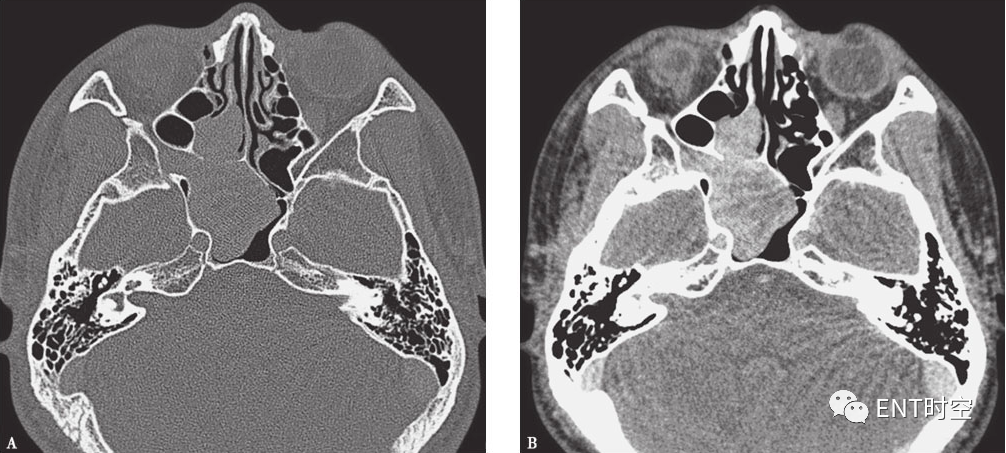
鼻咽纤维血管瘤
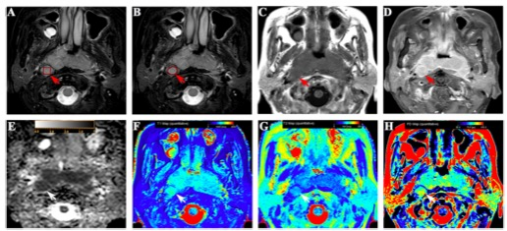
A.CT横断面(骨窗)示右侧鼻咽腔内结节状软组织肿块,突入翼腭窝、蝶窦和后组筛窦,右侧蝶腭孔扩大;
B.CT横断面(软组织窗)示右侧鼻咽腔内结节状软组织肿块,密度均匀,边界清楚。
治疗
鼻咽癌在全世界的发病率并不高,其高发区主要在东南亚和中国南方。我国有世界上约80%的鼻咽癌患者,尤其是广东、广西、福建、江西等省发病率较高,部分地区可高达(15~50)/10万,其中约75%患者诊断时即为晚期。鼻咽癌大部分属于低分化或未分化鳞状细胞癌,其恶性程度较高,易出现远处转移,单纯放疗或同步放化疗是鼻咽癌重要的治疗手段。随着时代的进步,鼻咽癌的治疗方法也是日趋增多,药物治疗从辅助化疗、诱导化疗、同期放化疗、抗EGFR治疗到免疫治疗不断更新,放射治疗从二维放疗、三维适形放射治疗到适形调强放射治疗,不但提高了放疗的精准性,更减轻了放疗的副作用。尽管鼻咽癌对放化疗敏感以及新药物和新技术的应用,但失败率仍然较高,失败的主要原因是远处转移和区域复发。
本文从调强放射治疗、诱导化疗、同期放化疗、抗EGFR分子靶向治疗、免疫检查点抑制剂(PD-1/PD-L1)五个方面总结近年来局部晚期鼻咽癌治疗现状及进展。
01
调强放射治疗
适形调强放射治疗(IMRT)是放射物理、放射技术、医学影像和计算机技术密切结合的产物,它具有从三维方向上使高剂量曲线的分布与肿瘤靶体积形状一致,并明显减少周围正常组织器官的照射剂量和体积的能力。IMRT的剂量分布高度适形,准确勾画靶区就成为调强放射治疗的关键,基于《2017国际指南:鼻咽癌临床靶区勾画》《NCCN临床实践指南:头颈部肿(2018.V2)》,ICRU50和ICRU62号报告,进行靶区及危及器官的勾画准则。
当前,IMRT已成为应用最广泛的鼻咽癌放疗技术,尤其是在鼻咽癌高发的华南地区,很多县市级医院都开展鼻咽癌调强放射治疗。IMRT技术治疗早期鼻咽癌的5年生存率可达90%以上,局部晚期鼻咽癌的5年生存率为74.5%~86.0%。
02
诱导化疗
诱导化疗能短时间内减轻肿瘤负荷及缩小瘤体,还能杀灭远处微转移病灶,能快速缓解肿瘤压迫周围组织形成的症状与体征,在近期疗效显著。以铂类为主的诱导化疗是主要选择药物,TP、TPF成为局部晚期鼻咽癌诱导化疗的主要方案,目前多个试验显示头颈部肿瘤中TPF方案诱导化疗较PF方案更有生存优势,研究认为诱导化疗可降低远处转移率。
研究成果
1.杨保庆等研究46例局部晚期鼻咽癌,2周期TP方案诱导化疗后,1例CR(2.2%),36例PR(78.3%),9例SD(19.5%)。
2.多西他赛、顺铂治疗有效率高,安全性好。
3.2019年新英格兰医学杂志发表一项来自中国的鼻咽癌多中心研究成果,该研究纳入480例Ⅲ-Ⅳ期鼻咽癌随机分成2组,242例患者接受吉西他滨+顺铂诱导化疗3个周期,后再进行3个周期的同步放化疗。238例仅接受同步放化疗,中位随访时间为42.7个月。诱导化疗组3年无复发生存率为85.3%,同步放化疗组76.5%,诱导化疗组的复发或死亡风险显著降低4%(HR=0.51,95%CI:0.34~0.77,P=0.001);这是目前诱导化疗在局部晚期鼻咽癌降低复发或死亡风险最大型的研究成果之一,把吉西他滨加顺铂的辅助化疗地位前推至诱导化疗,改变了鼻咽癌诱导化疗以紫杉类为主的格局。
03
同期放化疗
同期放化疗已成为局部晚期鼻咽癌的标准治疗方案,多项临床研究显示同期放化疗较诱导化疗、辅助化疗以及单纯放疗能提高患者生存率。
研究成果
-
杨保庆等报道局部晚期鼻咽癌调强放疗,同期单药DDP化疗,3年局部控制率(LCR)、无远处转移生存率(DMFS)、无瘤生存率(DFS)、总生存率(OS)分别为89.1%、82.6%、73.9%、87.0%。
-
lSUN等回顾分析868例鼻咽癌同步化疗调强放射治疗的结果显示,5年疾病特异生存率(DSS)、无局部复发生存率(LRFS)、无区域复发生存率(RRFS)、DMFS和无进展生存率(PFS)分别为84.7%、91.8%、96.4%、84.6%和77.0%。
-
lMAC-NPC研究表明化疗可带来6%的5年OS的获益,其中同期化疗作用最大,单纯诱导化疗、辅助化疗并未带来显著的生存获益。
-
有团队研究局部晚期鼻咽癌3个周期TPF方案诱导化疗+调强放疗同期DDP化疗3个周期与同期放化疗相比,3年无失败生存率分别为80%和72%。2019年在局部晚期鼻咽癌治疗领域的新成就,就是诱导化疗加同期放化疗,既能减轻放疗毒副反应,也显著提高5年DSS、LRFS、RRFS、DMFS。故诱导化疗加同期放化疗在局部晚期鼻咽癌治疗中已形成共识。
04
抗EGFR分子靶向治疗
表皮生长因子受体(epidermal growth factor receptor,EGFR)与鳞状细胞的恶性变、肿瘤细胞的增殖有所相关,EGFR为靶点的分子靶向药物被广泛应用于肿瘤患者的治疗。EGFR在鼻咽癌中的阳性表达率达70%以上,即使在转移病灶中也有超过50%的阳性表达。
尼妥珠单抗是我国批准的第一个以EGFR为靶点的分子靶向药物,能够有效的封闭EGFR,降低肿瘤细胞的增殖,同时提高肿瘤细胞对辐射的敏感性,从而提高放疗敏感度。尼妥珠单抗也是人源化单克隆抗体药物,其具有较强的特异性,较低的不良反应,与放化疗联合治疗鼻咽癌,将发挥协同作用。
05
免疫治疗
免疫检查点主要包括程序性死亡受体-1( programmed death 1,PD-1)、程序性死亡配体-1(programmed death-ligand 1,PD-L1)和细胞毒性T淋巴细胞相关抗原4(CTLA-4)。在新疗法的现有发展中,免疫检查点疗法在治疗复发或转移疾病方面取得了突破,并给复发或转移鼻咽癌带来了新希望。
抗PD-1和PD-L1抗体
PD-1有两个配体,即PD-L1和程序性死亡配体-2(programmed death-ligand 2,PD-L2)。PD-L1蛋白不仅表达于抗原提呈细胞,还表达于B细胞、T细胞和肿瘤细胞。PD-L1与PD-1结合后,可向T细胞传递免疫抑制信号,抑制T细胞免疫,对机体免疫应答起负调控作用。新型抗PD-1可以阻断PD-1对T细胞的抑制作用,从而激活肿瘤患者体内的免疫效应细胞杀瘤效应。
最近研究发现,PD-L1表达与鼻咽癌预后、转移密切相关,目前与鼻咽癌治疗相关的抗PD-1和PD-L1抗体主要包括帕博利珠单抗、纳武利尤单抗、卡瑞利珠单抗。帕博利珠单抗是一种人源化IgG4同型单抗,靶向阻断淋巴细胞上的PD-1;纳武利尤单抗为首个IgG单克隆抗体,对PD-1具有很高的亲和力;卡瑞利珠单抗(SHR-1210)是一种高亲和力、完全人源化的IgG4-κPD-1单克隆抗体,可阻止PD-1与其配体结合。
抗CTLA-4单抗
CTLA-4是免疫球蛋白超家族的成员,细胞毒性T淋巴细胞(CTL)表面受体之一。在正常情况下,T细胞的激活依赖于第一信号(抗原-抗体复合物的形成)和第二信号(B7介导的活化信号)双活化。而CTLA-4可以与CD28竞争性结合到B7上,阻断T细胞受体信号。CTL表面的CTLA-4上调可导致CTL细胞周期阻滞,使肿瘤细胞免疫逃逸增强。
Huang等研究中,检测到CD28和CTLA-4在鼻咽癌肿瘤细胞和肿瘤浸润淋巴细胞中共表达,而CTLA-4的阻断可能为鼻咽癌提供治疗益处。易普利单抗能有效阻滞CTLA-4分子,并通过阻断CTLA-4和B7之间的相互作用,抑制这个消极的免疫信号,从而消除免疫抑制作用及诱导和增强抗肿瘤免疫反应。
总而言之,CTLA-4是一种白细胞分化抗原,是T细胞上的一种跨膜受体,与CD28共同享有B7,而CTLA-4与B7结合后诱导T细胞无反应性,参与免疫反应的负调节。基因重组的CTLA-4Ig可在体内外有效、特异地抑制细胞和体液免疫,对移植排斥反应及各种自身免疫性疾病有显著的治疗作用,毒副作用极低,是目前认为较有希望的新的免疫抑制药物。目前CTLA-4阻断剂主要用于治疗晚期黑色素瘤,其鼻咽癌治疗的安全性、有效性仍需进一步研究。
本文来源于:ENT时空
参考文献:
[1]张斌,莫运燕. 局部晚期及复发或转移鼻咽癌的治疗进展[J]. 临床医学研究与实践,2022,17:192-195.
[2]杨保庆. 局部晚期鼻咽癌治疗现状及进展[J]. 现代肿瘤医学,2021,02:337-341.
[3]张薇. 靶向治疗联合放疗治疗局部晚期鼻咽癌的临床疗效分析[J]. 中国实用医药,2021,23:164-167
本文观点仅代表作者本人,仅供交流学习
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言