Cell Rep:天然分子立功了!糖尿病有望迎来再生细胞疗法
2018-02-28 药明康德 学术经纬
《细胞》子刊《Cell Reports》上,来自迈阿密大学医学院糖尿病研究所的科研人员们在线发表了一项重要研究。他们发现,在一款天然分子的诱导下,胰岛中的一些细胞能分化成β细胞,并对葡萄糖产生反应。这一重要发现有望为我们带来针对糖尿病的再生细胞疗法。
《细胞》子刊《Cell Reports》上,来自迈阿密大学医学院糖尿病研究所的科研人员们在线发表了一项重要研究。他们发现,在一款天然分子的诱导下,胰岛中的一些细胞能分化成β细胞,并对葡萄糖产生反应。这一重要发现有望为我们带来针对糖尿病的再生细胞疗法。
糖尿病分为两种:1型糖尿病是一种严重的疾病,病因在于患者自身的免疫系统错误地对胰岛中产生胰岛素的细胞展开攻击,导致后者被摧毁。因此,患者不得不依赖体外的胰岛素,来进行自身血糖的控制;在2型糖尿病里,患者的β细胞也往往会出现问题,不能100%地工作。因此,在胰岛素治疗之外,胰岛移植就成了这些糖尿病患者、尤其是1型糖尿病患者的一个治疗选择。
然而,胰岛移植有着一大局限——能从中受益的患者以百万计,能使用的细胞却太少。为此,目前的研究也主要集中在如何扩增这些关键的胰岛细胞上。多年来,科学家们取得了一些成果,并成功利用胚胎干细胞、多能干细胞、或是猪的胰岛,开发出了一些能够用于移植的细胞源。但这些方法的安全性和效率依旧值得改进。
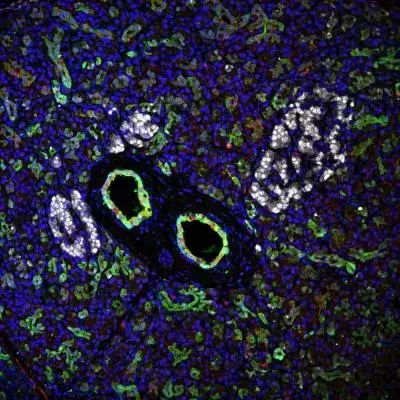
这正是这项研究的意义所在。先前,这支研究团队发现,一款叫做BMP-7的天然生长因子能在非内分泌胰腺组织中,激活一类细胞。在今日发表的研究里,他们进一步阐明,这些对BMP-7产生反应的干细胞存在于胰腺的导管和腺体中。有意思的是,通过对这些细胞进行分子特征分析,研究人员们发现了两个关键的蛋白——对于β细胞发育至关重要的PDX1,以及和组织再生有关的ALK3。而通过特殊的分子捕获技术,他们能将表达这两个蛋白的细胞分离出来,在培养基里进行培养,分化成β细胞!
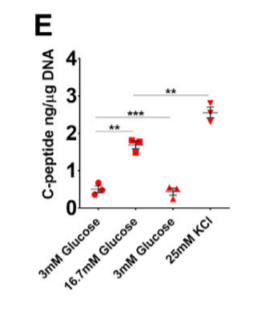
▲这些诱导出的细胞对葡萄糖有反应(图片来源:《Cell Reports》)
“我们对于这些胰脏干细胞的深入研究,有望让我们拥有内源的细胞供给库,用于β细胞的再生。将来,这有望为1型糖尿病患者带来全新的治疗方案,”该研究的共同负责人Juan Dominguez-Bendala博士与Ricardo Pastori博士说道:“我们发现BMP-7能激活这些细胞的生长,这能让我们诱导这些干细胞,产生功能性的胰岛。”

▲该研究的图示(图片来源:《Cell Reports》)
“通过再生医学,我们能在自然胰腺中恢复胰岛素的生产力,并有朝一日取代胰腺或胰岛素产生细胞的移植。在1型糖尿病里,我们需要克服自身免疫,避免免疫系统对新生成的胰岛素产生细胞进行攻击。而我们的方法能提高免疫耐受,无需终身服用抗排斥的药物。”迈阿密大学医学院糖尿病研究所的主任Camillo Ricordi博士补充说。
我们期待这个发现能尽快在大规模的试验中证实自己的潜力,给糖尿病患者带来治愈的希望。
原始出处:
Mirza Muhammad Fahd Qadir, Silvia álvarez-Cubela, Dagmar Klein, et al.P2RY1/ALK3-Expressing Cells within the Adult Human Exocrine Pancreas Are BMP-7 Expandable and Exhibit Progenitor-like Characteristics.Cell Reports.Volume 22, Issue 9, p2408–2420, 27 February 2018 DOI: https://doi.org/10.1016/j.celrep.2018.02.006 |
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#CEL#
62
#再生细胞疗法#
68
#Cell#
68
科技创新.造福人类!加油!
104