【论著】双侧椎动脉不对称性与椎动脉起始段狭窄的相关性分析
2024-06-29 中国脑血管病杂志 中国脑血管病杂志 发表于上海
本研究拟进一步探讨无心脑血管疾病危险因素行颈部血管彩色多普勒超声的人群发生VAOS的相关影响因素及椎动脉不对称性对VAOS的影响。
摘要:目的分析无心脑血管疾病危险因素人群的椎动脉不对称性与椎动脉起始段狭窄(VAOS)病变发生的相关性。方法回顾性连续纳入2019年12月至2021年12月“脑卒中高危人群筛查脑颈动脉超声规范化评估数据库”中无心脑血管疾病危险因素接受颈部动脉粥样硬化超声筛查者共6423例。收集受试者一般资料,包括性别、年龄、体质量指数(BMI)及左、右两侧椎动脉超声检查参数,即椎间隙段(V2段)内径及采用椎动脉血流动力学参数[收缩期峰值流速(PSV)、 舒张期末流速(EDV)和PSV起始段/PSV椎间隙段]评估的VAOS的程度(轻度、中度、重度及闭塞)。依据检测结果将所有患者分为VAOS组与非VAOS组。将椎动脉内径≤2.0mm定义为椎动脉发育不良(VAH);将双侧椎动脉V2段内径差值≥1.2mm定义为椎动脉优势(VAD),并将所有患者分为VAD组和非VAD组(内径差<1.2mm)。最终统计分析时,若涉及侧别,各组以侧进行统计;若未涉及侧别,各组以例数进行统计。以发生VAOS作为因变量,将一般资料、解剖学因素(VAH、VAD)进行单因素Logistic回归分析,并将其中P<0.05的项目作为自变量,进一步采用多因素Logistic回归分析VAOS的独立影响因素。 结果共纳入符合纳排标准的人群6423例,男1985例,女4438例;年龄19~80岁,平均(43±13)岁。其中VAD组628例,非VAD组5795例。(1)与VAD组比较,非VAD组女性占比更高 (69.9%比61.3%,P<0.01),年龄更小[(43±13)岁比(45±14)岁,P<0.01],且年龄<40岁人群占比高于VAD组(46.3%比38.4%,P<0.01),VAH患者比例和VAOS发生比例均低于VAD组 (分别为0.6%比17.2%和1.5%比4.0%,均P<0.01)。(2)无心脑血管疾病危险因素人群发生VAOS的单因素Logistic回归分析结果显示,VAOS组男性比例、年龄、BMI及VAH和VAD的比例均高于非VAOS组,组间差异均有统计学意义(均P<0.05)。进一步进行多因素Logistic回归分析显示,男性 (OR=1.92, 95% CI:1.30~2.85,P=0.001)、年龄 (OR=1.12, 95% CI: 1.10~1.14,P<0.01)和VAD (OR=2.14, 95% CI:1.30~3.40,P=0.002)是无心脑血管疾病危险因素行颈部动脉粥样硬化超声筛查人群发生VAOS的独立危险因素。 结论VAD的发生受性别和年龄影响,VAD是无心脑血管疾病危险因素人群发生VAOS的独立危险因素。
椎动脉起源于左、右侧锁骨下动脉,在颅内汇合为基底动脉,是脑干及颅内后循环的供血动脉。有研究回顾性分析了2490 份门诊血管超声实验室的彩色多普勒超声结果,结果显示,存在至少一侧椎动脉起始段狭窄(vertebral artery origin stenosis,VAOS)或闭塞者的比例为8.2% ,双侧椎动脉起始段均存在狭窄或闭塞者比例为1.4%。新英格兰医学中心后循环系统注册登记研究结果表明,约9%的后循环卒中由椎动脉V1段狭窄导致。Mysior 和Stefańczyk研究表明,健康受试人群双侧椎动脉内管径差值大于25%或0.5mm时,可出现双侧血流动力学的差异,即内径较大一侧椎动脉收缩期峰值流速(PSV)、舒张期末流速(EDV)均更高,阻力指数更低。椎动脉优势(vertebral artery dominance,VAD)是由双侧椎动脉不对称衍生出的概念,其确切定义目前尚未形成共识。既往研究多关注VAD与后循环缺血的相关性,对于VAD引起的双侧椎动脉不对称性与VAOS的关系研究较少。我们既往研究显示,颈动脉粥样硬化人群的VAOS不仅与心脑血管疾病危险因素有关,还与椎动脉解剖学因素(管径、 走行变异)可能存在关联。本研究拟进一步探讨无心脑血管疾病危险因素行颈部血管彩色多普勒超声的人群发生VAOS的相关影响因素及椎动脉不对称性对VAOS的影响。
1 对象与方法
1.1 对象
回顾性连续纳入2019年12月至2021年12月“脑卒中高危人群筛查脑颈动脉超声规范化评估数据库”中11255例行颈部动脉粥样硬化超声筛查的体检人群。
纳入标准:(1)年龄18~80岁;(2)门诊或住院行彩色多普勒超声检查筛查颈部动脉粥样硬化性病变者。排除标准:(1)基本信息不完整;(2)彩色多普勒超声数据缺失或录入错误;(3)椎动脉管壁增厚而引起的椎动脉弥漫性狭窄者;(4)有吸烟、饮酒、高脂血症、高血压病、糖尿病、肥胖[体质量指数(body mass index,BMI)≥28kg/m2]等心脑血管疾病危险因素者;(5)既往有心脑血管病史和家族史者。本研究方案经中山大学附属第六医院医学伦理委员会审核批准(伦理号:2020ZSLYEC-315)。
1.2 仪器与方法
1.2.1 仪器设备:采用荷兰Philips公司生产的IU22或Epiq7及日本日立-阿洛卡公司生产的Ascendus高档彩色多普勒超声诊断仪,选择3.0 ~ 7.0MHz和(或)4.0 ~ 8.0MHz和(或)3.0 ~ 9.0MHz和(或)3.0 ~ 11.0MHz和(或)3.0 ~ 12.0MHz超宽频线阵探头。
1.2.2 数据收集:收集受试者一般资料,包括性别、年龄、BMI及左、右两侧椎动脉超声检查参数,即椎间隙段(V2段)内径和超声评估的VAOS情况。
1.2.3 质量控制:进行超声检测及数据采集的血管超声专业技术人员均来自多中心课题组医院,均经过统一的血管超声检测操作规范培训。超声检测流程及诊断标准参考《中国脑卒中血管超声检查指导规范》,并将检测数据上传至国家卫生健康委国家健康医疗大数据创新应用示范中心的统一数据库。图像质量由质量控制小组人员按照研究方案统 一审查。
1.2.4 评价标准和定义:VAOS的诊断标准参照文献,根据椎动脉血流动力学参数(PSV、EDV和PSV起始段/PSV椎间隙段)确定VAOS程度,即轻度(狭窄率<50%:狭窄段流速PSV起始段≥85cm/s, PSV起始段/PSV椎间隙段≥1.3且EDV起始段≥27cm/s)、中度(狭窄率50%~69%: PSV起始段≥140cm/s,PSV起始段/PSV椎间隙段≥2.1且EDV起始段≥35cm/s)、重度(狭窄率70%~99%: PSV起始段≥220cm/s,PSV起始段/PSV椎间隙段≥4.0且EDV起始段≥50cm/s);闭塞为无血流信号。其中,狭窄以远段(V2~V3段)血流速度(PSV椎间隙段)明显减低,且PSV起始段/PSV椎间隙段≥4.0,出现低阻力性血流频谱改变为重度狭窄与中度狭窄(狭窄率50%~69%)鉴别的重要特征。依据VAOS 程度将受试者分为VAOS组(轻、中、重度狭窄及闭塞)与非VAOS 组(无狭窄)。将椎动脉内径≤2.0mm定义为椎动脉发育不良(vertebral artery hypoplasia, VAH)。VAD的定义为双侧椎动脉管径不对称, 且内径差≥1.2mm(差值法),并将受试者分为VAD组(内径差≥1.2mm)和非VAD组(内径差<1.2mm)。根据《〈中国脑卒中防治报告2020〉概要》中,40岁以上人群为卒中发生的高危人群,将人群分为<40岁组和≥40岁组。
心脑血管疾病危险因素:高血压病、糖尿病、高脂血症、饮酒史、吸烟史、肥胖的诊断依照中国国家卒中登记研究中使用的方法,即高血压病为既往高血压病史,或住院期间在安静状态下间隔1周重复测量血压≥140/90mmHg;糖尿病为既往糖尿病史,或入院后空腹血糖≥7.0mmol/L,或餐后2h血糖≥11.1mmol/L,或经糖耐量试验明确诊断者;高脂血症为既往高脂血症病史,或存在以下情况中任一项:血清低密度脂蛋白胆固醇≥3.12mmol/L,血清总胆固醇≥5.80mmol/L,三酰甘油≥2.25mmol/L;吸烟史为当前或既往吸烟≥1支/d且连续6个月以上;饮酒史为摄入纯酒精≥2个标准量/d(20g/d);肥胖为BMI≥28kg/m2。
1.3 统计学分析
使用R软件(4.2.1版本)对数据进行统计学分析。采用Kolmogorov-Smirnov检验对计量资料进行正态性检验,符合正态分布的计量资料以x- ± s表示,组间比较采用t检验;不符合正态分布的计量资料以中位数和四分位数[M(P25,P75 )]表示,组间比较采用秩和检验;计数资料以频数和百分比[例(%)]表示,组间比较采用χ2检验或Fisher确切概率法。以发生VAOS为因变量,将一般情况(年龄、性别、BMI)、解剖学情况(VAH、VAD)纳入单因素Logistic回归分析,并将其中P<0.05的项目作为自变量,进一步采用多因素Logistic回归分析VAOS的独立影响因素。以P<0.05为差异具有统计学意义。
2 结果
11255例行颈部动脉超声筛查人群中,排除基本信息不完整、彩色多普勒超声数据缺失或录入错误者122例,排除有心脑血管疾病危险因素及心脑血管病史和家族史者4710例,共纳入符合纳排标准的人群6423例,其中男1985例,女4438例;年龄19~80岁,平均(43±13)岁。VAD组628例(左侧VAD 486例,右侧VAD142例),男243例,女385例;年龄19~78岁,平均(45±14)岁。非VAD组5 795例,男1742例,女4053例;年龄19~80岁,平均(43±13)岁。VAOS者112例,其中99例为单侧VAOS,13例为双侧VAOS,男60例,女52例;年龄30~80岁,平均(62±10)岁;轻度狭窄47例,中度狭窄24例,重度狭窄22例,闭塞19例(双侧VAOS者以最高狭窄程度入)。非VAOS组6311例,其中男1925例,女4386例,年龄19~80岁,平均(42±13)岁。
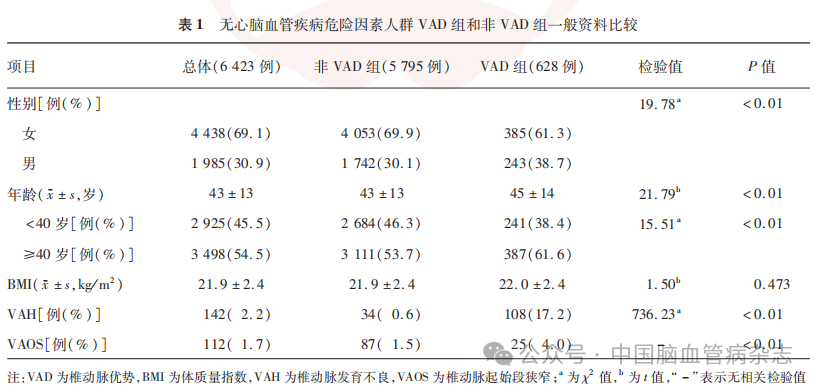
2.1 VAD组和非VAD组一般资料比较
与VAD组比较,非VAD组女性占比更高(P<0.01),年龄更小(P<0.01)。非VAD组年龄<40 岁人群占比高于VAD 组(P<0.01),VAH患者比例和VAOS 发生比例均低于VAD组(分别为0.6%比17.2%和1.5%比4.0% ,均P<0.01)。见表1。
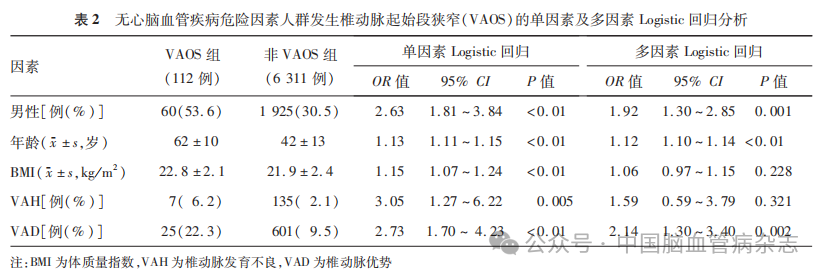
2.2 无心脑血管疾病危险因素人群发生VAOS的单因素及多因素Logistic回归分析
无心脑血管疾病危险因素人群发生VAOS的单因素Logistic回归分析结果显示,VAOS组男性比例、年龄、BMI及VAH和VAD的比例均高于非VAOS组, 组间差异均有统计学意义(均P<0.05)。进一步进行多因素Logistic回归分析显示,男性(OR=1.92, 95% CI:1.30~2.85)、年龄(OR=1.12,95% CI: 1.10~1.14)和VAD(OR=2.14,95% CI:1.30~ 3.40)是无心脑血管疾病危险因素人群发生VAOS的独立危险因素(均P<0.05)。见表2。
3 讨论
颅内、外动脉病变的分布特点与不同危险因素相关性的机制目前尚不明确。系统性因素(如高血压病、糖尿病等危险因素及遗传因素)和局部性因素(如血流动力学及血管走行、解剖结构等)对不同血管的影响可能存在选择特异性。受血流剪应力影响,后循环动脉粥样硬化病变多发生于椎动脉起始段与入颅段,且以前者更为多见。一项针对VAOS的荟萃分析表明,以DSA为参考标准,CT血管成像(CTA)、增强MR血管成像(MRA)和彩色多普勒超声诊断VAOS 的特异度分别为95.2%(95% CI:83.8 ~ 99.4)、94.8% (95% CI:91.1 ~ 97.3)和97.7% (95% CI:95.2 ~ 99.1),敏感度分别为100% (95% CI:15.8 ~ 100.0)、93.9% (95% CI:79.8 ~ 99.3)和70.2% (95% CI:54.2 ~ 83.3)。Hua等回顾性分析了653例后循环缺血性卒中患者,纳入247例单侧VAO患者,以DSA为参考标准,彩色多普勒超声诊断椎动脉起始段轻度(狭窄率小于50%)、中度(狭窄率50%~69%)、重度狭窄(狭窄率70%~99%)的敏感度分别为94.5%、96.2%、88.7%。研究表明,VAOS与颈动脉狭窄有共同的危险因素,包括高血压病、糖尿病、冠心病和吸烟史等。我们既往研究表明,椎动脉解剖学因素可能是颈动脉粥样硬化人群发生VAOS 的影响因素,其中走行变异(OR=0.47,95% CI: 0.26~0.80,P=0.009)为发生VAOS的保护因素, 此外,心脑血管疾病危险因素中的吸烟史(OR= 1.91,95% CI:1.53~2.37,P<0.01)、高血压病(OR=1.90,95% CI:1.56~2.31,P<0.01)、高脂血症(OR=1.30,95% CI:1.01~1.65,P<0.01)、糖尿病(OR=1.44,95% CI:1.14~1.80,P= 0.002)为发生VAOS的独立危险因素。对于无心脑血管疾病危险因素人群发生VAOS的影响因素, 目前尚缺少相关研究。本研究基于“脑卒中高危人群筛查脑颈动脉超声规范化评估数据库”,对该数据库中6423例无心脑血管疾病危险因素行颈部动脉粥样硬化超声筛查人群数据进行分析,结果显示, VAD对VAOS的发生存在影响。
本研究结果显示,与VAD组比较,非VAD组女性占比更高(P<0.01),年龄更小(P<0.01),且非VAD组中年龄<40 岁人群比例高于VAD组(P<0.01)。随着年龄的增长,动脉管壁的弹性蛋白纤维被胶原纤维所取代,并且细胞外基质中弹性蛋白含量减少,可诱导动脉管壁中的弹性纤维机械断裂从而导致血管重构。李佳珊等研究显示,无心脑血管疾病危险因素的成年人颈动脉管腔结构、血流速度与年龄、性别及侧别有关。本研究结果显示, VAD的检出受性别和年龄因素影响,提示性别和年龄因素可能均参与椎动脉管径的重构。VAD、VAH均为由双侧椎动脉不对称衍生出的概念,其确切定义尚未形成共识,诊断标准目前尚不统一,导致各研究报道的检出率差异较大。本研究VAH(椎动脉内径≤2.0mm)和VAD(双侧椎动脉管径不对称,且内径差≥1.2mm)诊断采用大多数研究的诊断标准,结果显示,VAH检出率为2.2%,与采用同样VAH 诊断标准(内径≤2.0mm)的研究结果(1.9%)接近。李子锋等将椎动脉内径差≥0.3mm定义为VAD,结果显示,前循环梗死组的VAD检出率为21.91%,后循环梗死组的VAD检出率为52.04%,均高于本研究的9.8%,可能原因为本研究设定的椎动脉管径差值更大(内径差≥1.2mm),纳入者均为无心脑血管疾病危险因素人群且以女性为主,而女性血管较男性细。
Mysior和Stefańczyk研究表明,健康受试人群[无椎-基底动脉疾病史、无椎-基底动脉解剖结构异常(起源异常、走行明显迂曲、颅内段闭锁)和动脉粥样硬化疾病病史]双侧椎动脉内径差值大于25%或0.5mm时,可出现双侧血流动力学的差异,即双侧PSV、EDV和阻力指数比值明显增大(均P<0.05), 内径较大一侧椎动脉PSV和EDV更高,阻力指数更低(均P<0.05)。本研究多因素Logistic回归分析显示,VAD 是无心脑血管疾病危险因素人群发生VAOS的独立危险因素(OR=2.14,95% CI:1.30~ 3.40,P=0.002),提示VAD人群椎动脉管径差异所导致的血流动力学的变化可能是促进VAOS发生的重要因素。本研究单因素Logistic回归分析结果显示,VAOS组内VAH患者比例明显高于非VAOS组,差异有统计学意义(OR=3.05,95% CI:1.27~ 6.22,P=0.005)。但是,多因素Logistic回归分析显示,两组VAH患者比例差异无统计学意义(OR= 1.59,95% CI:0.59~3.79,P=0.321),提示VAH可能为混杂因素。本研究中142例VAH者中有108例存在VAD,34例不存在VAD,我们分析原因可能为对于VAH人群,也可存在双侧管径接近而不存在VAD现象,VAD所导致的管径不对称才是VAOS 的危险因素。
既往研究较少关注年龄对VAOS的影响。迈阿密卒中登记(Miami Stroke Registry,MIAMISR)研究显示,年龄是后循环卒中患者发生VAOS的唯一预测因子(P=0.028)。张峰等研究显示,年龄是颈动脉粥样硬化性病变患者发生VAOS的独立危险因素(OR=1.08,95% CI:1.07~1.09,P<0.01)。本研究多因素回归分析显示,年龄是无心脑血管疾病危险因素人群发生VAOS的独立危险因素(OR=1.12, 95% CI:1.10~1.14,P<0.01),且VAOS组年龄高于非VAOS组(P<0.01)。动脉粥样硬化危险因素的暴露风险随着年龄的增加而增加,本研究纳入的受检者均无相关心脑血管疾病危险因素,提示随着年龄增长血管顺应性减退可能是导致椎动脉管径重构的原因,进而成为VAOS的相关暴露因素。
女性雌激素对心血管有保护作用,其机制可能为雌激素可抑制炎症发展、促进内皮损伤修复并改善体内脂质代谢、提高血浆高密度脂蛋白胆固醇浓度、减低血浆低密度脂蛋白胆固醇和三酰甘油浓度。 张峰等既往的研究显示,女性是颈部动脉粥样硬化性病变患者发生VAOS 的保护性因素(OR= 0.53,95% CI:0.42~0.66,P=0.001)。本研究多因素Logistic回归分析显示,男性是无心脑血管疾病危险因素人群发生VAOS的独立危险因素(OR= 1.92,95% CI:1.30~2.85,P=0.001),提示在无心脑血管疾病危险因素暴露的情况下,女性雌激素的调节可能对椎动脉粥样硬化的发生起到了预防作用。
本研究通过对大样本、多中心、标准化的数据进行分析,结果显示,无心脑血管疾病危险因素人群双侧椎动脉不对称性对VAOS的发生存在影响,并提示VAH和VAD的概念并不完全等同,未来应对VAD的诊断标准进行进一步探讨。本研究可能存在一定的局限性。首先,本研究使用超声筛查和评估椎动脉起始段,VAOS的检出率可能会受影响,结果中的相关性可能会被低估。其次,本研究未收集椎动脉走行角度等数据以进一步分析相关血流动力学对VAOS发生的影响,危险因素方面未矫正其他因素,比如饮食、运动等。
综上所述,VAD的发生受性别和年龄影响, VAD是无心脑血管疾病危险因素人群发生VAOS的独立危险因素。本研究结果有待进一步验证。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#双侧椎动脉不对称性# #椎动脉起始段狭窄#
29