JAMA Oncol:抗阿特珠单抗抗体与晚期肝癌患者临床预后不良相关
2022-10-24 MedSci原创 MedSci原创
在接受阿特珠单抗/贝伐单抗治疗的晚期肝细胞癌患者中,ADA水平的高度升高可能与临床预后不良有关
在IMbrave 150试验中,阿特珠单抗和贝伐单抗 (Atezo/Bev) 联合治疗显著改变了晚期肝细胞癌(HCC)的治疗前景。虽然对Atezo/Bev治疗有反应的患者表现出了良好的生存结局,但仍有小部分患者表现出原发性耐药。
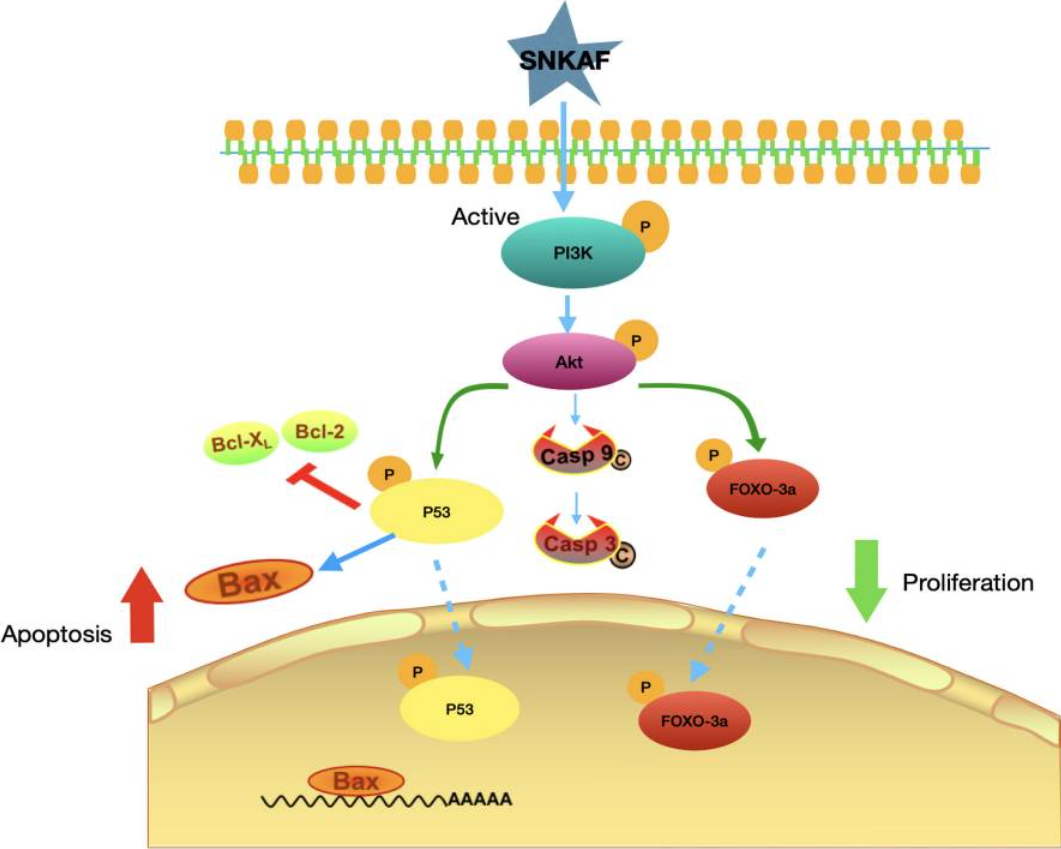
阿特珠单抗具有免疫原性,可能会导致不良的抗药物抗体(ADA)反应。这会干扰阿特珠单抗介导的作用,影响药物清除和血清浓度或诱导抗体中和。
该研究旨在探索晚期肝细胞癌患者在接受Atezo/Bev治疗后,ADA水平升高与临床结果的临床和免疫学相关性。
这项队列研究前瞻性地招募了174位接受Atezo/Bev一线治疗的晚期肝细胞癌患者。在治疗前和第3周(第2个疗程的第1天[C2D1])时检测其血清ADA水平(竞争性酶联免疫吸附测定)。主要评估ADA阳性与治疗结果和T细胞功能的相关性。
排除了样本不合格、失访和撤出试验的患者后,132位(发现队列:50位;82.0%的男性,中位年龄61岁;验证队列:82位,85.4%的男性,中位年龄61岁)患者被纳入分析,其中23位 (17.4%) 患者在C2D1时检测到ADA的强烈应答 (≥1000 ng/mL)。进展性患者在C2D1时的ADA水平明显高于应答患者(中位水平:65.2 vs 0 ng/mL)。
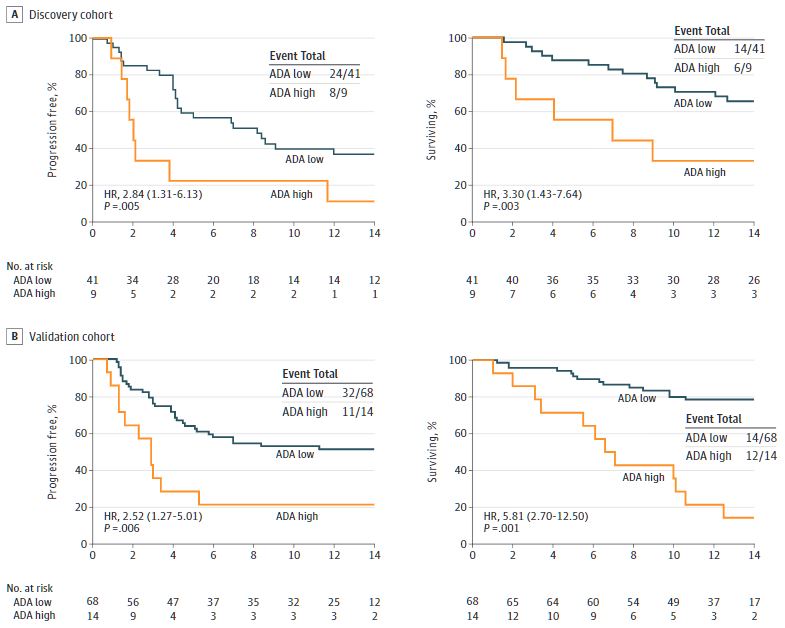
在两个队列中不同ADA水平患者的无进展生存率和总生存率
无论是在发现还是在验证队列中,与低ADA水平的患者相比,C2D1时的高ADA水平与接受Atezo/Bev治疗的缓解率降低(发现队列:34% vs 11%;验证队列:29% vs 7%)、无进展生存期变短(HR:发现队列:2.84,p=0.005;验证队列:2.52,p=0.006)和总生存期变短(HR:发现队列:3.30,p=0.003;验证队列:5.81,p=0.001)相关。
在多变量Cox回归分析中,在调整了各种混杂因素后,高ADA水平的临床意义仍然存在,且在1000 ng/mL或更高的水平上时最为显著。与低ADA水平的患者相比,高ADA水平患者血清中的阿特珠单抗浓度降低,CD8阳性T细胞增殖受损,CD8阳性T细胞中的γ-干扰素和α-肿瘤坏死因子减少。
综上,该研究发现,在接受Atezo/Bev治疗的晚期肝细胞癌患者中,第2个疗程第1天时的ADA水平的高度升高可能与临床预后不良有关。高ADA水平可能会减少阿特珠单抗的暴露,进而减弱药物的抗癌效果。
原始出处:
Kim C, Yang H, Kim I, et al. Association of High Levels of Antidrug Antibodies Against Atezolizumab With Clinical Outcomes and T-Cell Responses in Patients With Hepatocellular Carcinoma. JAMA Oncol. Published online October 20, 2022. doi:10.1001/jamaoncol.2022.4733
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言