Cell惊人发现:会传染的癌症
2015-04-10 何嫱 生物通
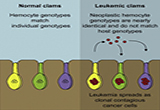
数十年来,白血病爆发毁灭了北美东海岸的一些软壳蛤(soft-shell clams)种群,其却是由于恶性肿瘤细胞从一个蛤传播至另一个蛤所导致。在4月9日的Cell杂志上,研究人员将之称作为是“惊人至极”的一个研究发现。霍华德休斯医学研究所和哥伦比亚大学的Stephen Goff说:“证据表明肿瘤细胞自身具有传染性,在海洋中这些细胞可从一个动物传播至另一个动物处。我们知道这一定是真实的,因为肿瘤细胞
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#CEL#
71
#Cell#
75
生命很复杂
122