胃蛋白酶原(PG)临床应用大全!
2022-09-08 检验之声 豪迈生物
血清PG联合Hp检测,有助于评估胃癌发生风险,可以作为普通人的常规胃癌筛查手段,但是,它并不能替代胃镜检查,针对高危人群,依然强烈推荐进行胃镜检查。
一、什么是“胃蛋白酶原”?
胃蛋白酶原(PG)是胃蛋白酶的前体,根据其生化性质和免疫原性将其分成2个亚群,1~5组分的免疫原性相同,称为胃蛋白酶原Ⅰ(PGⅠ),主要由胃底腺的主细胞和黏液颈细胞分泌;组分6和7被称为胃蛋白酶原Ⅱ(PGⅡ),除由胃底腺的主细胞和黏液颈细胞分泌外,贲门腺和胃窦的幽门腺的黏液颈细胞以及十二指肠上段也能产生PGⅡ。

通常情况下,约有1%的PG透过胃黏膜毛细血管进入血液循环,进入血液循环的PG在血液中非常稳定。血清PGⅠ和PGⅡ反映胃黏膜腺体和细胞的数量,也间接反映胃黏膜不同部位的分泌功能。当胃黏膜发生病理变化时,血清PG含量也随之改变。因此,监测血清中PG的浓度可以作为监测胃黏膜状态的手段。
二、胃癌早期预警指标-胃蛋白酶原(PG)检测
1.慢性萎缩性胃炎在胃黏膜癌变是重要的“过渡性事件”
胃癌是我国常见的恶性肿瘤之一,其病死率居各种恶性肿瘤之首,其早期诊断、早期治疗成为提高患者生存质量、降低病死率的唯一途径。目前诊断胃癌的主要方法是纤维胃镜和上消化道造影检查,其中胃镜被称为是确诊胃癌的“金标准”。
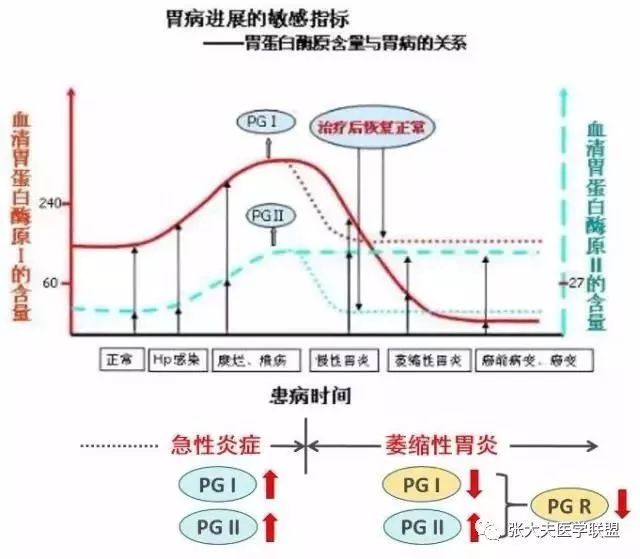
目前观点认为,部分萎缩是可以逆转的,而一旦进入肠化生后,就很难发生逆转。因此,急需要一种工具,能够敏锐地发现胃黏膜萎缩的情况。此时,胃蛋白酶原检测即发挥出强大的作用。
当胃底腺萎缩时,主细胞数量减少,PGⅠ水平下降;而由于分泌PGⅡ细胞较多,此时PGⅡ仍然可以维持高水平状态,此时PGⅠ/PGⅡ显著下降;当萎缩性胃炎伴有肠化生以及胃窦腺向胃体延伸,出现胃底腺假幽门腺化生时,PGⅡ水平升高更多,PGⅠ/PGⅡ进一步下降。因此PGⅠ水平降低是胃底腺黏膜萎缩的可靠标志,PGⅠ/PGⅡ侧面反映了胃底腺黏膜萎缩程度。
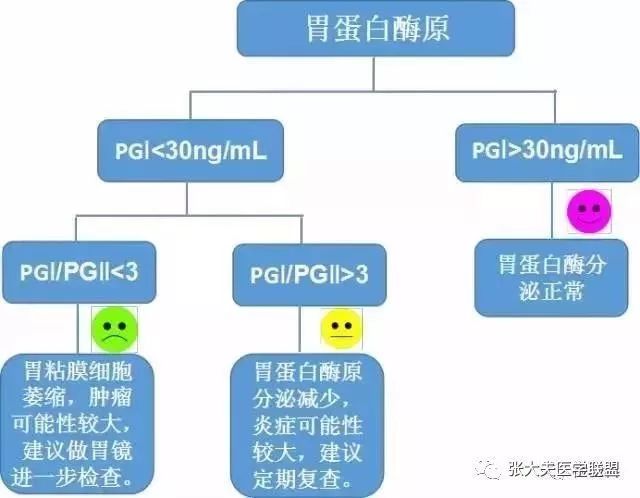
2.幽门螺杆菌感染是胃癌发展的始动因素
胃癌的发生是多因素共同作用的结果。胃癌发生的多步骤假说,即从慢性非萎缩性胃炎(旧称慢性浅表性胃炎)→萎缩性胃炎→肠化生→上皮内瘤变(旧称异型增生)→胃癌的病变过程已被普遍接受,而幽门螺杆菌(Hp)感染已成为最重要的始动因素,同时Hp感染目前也已经公认为是胃癌发生的独立危险因素。

因此,积极进行Hp检测,已经成为了防治胃癌的重要措施之一。Hp检测主要分为侵入性和非侵入性两大类手段,针对Hp阳性的感染人群,各大指南已达成共识,即Hp感染相关胃炎是一种感染性疾病,建议根除。
Hp感染也会显著影响血清PG水平,起始时,PGⅠ、PGⅡ均升高,PGⅡ升高的幅度更快,则PGⅠ/PGⅡ下降,且Hp感染病灶越大,PGⅠ/PGⅡ降低幅度越大。但是,胃蛋白酶原检测的结果缺乏特异性,对于判断Hp是否感染仍需接受专门的Hp检测。
三、胃蛋白酶原Ⅰ(PGⅠ)、胃蛋白酶原Ⅱ(PGⅡ)结果分析如下:
|
检测结果 |
可能原因 |
|
PGⅠ>70ng/mL或PGⅠ/Ⅱ>3 |
正常范围 |
|
PGⅠ<70ng/mL且PGⅠ/Ⅱ<3 |
萎缩性胃炎、胃癌肠上皮化生等高风险因素,建议立即胃镜检查 |
|
PGⅠ>240ng/mL |
首先检测Hp,确认是否是Hp感染,如排除Hp感染则可能为轻度胃溃疡,建议调整饮食,两周后复查 |
|
PGⅡ>13ng/mL |
首先检测Hp,确认是否是Hp感染,如排除Hp感染则可能为胃萎缩性胃炎,两周后复查 |
四、“胃蛋白酶原”检测结果误解说明:
误区一:假若体检时只测PGⅠ,近70%的结果在40~70ng/mL,表面看起来都低于70ng/mL,怀疑胃萎缩,但因未测PGⅡ及比值导致结果不好解释。当复测PGⅡ时比值90%以上都大于3,此类情况是因中国人群慢浅表性胃炎高发,属正常生理性胃酸分泌不足。
误区二:PG阳性就是“胃癌说”:阳性是代表胃癌高风险人群。PG项目是适用于体检早期简易筛查胃癌的项目,替代X光及超波筛查胃癌。主要意义不在诊断而在于早发现早预防。正常体检测15%PG阳性,PG阳性者罹患胃癌的高风险有1%~2%的胃癌早发现率。
误区三:只看重PGⅠ、PGⅡ的参考范围值的变化,不重视比值。因胃黏膜分泌PGⅠ受炎症攻击分泌变动幅度大(70~800ng/mL以上),PGⅡ分泌相对恒定。对比值>3时,PGⅠ增高程度确定胃病种类只能结合临床分析。对比值<3时建议进一步深度内镜检查或病理取材确证预警早期胃癌高风险,并且在近五年都要随访监测。因PG阳性者在当年无胃癌者后续5年的胃癌发病率有2%。
五、日本经验借鉴(“ABC”法+内镜筛查)
我们的邻国日本,同样作为胃癌高发国家,在早癌筛查方面却做得非常出色。他们早癌的筛查策略就紧紧抓住Hp感染及是否发生胃底腺萎缩这两项可控因素。
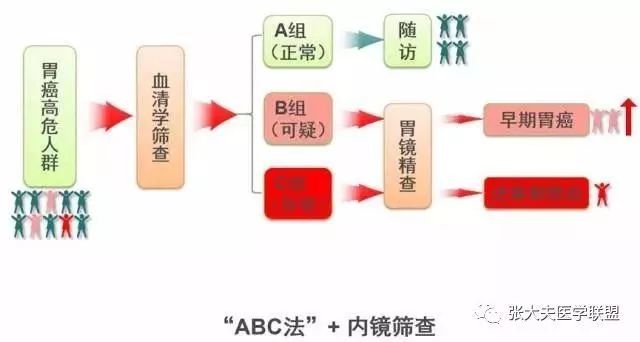
日本京都共识针对全民早癌筛查策略,作了如下推荐:首先针对Hp感染,京都共识针对Hp感染,强调“格杀勿论”,全民人人杀菌,根除Hp后,再进行PG的评估。将PGⅠ/ PGⅡ比值≤3.0,作为萎缩性胃炎的诊断临界值,并以此作为胃癌高危人群筛查的标准。
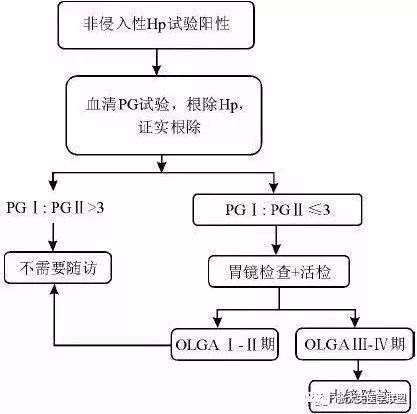
六、任重而道远-中国早癌筛查的策略:
中国人口基数大,同时胃癌发病率也居高不下,所以找到易行且精准有效的胃癌筛查手段势在必行。2017年《中国慢性胃炎共识意见》高度肯定了PG的价值,指南给出了如下推荐意见:血清胃蛋白酶原(PG)Ⅰ、Ⅱ以及促胃液素-17的检测可能有助于判断有无胃黏膜萎缩和程度。血清PGⅠ、PGⅡ、PGⅠ/ PGⅡ比值联合抗Hp抗体检测有助于风险分层管理。
而于2017年年底公布的《中国早期胃癌筛查流程专家共识意见》,在肯定血清PG价值的同时,进一步提出了新型胃癌筛查评分系统,其中高龄、男性、Hp抗体阳性、低胃蛋白酶原比值(PGR)、高血清胃泌素17(gastrin-17,G-17)水平作为胃癌的高危因子。

其中,G-17是中国指南新增项目。G-17是由胃窦G细胞合成和分泌的酰胺化胃泌素主要生理功能为刺激胃酸分泌、促进胃黏膜细胞增殖与分化。G-17是反映胃窦内分泌功能的敏感指标之一,可以提示胃窦黏膜萎缩状况或是否存在异常增殖,G-17本身在胃癌的发生、发展过程中也有促进作用。当血清G-17水平升高,可以提示存在胃癌发生风险。
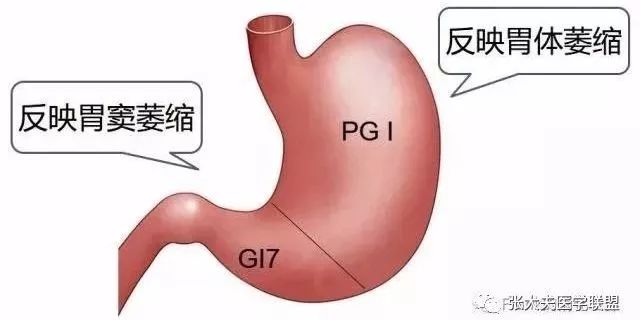
此外与京都共识不同的是,我国共识意见首次提出了适合我国人群的血清学检测临界值:即当PGR<3.89,G-17> 1.50pmol/L 时,胃癌的发生风险显著增高。而京都共识定义的PGR临界值为≤3。
针对积分的高低,指南将人群分为低危、中危、高危三组,并给出了筛查策略。
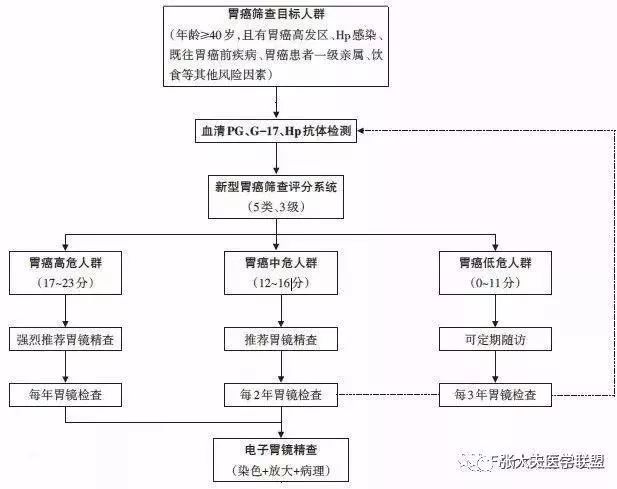
但同时,我们也应该看到中国指南的缺点,筛查人群为年龄≥40岁,且有胃癌高发区、Hp感染、既往胃癌前疾病、胃癌患者一级亲属、饮食等其他风险因素的人群。但目前胃癌发病年龄越来越提前,相信未来一定会进入全民普查阶段。
综上所述,血清PG联合Hp检测,有助于评估胃癌发生风险,可以作为普通人的常规胃癌筛查手段,但是,它并不能替代胃镜检查,针对高危人群,依然强烈推荐进行胃镜检查。

本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#胃蛋白酶原#
96
#蛋白酶#
82
#临床应用#
99