Cell Host Microbe:出乎意料的线粒体新作用:杀死细菌?!
2019-01-30 小通 生物通
密歇根大学医学院的免疫学家Mary O'Riordan在让小鼠巨噬细胞接触金黄色葡萄球菌时也发现了同样的问题,这说明这个过程似乎激活了细胞内质网中的特定应激途径,从而加速了ROS的产生。
这一研究结果代表了巨噬细胞抗菌防御的“新转折”
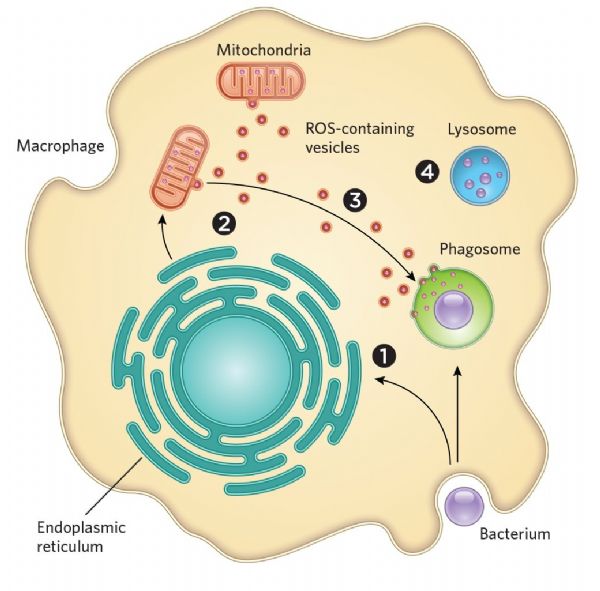
生物学教科书告诉我们,巨噬细胞吞噬细菌,将其内化于一种称为吞噬小体(phagosome,生物通译)的充满毒素的囊泡中,然后将细胞残余物运送到溶酶体中进行降解。但是具体来说,杀死微生物入侵者的过程要复杂得多,研究表明,其他细胞器如线粒体,也就是细胞中能量产生的主要部位,也参与这个过程。
这一出乎意料的研究发现公布在Cell Host Microbe杂志上。
2011年,科学家们发现了线粒体作用的一个新证据,当时研究人员在小鼠巨噬细胞线粒体中减少了活性氧(ROS)的生成,ROS是新陈代谢的副产物,也是具有高度破坏性的分子,结果他们发现免疫细胞杀灭细菌方面效果变得不明显了。
四年后,密歇根大学医学院的免疫学家Mary O'Riordan在让小鼠巨噬细胞接触金黄色葡萄球菌时也发现了同样的问题,这说明这个过程似乎激活了细胞内质网中的特定应激途径,从而加速了ROS的产生。
为了找出ROS的来源,O'Riordan和她的同事从小鼠中提取巨噬细胞,并使用CRISPR-Cas9切割编码IRE1α的基因,后者是内质网中的一种应激感应蛋白。
当研究人员让这些细胞接触金黄色葡萄球菌时,他们发现巨噬细胞线粒体中的ROS明显减少了,并且细胞杀死细菌的效果远低于未改变的巨噬细胞。然后研究小组使用荧光探针观测正常功能巨噬细胞中的ROS过氧化氢,发现了化合物从线粒体传播到吞噬小体的过程。
此外,实验也表明这种转运是通过从线粒体发芽,再穿梭到吞噬小体的囊泡发生的。如果缺乏Parkin(一种参与产生线粒体的囊泡的基因),那么巨噬细胞就无法胜任杀死金黄色葡萄球菌和其他两种类型微生物的功能了。
“我认为发生的是细菌发生了吞噬,信号发送出来,开启ER应激和线粒体ROS,它们很快将这些包装送到吞噬小体,”O'Riordan解释说。虽然线粒体主要功能是作为发电厂,“但实际上,细胞已经进化,它们会以多种不同的方式利用这些细胞器及其许多组成部分,”例如在过氧化物酶体在介导程序化细胞中死亡中的作用。
多伦多大学的细胞生物学家Greg Fairn(未参与这项研究)认为,这一研究结果代表了巨噬细胞抗菌防御的“新转折”。他指出,吞噬小体有自己的毒素和产生ROS的机器来杀死细菌,因此这一新发现的机制可能可以对抗更强韧,更具抗性的菌株。重新利用线粒体ROS来杀死病原体也许是具有潜力的新策略。
原始出处:Abuaita BH1, Schultz TL1, O'Riordan MX2. Mitochondria-derived vesicles deliver antimicrobial reactive oxygen species to control phagosome-localized Staphylococcus aureus. Cell Host Microbe. 2018 Nov 14;24(5):625-636.e5.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#新作用#
80
#Micro#
53
#CRO#
61
#CEL#
59
#Cell#
50