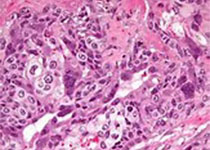
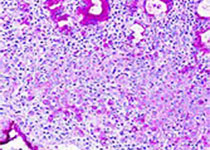
- 比较复杂,包括:遗传、激素、生殖、营养和环境等
- 家族性乳腺癌多数由单基因或多基因改变引起,其中最主要的是乳腺癌相关基因有BRCA1、BRCA2、TP53等
- 小叶原位癌(LCIS)归类良性病变从分期系统删除;
- 最大径1.0~1.5mm的浸润癌应记录为2.0mm,避免被归为微小浸润(microinvasive carcinomas)导致肿瘤分期低估;
- 新辅助治疗前SLN微转移灶增加cN1mi标准,删除pN0目录下pN0(i-)及pN0(mol-);
- 肯定CTC意义,临床晚期乳腺癌外周血CTC≥5个/7.5ml,临床早期乳腺癌外周血CTC≥1个/7.5ml提示预后不良,证据水平为Ⅱ级。

- 强调综合治疗,全程管理:生存期、生活质量、经济、毒性等
- 乳腺癌各期总的治疗原则
- 多学科参与:内科、外科、放疗、妇科、影像、病理、心理、社会、护理和姑息等
- 个体化治疗,尊重意愿

- 无论绝经前后,辅助化疗均能降低复发率和病死率,但绝经前患者获益更大
- 化疗特点:细胞毒药物;效率高、起效快、不良反应大
- 适应症
- 常用化疗药物

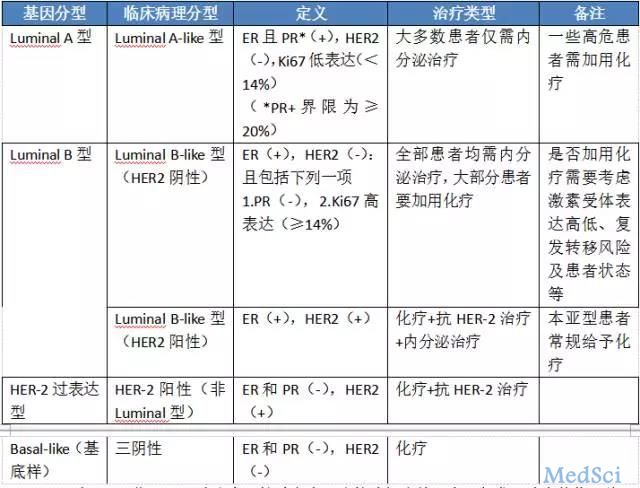
- 诊断时复发风险较高
- 更年轻的患者
- 不存在威胁生命的合并疾病
- 耐受性较好
- 患者选择
- 晚期复发的生物标志物
- 第一个内分泌靶向药物
- 辅助内分泌治疗的金标准、首选推荐
- 5年标准治疗到10年延长治疗:5年SERM治疗是绝经前激素受体阳性患者的内分泌辅助治疗金标准;而患者的依从性是影响疗效的真正挑战,影响依从性最主要是因为药物不良反应
- 显着降低乳腺癌患者复发和死亡风险度
- 对于HER-2阳性患者推荐曲妥珠单抗靶向辅助治疗1年
- 3%-10%的乳腺癌初次诊断即为晚期乳腺癌
- 早期患者中1/3将发展为晚期乳腺癌
- 晚期乳腺癌中位生存期2-3年,5年生存率约20%
- 晚期乳腺癌不可治愈
- 治疗目标:缓解症状、提高质量、延长生存
- 对于病情发展迅速,肝、肺等出现广泛的内脏转移,术后至复发转移时间较短者,ER和PR阴性的晚期乳腺癌是全身化疗的适应证
- 对于病变发展相对缓慢,骨和软组织转移,术后至复发转移时间较长者,ER和(或)PR阳性的晚期乳腺癌是内分泌治疗的适应证
- 优先考虑蒽环和/或紫杉类药物
- 蒽环类耐药或蒽环类药物达到累积剂量或蒽环类心脏毒性:优选紫杉类方案
- 紫杉类辅助化疗结束后1年以上:仍可考虑再次使用,但建议优先考虑之前未使用过的药物
- 使用过蒽环及紫杉类:优先考虑卡培他滨、长春瑞滨、吉西他滨等
- 寻找毒性较低、使用方便的化疗药物维持是乳腺癌维持治疗的发展方向
- 晚期乳腺癌的无特定的化疗周期;对于年轻、疗效好的患者推荐延长化疗周期以获得最佳化疗;对于毒性反应较大或不愿继续化疗者应及时停止
- 化疗的持续时间:一线化疗持续时间长能够延长疾病控制时间,并可能延长总生存
- 联合化疗有效之后的单药维持治疗:选用原方案中的一个药物进行维持
- HR阳性乳腺癌化疗有效之后,采用化疗或内分泌维持都是合理的选择
- 节拍化疗:卡培他滨、环磷酰胺、甲氨蝶呤、VP16等
- 化疗是转移性三阴乳腺癌的唯一治疗手段
- 治疗目标是延长生存、减轻症状和提高生活质量
- 三阴性晚期乳腺癌,特别是年轻患者,建议行BRCA基因检测
- 三阴性乳腺癌的中国研究结果表明:顺铂联合多西他赛、顺铂联合吉西他滨的方案优于非铂类两药联合方案
- 转移性三阴乳腺癌的化疗尚无统一标准的方案
- 应根据肿瘤负荷、患者全身状态和治疗意愿、既往治疗毒性反应等选择最为合理的、个体化的化疗方案
- 贝伐珠单抗:PFS有限的获益,OS没有延长,应慎重选择患者
- 内分泌治疗与化疗不同时应用,因为不能提高生存
- 内分泌治疗可作为化疗结束后的维持治疗
- 芳香化酶抑制剂(AI)
- 非甾体类:阿那曲唑、来曲唑
- 甾体类:依西美坦
- 雌激素受体调节剂(SERMs)
- 他莫昔芬、托瑞米芬、氟维司群
- 其它:孕激素类、雄激素、雌激素
- 减少雌激素产生
- 阻断雌激素受体
- 可能的情况下要早期开始应用内分泌治疗
- 化疗和内分泌治疗同样可能有效的情况下,应优先使用内分泌治疗
- 内分泌治疗进展的情况下,还可考虑内分泌治疗
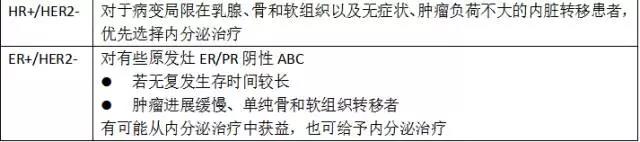

- 在内分泌治疗期间,应每2-3月评估一次疗效
- 原发性耐药
- 获得性耐药
- 对于既往内分泌治疗有效的患者(TTP>6个月),后续内分泌治疗仍然有可能控制肿瘤,疾病进展后可以换用不同作用机制的其它内分泌药物治疗
- 连续三线内分泌治疗后无效通常提示内分泌耐药,应该换用细胞毒药物治疗
- 进展后的药物选择
- HER2与EGFR成员形成二聚体,介导细胞生长信号通路
- HER2诱发肿瘤的机制
- HER2乳腺癌预后差,生存期显着缩短
- 复发转移性乳腺癌患者应尽量再次检测HER2,以明确复发转移灶的HER2状态
- 对病情发展不符合HER2状态特点的患者,更应重新检测HER2状态,即可以使原发病灶,也可以是复发转移灶
- 当原发灶和转移灶检测结果不一致时:只要有一次HR和(或)HER2阳性,就应推荐相应的内分泌治疗和(或)抗HER2治疗
- 对于HER2阳性/HR阳性晚期乳腺癌患者,优先考虑抗HER2治疗联合化疗。部分不适合化疗或进展缓慢的患者可以考虑抗HER2治疗联合AI治疗
- 推荐对停用曲妥珠单抗至复发间隔时间≤12个月患者可选用二线抗HER-2方案治疗;而对停用曲妥珠单抗至复发间隔时间>12个月以上的患者,仍可选择曲妥珠单抗或曲妥珠单抗和帕妥珠单抗联合细胞毒药物作为一线抗HER-2治疗方案
- HER-2阳性晚期乳腺癌患者首选曲妥珠单抗联合帕妥珠单抗双靶向治疗,除了联合紫杉醇、多西他赛外,也可联合长春瑞滨治疗
- 在不能获取帕妥珠单抗时,曲妥珠单抗可以与紫杉类、长春瑞滨、卡培他滨、脂质体蒽环、吉西他滨等药联合用药或联合节拍化疗
- 抗HER2治疗失败后的患者,持续HER2通路的抑制可以带来生存获益,无论是抗HER2治疗联合化疗、双靶向治疗或T-DM1,应继续抗HER2治疗
- T-DM1是曲妥珠单抗治疗失败后的首选治疗方案
- 在无法获得T-DM1时可选择其它二线治疗方案,包括继续曲妥珠单抗联合另一种细胞 毒性药物;拉帕替尼联合卡培他滨和曲妥珠单抗联合拉帕替尼双靶向都是可选方案
- 一线治疗中,无论是否接受过曲妥珠单抗治疗的HER2+晚期乳腺癌,使用曲妥珠单抗联合化疗疗效均优于拉帕替尼联合化疗
- 另有研究显示:mTOR抑制剂依维莫司联合曲妥珠单抗对于既往接受曲妥珠单抗的晚期患者有一定的生存获益可作为二线治疗的选择
- 以曲妥珠单抗为主的双靶向治疗优于单靶向治疗
- 小分子TKI并不优于曲妥珠单抗
- 患者接受曲妥珠单抗联合化疗时,根据肿瘤疗效和患者对化疗的耐受程度,推荐化疗应持续至少6-8周期
- 脑转移诊断确立后,需要根据患者一般情况、颅外病灶的控制情况及脑转移灶的数目和部位选择合理的局部治疗和支持治疗,并在此基础上根据原发肿瘤的分子分型和既往抗肿瘤全身治疗情况选择合理的全身治疗
- 对于HER-2阳性乳腺癌患者,当脑转移是唯一转移部位时,局部治疗基础上加化疗是否能够改变疾病进展尚不清楚。推荐如已停止抗HER-2治疗,应该再次抗HER-2治疗
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言