Eur J Radiol:放射组学在胃癌微卫星不稳定状态及其预后预测中的应用
2023-09-10 shaosai MedSci原创 发表于上海
最近,放射组学具有基于图像(经济上负责、快速)和病人可接受(非侵入性)的综合优势,已成为GC诊断的有力工具。
胃癌(GC)是一个全球公认的健康问题,就癌症发病率而言,GC是第五大最常被诊断的恶性肿瘤,就癌症死亡率而言,GC排在第四位。最近的证据表明,胃癌的分子高度多样化,随后提出了许多分类系统试图推动确定潜在的治疗目标并打破一刀切的治疗方式。尽管分子技术和分析各不相同,但其中三个工作组都将微卫星不稳定性(MSI)确定为其亚型之一。更重要的是,随着五项临床试验数据的公布,美国食品和药物管理局和日本药品和医疗器械管理局相继批准pembrolizumab用于治疗MSI高(MSI-H)的实体肿瘤,包括GC。美国国家综合癌症网络(NCCN)指南、欧洲肿瘤内科学会、日本临床肿瘤学会、日本肿瘤内科学会、美国临床肿瘤学会和中国临床肿瘤学会也强调了pembrolizumab在MSI-H GC患者中的价值。值得注意的是,最新的NCCN指南版本推荐增加Dostarlimab-gxly作为MSI-H GCs的治疗选择。因此,明确MSI在GCs中的地位是至关重要的,特别是对指导患者的免疫治疗。
目前,免疫组化(IHC)、聚合酶链反应(PCR)和新型的下一代测序(NGS)可用于确定MSI状态 。然而,这些方法有几个固有的缺点,如侵入性、耗时和昂贵的性质。这些挑战加强了临床对一个非侵入性的、具有成本效益工具的需求。最近,放射组学具有基于图像(经济上负责、快速)和病人可接受(非侵入性)的综合优势,已成为GC诊断的有力工具。同时,参考放射组学特征的定量事实有助于揭示肿瘤的异质性,一些研究也强调了放射组学在结直肠癌MSI状态中的作用。

近日,发表在Eur J Radiol杂志的一项研究通过开发和外部验证基于CT的MSI诊断模型评估了基于CT的放射组学在识别GC的MSI状态方面的潜在价值,并随后探索了该模型对患者预后的潜在作用。
本项研究从一个中心和一个公共数据库中回顾性地招募了396名有治疗前CT图像的GC患者,并将他们分为原始队列(n = 356)和外部验证队列(n = 40)。使用SMOTE算法生成平衡的训练队列(n = 192),并构建了独立的放射组学模型、临床模型和放射组学-诊所联合模型来确定MSI状态。通过AUC、校准、决策曲线分析和Kaplan-Meier曲线分析,分别评估了模型的分辨力、校准、临床实用性和预后意义。
在所有队列中,由临床和基于CT定量的 "Radscore "得出的放射组学-诊所联合模型对MSI状态表现出最好的鉴别能力,在训练队列中AUC为0.836(95%CI,0.780-0.893),在外部验证队列中为0.834(95%CI,0.688-0.981),在原队列中为0.750(95%CI,0.682-0.819)。同时,与任何独立的模型相比,联合模型表现出良好的适应性、更高的临床净效益以及显著的正向综合辨别力的提高。虽然没有显示出明显的基于总生存期或无进展生存期的风险分层能力(P>0.05)。
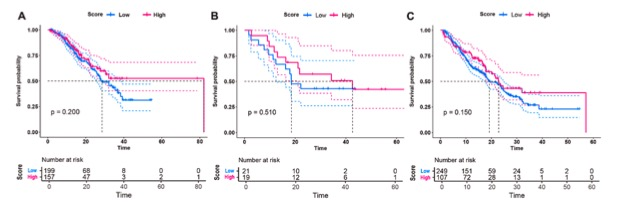
图 MSI诊断模型的风险分层性能。(A) 原始队列的总生存分层。(B) 外部验证队列中的总体生存分层。(C) 原始队列中的无进展生存分层
本项研究表明,放射组学-诊所联合模型是GC中MSI状态的一个潜在的非侵入性生物标志物,有助于临床决策,但可提供的预后能力有限。
原始出处:
Huiping Zhao,Jianbo Gao,Biaosheng Bai,et al.Development and external validation of a non-invasive imaging biomarker to estimate the microsatellite instability status of gastric cancer and its prognostic value: The combination of clinical and quantitative CT-imaging features.DOI:10.1016/j.ejrad.2023.110719
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言