Cell:母乳喂养新益处!让新生儿对有益肠道细菌产生耐受性
2016-05-07 生物谷 不详
从新生儿出生那一刻起,多种多样的有助消化和增强免疫力的微生物就定植在他们的肠道中。但是人们并不清楚新生儿免疫系统如何学会耐受这些外来物种中的绝大多数,而不是将它们作为不友好的入侵者进行攻击。 在一项针对小鼠的新研究中,来自美国加州大学伯克利分校等机构的研究人员揭示出从母乳中获得的免疫球蛋白G(IgG)抗体有助抑制在生命早期对新获得的微生物产生的免疫反应。相关研究结果发表在2016年5月5
从新生儿出生那一刻起,多种多样的有助消化和增强免疫力的微生物就定植在他们的肠道中。但是人们并不清楚新生儿免疫系统如何学会耐受这些外来物种中的绝大多数,而不是将它们作为不友好的入侵者进行攻击。
在一项针对小鼠的新研究中,来自美国加州大学伯克利分校等机构的研究人员揭示出从母乳中获得的免疫球蛋白G(IgG)抗体有助抑制在生命早期对新获得的微生物产生的免疫反应。相关研究结果发表在2016年5月5日那期Cell期刊上,论文标题为“Maternal IgG and IgA Antibodies Dampen Mucosal T Helper Cell Responses in Early Life”。
降低对有益肠道微生物耐受性的异常免疫反应能够导致炎症性肠病,如溃疡性结肠炎和克罗恩病(Crohn's disease)。之前的研究提示着母乳提供的免疫球蛋白A(IgA)抗体主要负责在生命早期教授新生小鼠免疫系统对有益肠道微生物产生耐受性。相反,从母体获得的IgG大多被认为在保护新生小鼠免受一系列病原体感染中发挥着至关重要的作用。
这项新的研究挑战了这一常规看法,揭示出来自母乳的IgG抗体在新生小鼠体内对多种多样的肠道微生物建立起合适的免疫反应。论文第一作者、加州大学伯克利分校科学家Meghan Koch说,“这些发现证实针对肠道菌群的抗体免疫反应要比之前所认为的更加复杂,而且揭示出母体IgG抗体在生命早期协助建立合适的免疫反应中具有更加广泛的功能。”
研究人员发现健康小鼠产生的IgG抗体要比IgA抗体识别更加广泛的微生物,这提示着IgG抗体扩大免疫系统对肠道微生物的识别。进一步实验揭示出IgG抗体早在小鼠两周大时就存在于它们体内,而且是从出生后而不是在子宫中从母体中获得的。这些IgG抗体在抑制针对新生小鼠体内的肠道微生物产生的免疫反应中发挥着关键性作用。
为了扩大这项研究,研究人员计划研究IgG抗体如何针对肠道微生物建立适当的免疫反应。他们也将研究IgG抗体在长期肠道健康中的作用。比如,接受抗体缺乏的母体母乳喂食的新生小鼠可能更容易遭受肠道炎症,不过是否真是这种情形还言之过早。
论文通信作者、加州大学伯克利分校科学家Gregory Barton说,“这些发现提示着对人体内的抗体免疫反应进行分析可能有助于描述针对肠道微生物产生的免疫反应。这种信息可能能够被用来评估一个人患上炎症性肠病的风险和在疾病早期制定治疗性干预。”
Maternal IgG and IgA Antibodies Dampen Mucosal T Helper Cell Responses in Early Life
doi:10.1016/j.cell.2016.04.055
Meghan A. Koch, Gabrielle L. Reiner2, Kyler A. Lugo3, Lieselotte S.M. Kreuk, Alison G. Stanbery, Eduard Ansaldo, Thaddeus D. Seher4, William B. Ludington, Gregory M. Barton
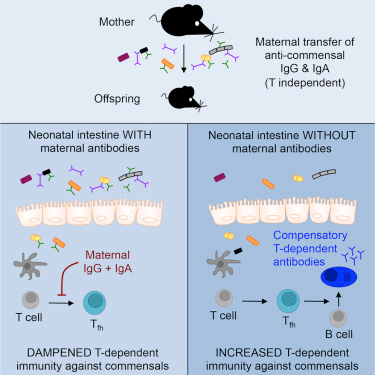
To maintain a symbiotic relationship between the host and its resident intestinal microbiota, appropriate mucosal T cell responses to commensal antigens must be established. Mice acquire both IgG and IgA maternally; the former has primarily been implicated in passive immunity to pathogens while the latter mediates host-commensal mutualism. Here, we report the surprising observation that mice generate T cell-independent and largely Toll-like receptor (TLR)-dependent IgG2b and IgG3 antibody responses against their gut microbiota. We demonstrate that maternal acquisition of these antibodies dampens mucosal T follicular helper responses and subsequent germinal center B cell responses following birth. This work reveals a feedback loop whereby T cell-independent, TLR-dependent antibodies limit mucosal adaptive immune responses to newly acquired commensal antigens and uncovers a broader function for maternal IgG.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#喂养#
86
#CEL#
62
#Cell#
117
还是母乳喂养好…
144
#母乳#
80
#肠道细菌#
85
#耐受性#
73
做一个队列分析?
155
母乳肯定好
151
学习啦!
167