临床医生为什么要用数据库开展临床研究?
2015-10-30 MedSci MedSci原创
临床科研是每一位医生的必争之地,然而也是最痛的痛点之一。如何设计临床科研,如何积累有价值的科研数据,如何将收集的数据转换成科研的成果,并且将科研成果转换为公众健康意识是永恒的话题。 然而,如何积累有价值的科研数据更多的是执行层面的部分,包括如何设计CRFs、如何构造电子数据采集系统(EDC)、如何检查数据质量、清理和分析数据、整合数据库,也包括对数据录入员的管理等。串接这两部分的核心就是CR
临床科研是每一位医生的必需要技能(王辰院士:医生是天然的研究者),如何设计临床科研,如何积累有价值的科研数据,如何将收集的数据转换成科研的成果,是永恒的话题。
使用EDC之后,site可以在第一时间直接录入数据到数据库里,简单的逻辑错误会直接由数据库的电子检查跳出query,DM在清理数据时还有query就直接加在数据库中,site直接在EDC系统里解决query。CRA去做SDV时比对的就是电子数据和原始病历化验单。这样极大节约了工作量,提高工作效率。
其一:CRFs设计难度大,且耗时,过程容易出错。
CRFs的设计是临床科研项目的核心,根据某一研究目的确定需要收集的信息并且规定收集的整个标准流程。除了必要的科研想法和试验设计外,一些方法是可以降低设计CRFs难度的。
其二:数据收集成本高
每一个科研项目常有不同的CRFs设计,变量名或收集的流程可能存在很大的差异。
数据录入员进行数据收集前,需要耗时培训和长期适应才能保证对CRFs内问题的了解。这样无形增了科研项目执行的培训成本;另外,也容易出现理解错误而导致不合适的执行行为;
其三:各数据库间相互不通用,数据交换存在困难
创建CRFs时没有统一标准;CRFs间使用不同的标准,导致后期无法合并使用。正因为数据间缺少一致性而导致了数据的分散而不可用,这是非常可惜的事情。
其四:数据管理与数据分析成本高
同样是因为CRFs设计规范的差异,包括变量名、收集方式等,导致数据分析员分析每一个项目时都需要重新熟悉数据数据库,甚至重新进行编码;如果需要进行数据库合并更是难上加难。
数据库必须保证一致性!目前国际上要求必需遵循CDISC规范,进行统一编码。
1. 统一变量名(数据编码):编码的数据便于数据录入,帮助统计师对数据进行解释和分析;
要求数据的一致性:包括日期、小数点、测量单位、选项设置(不明/不适用/不可用/未实施)等格式一致性;
2.通用标识性变量和时间变量应该出现在CRFs或数据采集系统,至少包括方案编号、受试者ID、中心ID和访视日期;也可添加申办方ID、受试者姓名缩写、CRF版本号等信息;对CRF内的问题进行详细说明,保证收集内容理解的一致性;根据统一标准进行CRF设计。
保证CRFs一致性的好处:
1.最大化的重复利用产生的数据、CRFs和电子数据库
同一治疗领域,科研目的也许千差万别,分析角度也大相径庭;但CRFs的内容却有很多可以重复利用的部分;如果保持所有CRFs具有相同的编码系统,统一的格式,将大大减少制作CRFs的时间;提高首次填写的依从性和数据质量;
2.可使数据元的再利用成为可能,减少系统间的重复作业,并改善数据的可靠性,同时收集到的数据可以相互匹配轻松扩大数据库信息量;
3.降低统计分析的难度
4. 促进数据共享与交换。尤其是多中心数据之间的合并,尤其如此。
MedSci为大家量身定做一套标准的数据库管理系统,方便大家规范开展临床研究,关键一切都是免费。有需要,可以联系MedSci。
为什么说它是规范的呢?因为它遵循了CDISC规范,包括其中的“CDASH”。
Clinical Data Acquisition Standards Harmonization (CDASH)定义了临床数据收集的基本标准,并且开发了一些列新药研发临床试验的CRFs基本内容标准(即,定义了最常用的变量库)。
一、CDASH提供了设计数据收集系统的方法学
Clinical Data Acquisition Standards Harmonization(CDASH)定义了临床数据收集的基本标准,并且开发了一些列新药研发临床试验的CRFs基本内容标准(即,定义了最常用的变量库)。
先附上CDASH推荐的CRFs制作流程:
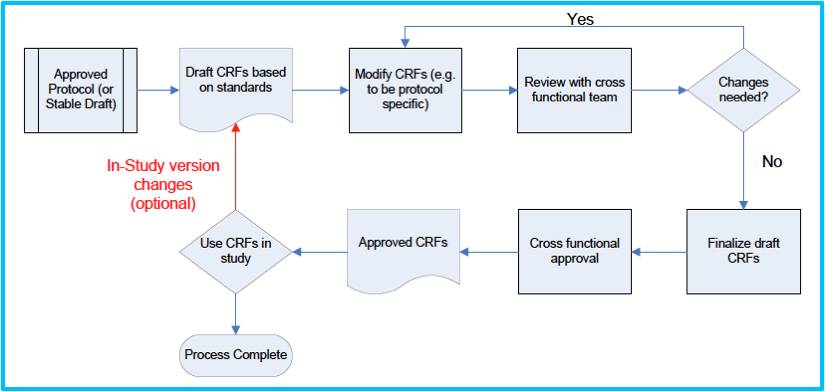
(引用自:CDASH standard v1.1, 2011)
从上图可以看出,CRFs制作绝对不是一个人的事情,而是整个临床科研过程中所有角色都应该参与撰写、修改、测试和确认的过程。
整个CRFs制作流程必须严格控制,正如上图所示。当研究方案通过后,就进入草拟CRFs阶段。需要注意:
1. 仅采集必要的数据:仅采集将用于分析的数据和避免冗余数据采集或过度采集
-
采集的变量并不是越多越好,因为数据的质量和数据量成反比,但收集成本和时间与数据量成正比。同时,从伦理上来说,也应该把控数据采集的量。比如,过度采集数据,就会对受试者身体造成负担,例如药代动力学数据;
2. 采集的数据应该与统计分析计划相关:根据统计分析计划,保证所有分析涉及的变量以符合统计要求的方式被合理收集;
3. 数据采集标准化:使用CDASH数据标准。重点说一说数据库编码问题:
(1)CRFs内的问题名建议使用CDSIC受控术语(CDSIC Controlled Terminology)。比如,twice per day=BID,Diastolic Blood Pressure=DBP等。受控术语列表下载链接:http://dwz.cn/26H7Km;如果在列表中没有,尽量使用列表中的变量名,或根据实验目的创建新的变量名,但必须保证在同一组织内使用统一标准;
(2)同一研究机构内所有科研项目的CRFs使用统一变量名;
4. 使用清晰简洁的问题名、提示和说明,保证CRFs内的问题和收集说明不会引起误导。比如,使用标准日期格式(dd/mm/yyyy)、指明小数点应记录的位数、测量单位、设置“不明/不适用/不可用/未实施”选项,如果数据可以从其他问题延伸而来则不必要收集,使用合理的跳转关系避免混淆等;
5. 每一个问题都应该有独立的操作说明,以免需要附加额外的说明文档进行说明;
6. 设置数据清理的提示语:数据库应该包含一些提示是否完成某些检查的问题。比如:“否/是-评价是否完成” 优于 “勾选是否未实施”:因为“否/是-评价是否 完成”可以得到完全的信息,然而“勾选是否未实施”,如果用户未选择不能确定是做了,还是漏了;
7. 避免“自由文本”,因为他需要编码后才能分析;因为自由文本会给后续统计分析带来很大困难。
8. 强烈建议使用电子数据采集系统进行数据收集,可以加快数据分析过程,项目管理和统计检查。检查包括计算机核查和人工核查,稽查几个步骤,以最大可能减少错误。一旦开始数据收集后,除不可抗拒因素外,不建议修改CRFs。因为一旦修改,可能会导致前后数据库格式不统一。
二、充分利用CDASH中已经储备的CRF模版,简化模板编制
CDASH根据常用的数据收集的类型进行归纳总结,提供了非常完备的模版库供我们参考。
模版涉及如下方面:


尽管这是为企业新药研发而设计的,但在临床研究中都可以参考,非常有价值。
举一个例子说明:
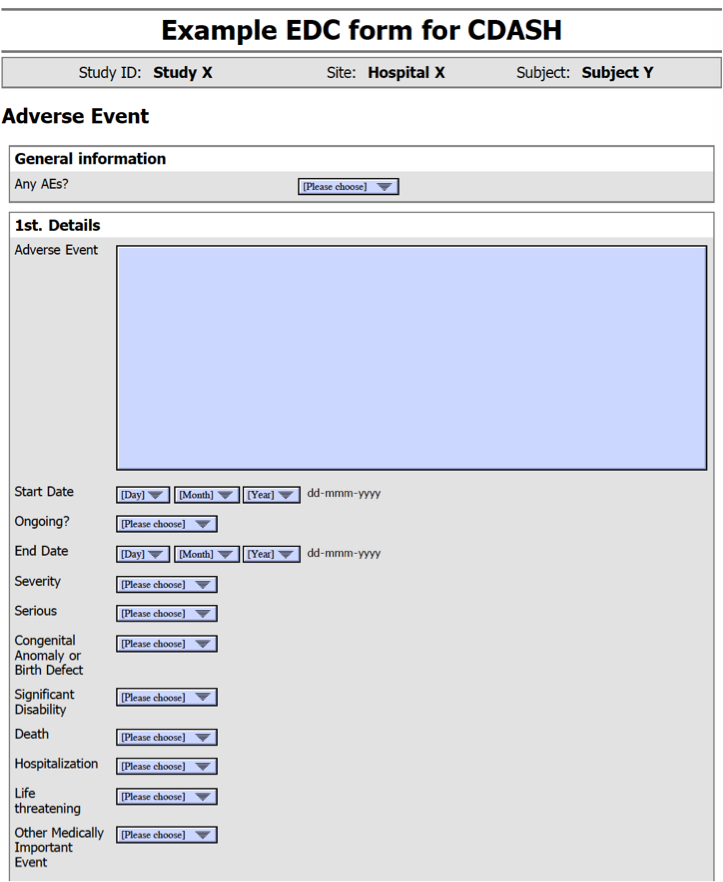
这是一个来自CDASH官网的eCRF的例子,并且提示常规需要收集的变量包括:
-
AETERM-不良事件名称
-
AESTDAT-不良事件发生日期
-
AESTTIM-不良事件发生时间
-
AEENDAT-不良事件缓解日期
-
AEENTIM-不良事件缓解时间
-
AEREL-与试验药物的关系
-
AEACN-措施记录
-
AEACNYN-采取措施(是/否)
-
AEOUT-不良事件结局
-
AESEV-严重程度
-
AETOXGR-毒性级别
-
AESER-严重不良反应事件SAE
-
AESAEDAT-报告严重不良反应事件日期
-
AESCONG-认知异常或出生缺陷
-
AESDISAB-致残
-
AESDTH-致死
-
ASSHOSP-导致住院
-
AESLIFE-生命受到威胁
-
AESMIE-其他医学重要事件
-
AEDRYN-因不良事件退出试验(是/否)
说明:
其中中文之前的编号的规律,简略说域名(domain)+变量缩写。比如,AE代表不良反应域,TERM代表变量名称。大部分的变量名CDSIC已经做了规定,至于如何创建CDSIC没有包含的变量名,以及如何设计和理解数据库导出格式等内容。除此之外,一般来说,域由两个字符限定,而变量缩写不要超过6个字符,合计在8个字符以内。字符缩写后期由一个“变量字典”进行识别。
总之,CDASH就是我们一个很好的制作CRFs的开始。他给我们提供了很多CRFs常用收集的数据模版,帮助我们规范CRFs的制作和使用规范,大大降低制作CRFs的难度,也为后期数据分析奠定基础。
不过,作为临床医生发起的小型临床研究,也需要尽量遵循这些规范,包括CDISC规范和HL7规范,可以实现后期的统计分析方便,以及数据交换的便捷性。
三、注册数据库研究中EDC使用
注册数据库研究与经典的药厂主导的RCT研究不同,它是真实世界的研究,临床医生为主导,因此,临床医生往往并没有大量时间录入数据。一般来说,一个标准的EDC环境下,录入单个患者的数据需要2个小时左右,因此,使用EDC数据库的情况下,往往也需要专门的机构来完成,主要是CRO公司,临床医生几乎无法承担这个任务。
但是注册数据库的主体是临床医生本身,因此,还要考虑EDC的便捷性。以及如何符合真实世界研究情况下的EDC。
真实世界下的EDC,也同样在遵循CDISC规范,遵循规范,可以有效开展临床研究,尤其是注册数据库的研究,为今后的长期工作打下良好的基础和铺垫。但是,需要对上述规范进行大量简化,才有可能真正在临床上使用。
MedSci提供的数据库系统,具备上述功能,可以大大减少录入的工作量,而且方便采用手机拍照为一体的方式进行,允许事后录入,极大方便临床医生开展的注册数据库研究。
一般来说,CRFs建设完毕后,录入一个患者的数据控制在10-20分钟以内,极大减少了必要的工作量,使得临床医生使用EDC成为可能。
而且,数据收集完毕,MedSci还能提供全面的统计服务(MedSci 医学统计服务,让临床科研得心应手),帮助大家无忧做科研工作。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












学习了谢谢作者分享!
91
看完后有些迷糊,到底我们临床医生应该怎么做?能否给个具体的例子?
193
#临床医生#
52
收藏了这个感觉不错
139
赞
189
赞
144