多篇文章阐明肠道微生物与机体健康的密切关联
2017-02-24 生物谷 生物谷
肠道微生物也就是我们通常所说的“肠道菌群”,机体中的肠道微生物数量超过自身细胞的10倍以上,而肠道微生物在机体消化、营养代谢、自身发育、免疫及疾病的产生等方面都扮演着重要角色,近年来全球科学家都将目光转移到研究肠道微生物上,而且很多研究结果都表明肠道微生物和多种疾病发病直接相关,比如癌症、肥胖、神经变性疾病等;本文中小编就盘点了一些重磅级文章来阐明肠道微生物和人类机体健康的密切关联,分
肠道微生物也就是我们通常所说的“肠道菌群”,机体中的肠道微生物数量超过自身细胞的10倍以上,而肠道微生物在机体消化、营养代谢、自身发育、免疫及疾病的产生等方面都扮演着重要角色,近年来全球科学家都将目光转移到研究肠道微生物上,而且很多研究结果都表明肠道微生物和多种疾病发病直接相关,比如癌症、肥胖、神经变性疾病等;本文中小编就盘点了一些重磅级文章来阐明肠道微生物和人类机体健康的密切关联,分享给各位!
【1】Cell Host Microbe:科学家阐明驱动肠道菌群失衡及炎症发生的分子机制
doi:10.1016/j.chom.2017.01.005
日前,一项刊登在国际杂志Cell Host & Microbe上的研究报告中,来自德州大学西南医学中心(UT Southwestern Medical Center)的科学家通过研究揭开了在炎性疾病发病过程中干扰肠道细菌平衡背后的分子途径。
研究者Sebastian Winter教授指出,深入理解这些途径或许能够帮助我们开发预防或治疗多种疾病的新型策略,比如炎性肠病(IBD)、特定的胃肠道感染以及结直肠癌等。目前在美国有超过100万人都患有炎性肠病,炎性肠病是一种慢性、长期的肠道炎性疾病,目前并没有有效的治疗和预防措施。
本文研究中研究人员就解释了肠道炎性发生期间肠道改变背后存在的关键机制,研究者表示,肠道炎症和肠道从细菌中获取的营养物质的改变直接相关,健康人的肠道中聚集着多种微生物群落,肠道细菌细胞的数量大约是人体细胞数量的10倍,在一个人一生的大部分时间里,机体的微生物群落都会帮助促进消化,保护机体免于感染或者调节机体健康免疫系统的发育。
doi:10.1016/j.cell.2016.11.018
最近一项研究似乎改变了我们长久以来对帕金森症发病的固有观念。
这项研究认为,帕金森症的病发并不是起始于大脑,而是与肠道微生物有关。这一观点能够解释为什么帕金森症患者会首先出现便秘的症状,十几年之后才会进而产生其它并发症。
帕金森症经常与颤动,肢体僵硬,运动不便等相关联,而主要原因是大脑内部的关键神经元发生了损伤。
尽管目前有一些能够针对神经退行性疾病的治疗手段,但并没有完全预防或治疗的效果,而且研究者们至今也不清楚该疾病的发生与恶化的分子机制。
【3】Cell:首次发现肠道微生物运动或会影响宿主的昼夜节律
doi:10.1016/j.cell.2016.11.003
甚至是肠道微生物也有着自己的生活规律,就好像时钟一样,它们会在部分肠道粘膜组织中开始每天的生活,向左或向右移动几微米,随后在回到原来的位置,日前一项刊登于国际杂志Cell上的研究报告中,来自魏茨曼科学研究学院的研究人员通过对小鼠进行研究发现,肠道微生物定期的运动或许会通过将肠道组织暴露于不同微生物或一些代谢产物中,从而影响宿主的昼夜节律。
研究者Eran Elinav说道,这项研究揭示了原核生物和真核生物,以及哺乳动物有机体和寄生在宿主体内的微生物菌群之间行为的互联机制,这些群体之间能够发生相互作用并且被彼此互相影响。此前研究中研究者发现,我们机体的生物钟能够同机体微生物菌群的生物钟协同工作,而且干扰小鼠机体的睡眠模式并且给其多次喂食就能够诱导小鼠机体肠道微生物菌群的行为改变。
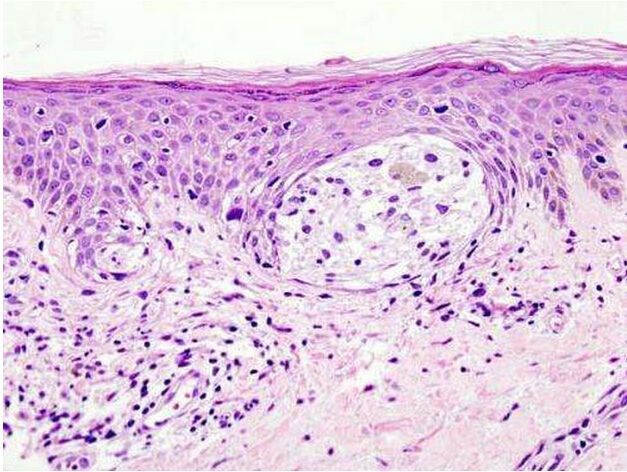
【4】强大的肠道菌群!竟然影响黑色素瘤病人对免疫治疗药物的应答
新闻阅读:Gut microbes linked to immunotherapy response in melanoma patients
在利物浦举办的国家癌症研究所(NCRI)癌症会议上,德克萨斯大学安德森癌症中心的科学家介绍了他们的一项最新发现:对于癌细胞已经扩散的恶性黑色素瘤病人来说,如果他们的肠道细菌多样性更加丰富,他们对免疫治疗产生应答的可能性会更大。
参与该研究的科学家们共分析了超过200张嘴和100份肠道菌群样本,这些样本都来自晚期黑色素瘤患者。他们发现对免疫治疗产生应答的癌症病人其肠道中的细菌多样性也更加丰富,他们还发现了在应答者和不应答者之间存在显著差异的细菌类型。病人的口腔细菌类型并没有差异。
在小鼠上进行的一些早期研究已经发现改变肠道细菌可以提高对免疫治疗的应答情况,但这是首次在病人体内研究这两者之间的关联。
这项研究表明在进行免疫治疗之前通过给予抗生素,益生菌或者粪便移植改变肠道菌群能够增加免疫治疗药物的效果,这些新药目前已经用于治疗几种不同类型的癌症。但是这还需要进行更进一步的临床试验验证。
DOI:10.1016/j.cell.2016.10.020
由美国麻省总医院、MIT布罗德研究所、哈佛大学和荷兰两个医学中心德研究人员进行的一项关于阐述健康人体内肠道菌群差异如何影响免疫应答的最新研究发表在国际学术期刊Cell上。同期发表的还有另外两篇关于基因和环境如何影响免疫应答的研究。这些研究是人类功能基因组学计划(HFGP)的一部分。
我们都知道有些人比其他人更易受到感染;有些人会患自身免疫疾病,而其他人却不会。研究人员希望通过研究发现基因,环境因素以及肠道菌群如何影响免疫系统,如何影响人们对疾病的易感性以及如何影响免疫系统对不同病原体的应答。
在这项关于肠道菌群与免疫应答关系的研究中,研究人员分析了500名健康参与者的血液和粪便样本,希望找到对病原体免疫应答的个体差异,肠道菌群的差异以及这两个因素之间如何产生相互影响。来自每个参与者的免疫细胞都暴露于三种细菌刺激物——共生细菌B.fragilis,常见病原体S.aureus和E.coli产生的一种毒性物质——还有两种念珠菌属真菌。它们的应答情况通过细胞因子的产生情况得到反映。通过研究参与者的免疫应答与微生物群体之间的可能关系,研究人员发现了微生物群体及其功能与免疫应答之间相互作用的清晰模式。其中一些相互作用依赖于特定病原体,也有一些依赖于细胞因子,还有的相互作用同时依赖于两者。
【6】Nature:肠道细菌不平衡增加糖尿病风险
doi:10.1038/nature18646
目前,科学家们认为导致胰岛素耐受性(insulin resistance)的主要因子是体重超重和缺乏身体活动。一项新的由欧盟资助的一个欧洲-中国团队开展的被称作MetaHit的突破性研究发现特定的肠道细菌不平衡能够导致胰岛素耐受性,从而导致2型糖尿病等健康问题的风险增加。相关研究结果于2016年7月13日在线发表在Nature期刊上,论文标题为“Human gut microbes impact host serum metabolome and insulin sensitivity”。
论文共同通信作者、丹麦哥本哈根大学代谢中心教授Oluf Pedersen说,“我们证实特定的肠道菌群不平衡是胰岛素耐受性的重要促进因素。胰岛素耐受性是2型糖尿病、高血压和动脉粥样硬化性心血管疾病(不断增加的流行病)的先驱状态。”
在对277名非糖尿病丹麦人和75名2型糖尿病丹麦患者的研究中,这个团队分析了胰岛素的作用。他们监测了血液中1200多种代谢物的浓度,并且对人肠道中的上百种细菌进行先进的基于DNA的分析以便探究肠道菌群的某些不平衡是否与常见的代谢疾病和心血管疾病存在因果关系。
doi:10.1038/srep28484
如果被问及有害的肠道细菌会引发什么问题,大多数人或许都认为有害肠道菌群会引发消化道问题,比如便秘、胃胀气或腹泻;但近日科学家们发现,有害细菌,或有益细菌水平不够或许和多发性硬化症发生直接相关,相关研究发表于Scientific Reports杂志上。
Ashutosh Mangalam博士表示,人类机体肠道中携带着数万亿个细菌,俗称为肠道微生物组,近年来多项研究表明,肠道菌群在改善并维持人体健康上扮演着重要作用。肠道细菌往往机体健康息息相关,为此研究人员就想知道是否肠道菌群和慢性自身免疫性疾病直接相关,比如多发性硬化症等,同时研究者还想知道是否自身免疫性疾病患者机体的肠道微生物组不同于健康个体的肠道微生物组。
研究者表示,实际上多发性硬化症患者有着和健康个体不同的肠道微生物组,尽管这是一项初步研究,但相关数据表明,多发性患者机体中有益菌群的水平较低,比如那些从健康食物(黄豆、亚麻)中获取效益的有益菌群。
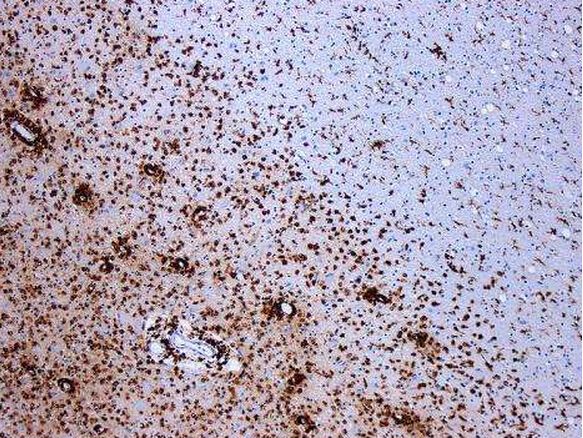
doi:10.1016/j.cell.2016.06.001
在一项新的研究中,来自美国贝勒医学院的研究人员报道,缺乏一种特定的肠道细菌物种导致小鼠社交能力不足(social deficit)。这些社交能力不足令人想起人类自闭症谱系障碍(autism spectrum disorder, ASD)的症状。通过将这种细菌物种添加到受影响的小鼠肠道中,研究人员能够逆转这些小鼠的一些社交行为问题。相关研究结果发表在2016年6月16日那期Cell期刊上,论文标题为“Microbial Reconstitution Reverses Maternal Diet-Induced Social and Synaptic Deficits in Offspring”。如今,研究人员正准备在未来的研究中探究益生菌对神经发育障碍的影响。
“其他研究小组正在试图使用药物或脑部电刺激来逆转与神经发育障碍相关联的一些行为症状,但是在这项新的研究中,我们可能有一种新方法”,论文通信作者、贝勒医学院神经科学副教授Mauro Costa-Mattioli博士说,“我们目前仍然不知道它是否能够在人体内有效,但是它一种非常令人激动的从肠道影响脑部的方法。”
这项研究的灵感来自人类流行病学研究,这些研究已发现怀孕期间孕妇肥胖可能增加小孩患上神经发育障碍(包括ASD)的风险。此外,一些ASD患者也表现出反复发作的胃肠道问题。随着不断有研究证实饮食如何能够改变肠道微生物组和肠道细菌如何影响脑部,Costa-Mattioli和他的同事们猜测这之间可能存在关联。
doi:10.1038/nature18309
上万亿个微生物栖息在我们的肠道中。肥胖与我们肠道细菌变化相关联,但是其中的机制是不清楚的。在一项新的研究中,来自美国耶鲁大学医学院和丹麦哥本哈根大学的研究人员鉴定出肠道菌群变化如何导致肥胖。相关研究结果于2016年6月8日在线发表在Nature期刊上,论文标题为“Acetate mediates a microbiome–brain–β-cell axis to promote metabolic syndrome”。
在早前的一项研究中,耶鲁大学医学院主任医师Gerald I. Shulman博士已观察到一种短链脂肪酸,即乙酸,刺激啮齿类动物体内的胰岛素分泌。在这项新的研究中,为了更多地了解乙酸的作用,Shulman和他的团队在肥胖模式啮齿类动物体内开展一系列实验。
研究人员比较了乙酸和其他的短链脂肪酸,发现在摄入高脂肪食物的啮齿类动物体内存在更高水平的乙酸。他们也观察到灌注乙酸也会刺激胰腺中的β细胞分泌胰岛素,但是仍然不清楚这是如何实现的。
DOI:10.1126/science.aad9948
肠道微生物最调节宿主的免疫系统以及在炎症性肠炎(IBD)等疾病发病过程中发挥了十分重要的作用。由于在同卵双胞胎中该疾病的发病率一致性只有40%-50%,因此遗传-环境因素的相互作用对该疾病的发病具有重要的影响。DNA测序技术的发展使得我们能够详细地了解人体基因组的信息以及肠道微生物的基因组构成,进而发现在肠炎发病患者体内肠道微生物的种类发生了慢性的变化。
此前的研究发现:人体肠道中的一类叫做"脆弱类拟杆菌(B.A)"的共生菌对人体免疫系统具有正面的调控作用。在小鼠试验中,该细菌能够将LPS通过"OMV"的分泌小泡传递到宿主的肠道DC中,进而诱导DC分泌IL-10并促进调节性T细胞的分化。
来自加州理工大学生物工程学系的Sarkis K. Mazmanian针对"脆弱类拟杆菌"的这一机制在肠炎发病过程中的作用进行了深入研究,相关结果发表在最近一期的《Science》杂志上。
首先,作者提取了野生型小鼠的BMDC,并将其与野生型B.A的OMV或者确实突变了PSA的OMV共同孵育,之后进一步与CD4 T细胞孵育。结果显示,野生型细菌的OMV能够促进DC分泌IL-10,但是缺失了PSA的OMV则没有这一活性。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#机体健康#
79
#微生物#
85
学习了谢谢分享
150