三阴性乳腺癌:循证证据不足 研究道路漫长
2011-07-14 医师报 医师报
▲ 北京大学肿瘤医院乳腺肿瘤内科 严颖 任军 在西方人群中,三阴性乳腺癌占全部乳腺癌的10%~15%,尤以非洲裔人群多见(超过50%)。来自亚洲的报告显示,三阴性乳腺癌发病率为7%~19%,与白种人相差不多。三阴性乳腺癌因为其本身具有较高的侵袭性,术后复发转移风险高,疾病进展快,内脏转移
▲ 北京大学肿瘤医院乳腺肿瘤内科 严颖 任军
在西方人群中,三阴性乳腺癌占全部乳腺癌的10%~15%,尤以非洲裔人群多见(超过50%)。来自亚洲的报告显示,三阴性乳腺癌发病率为7%~19%,与白种人相差不多。三阴性乳腺癌因为其本身具有较高的侵袭性,术后复发转移风险高,疾病进展快,内脏转移风险高等特点,并且缺乏内分泌治疗,抗HER2靶向治疗的机会。
目前针对三阴性乳腺癌的治疗无论是化疗还是靶向治疗,均缺乏能够改变临床治疗策略的循证医学证据。多数临床试验仅能观察到治疗有效率的提高和疾病进展时间的延长,但生存获益有限。因为在转移性三阴性乳腺癌治疗方面没有较大的突破,在辅助治疗和新辅助治疗领域进展缓慢。因此,三阴性乳腺癌目前是乳腺癌治疗的瓶颈,也是研究的热点。
早期乳腺癌新辅助治疗:铂类和贝伐珠单抗研究之路漫长
三阴性乳腺癌常伴有BRCA1通路的失活,并且和BRCA1相关性乳腺癌具有许多相似的特征。两者不仅预后均较差,而且还有相似的分子特征:核分级高、 Ki67高表达、CK5/6阳性、EGFR阳性等。由于BRCA1基因与DNA双链的断裂修复有关,而铂类药物可与DNA双链交联,导致DNA双链断裂,阻碍DNA复制、转录并最终导致细胞死亡,因此铂类药物在三阴性乳腺癌中可能更有效。 在本届ASCO大会上也有几篇有关铂类药物在三阴性乳腺癌新辅助治疗中应用的报道。
GEICAM 2006-03是一项多中心Ⅱ期随机临床试验,旨在探讨在传统新辅助化疗方案的基础上加卡铂或不加卡铂对疗效的影响。研究入组94例腋窝淋巴结阳性或肿瘤 ≥ 2 cm 的三阴性乳腺癌患者,随机分为EC-T 组(表柔比星+环磷酰胺×4 cy序贯多西他赛×4 cy) 或EC-TCb 组(表柔比星+环磷酰胺×4 cy序贯多西他赛+卡铂×4 cy)。主要研究终点为pCR率,次要研究终点为临床有效率、毒副反应和保乳手术率。 结果显示,EC-T 组和EC-TCb 组pCR率分别为35% 和30%,无显著差异。两组保乳手术率也相似 (33% vs.28%,P=0.6029)。两组3~4级毒副反应相似,主要为中性粒细胞减少和粒细胞缺乏性发热,EC-TCb组贫血和血小板减少发生率增高。研究结果提示,三阴性乳腺癌并不能从含铂的新辅助化疗方案中获益。
抗血管生成治疗是在三阴性乳腺癌中应用最广泛的治疗方法。在转移性三阴性乳腺癌中,虽然贝伐珠单抗的生存获益有限,但能明显提高有效率和延长疾病进展时间。因此,研究者尝试在新辅助治疗中应用贝伐珠单抗治疗。
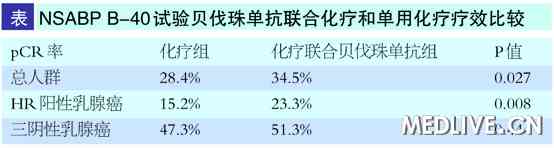
NSABP B-40研究是探索贝伐珠单抗和/或化疗药联合标准新辅助化疗方案治疗可手术HER2阴性乳腺癌是否能提高pCR率,本届ASCO年会上公布了该研究结果。研究共入组1206例可手术HER2阴性乳腺癌患者,随机分组:含紫杉类方案组;含紫杉类方案联合贝伐珠单抗(B)组(B:15 mg/kg,每三周×4周期)。主要研究终点为乳腺癌pCR率。结果显示,1180例可评价pCR的患者中,三阴性乳腺癌占41%。联合贝伐珠单抗可增加了pCR率。亚组分析显示,HR阳性乳腺癌从贝伐珠单抗的治疗中获益显著较多;三阴性乳腺癌无显著获益(表)。联合贝伐珠单抗组不良反应增加:包括高血压、手足综合征和黏膜炎(LBA1005)。贝伐珠单抗在三阴性乳腺癌新辅助治疗中并未取得pCR率获益,令人感到意外。而在本次大会上报道的另一项贝伐珠单抗+蒽环联合紫杉类化疗新辅助治疗三阴性乳腺癌的临床研究(GBG 44试验)结果显示,贝伐珠单抗能提高三阴性乳腺癌的pCR率。
这两项试验结果相互矛盾,可能与多种因素有关(包括样本检测准确性、三阴性乳腺癌的异质性和患者生物学的差异等)。加州大学旧金山分校Rugo教授对此发表评论,指出应避免满足于过低期望,应该设计更好的前瞻性试验。为了预测疗效,需要更准确地理解乳腺癌各亚型的生物学特性及其标志。
{nextpage}
早期乳腺癌辅助治疗:不断有尝试 寻找新机会
三阴性乳腺癌辅助治疗的研究偏少,在本届ASCO大会上仅有几篇报道涉及这一问题。伊沙匹隆是第一种埃博霉素类抗肿瘤药物,与紫杉类有不同的微管结合位点,因此对紫杉类耐药者仍有活性。伊沙匹隆治疗蒽环类、紫杉类和卡培他滨耐药转移性乳腺癌的Ⅱ期临床试验(081试验)结果显示,ORR为11.5%,中位PFS为3.1个月,中位OS为8.6个月。另外两项Ⅲ期临床研究(BMS 046/048试验)表明,对于蒽环类和紫杉类耐药及蒽环类、紫杉类、卡培他滨三重耐药的转移性乳腺癌,包括三阴性乳腺癌患者,伊沙匹隆联合卡培他滨均有一定的疗效,但3~4级不良反应增加明显,特别是周围神经病变。
美国Sarah Cannon研究中心开展的一项Ⅲ期临床试验,旨在比较三阴性乳腺癌辅助化疗方案中,伊沙匹隆替代紫杉醇,能否取得更好的疗效。目前研究已入组226例患者,随机分为AC序贯紫杉醇组和AC序贯伊沙匹隆组,在今年ASCO大会上,初步报道了其安全性数据,AC序贯伊沙匹隆组有10例(8%)患者因不能耐受毒副反应而出组;AC序贯紫杉醇组有18例(17%),两组最常见的终止治疗的毒副反应均为神经毒性。 两组过敏反应、乏力、疼痛等毒副反应发生率相似。研究提示,伊沙匹隆用于三阴性乳腺癌的辅助治疗,与紫杉醇的毒副反应相似,最常见的患者不能耐受的毒副反应是神经毒性。
转移性乳腺癌治疗:循证证据不足,研究尚需努力
Iniparib研究结果阴性
研究显示三阴性乳腺癌存在DNA修复缺陷,这让DNA修复酶多聚腺苷二磷酸核糖聚合酶(PARP)抑制剂成为一种潜在的靶向治疗药物。2009年ASCO 年会上公布的Olaparib和Iniparib两种PARP抑制剂治疗三阴性乳腺癌Ⅱ期临床研究结果令人振奋,Iniparib联合吉西他滨/卡铂可显著延长三阴性转移性乳腺癌患者PFS和OS。2011年1月《新英格兰医学杂志》上发表的一项开放Ⅱ期临床研究结果显示,对于晚期三阴性乳腺癌患者,吉西他滨/卡铂化疗联合Iniparib较单用化疗可提高临床获益和OS,且未增加化疗毒性。因此众人期盼Ⅲ期临床试验结果,PARP抑制剂的出现将为三阴性乳腺癌的治疗带来突破。
本届ASCO大会上公布了IniparibⅢ期随机临床研究结果。研究入组标准:年龄≥18岁;转移性三阴性乳腺癌;有可测量病灶;既往接受过≤2线细胞毒药物化疗方案。主要研究终点为OS和PFS。研究入组519例转移性三阴性乳腺癌患者,随机分为两组,吉西他滨/卡铂组(GC组,258例),给予 G:1000 mg/m2,d1,8,C:AUC=2,d1,8,Q21d;吉西他滨/卡铂+Iniparib组(GCI组,261例),给予G:1000 mg/m2,d1,8;C:AUC=2,d1,8;I:5.6 mg/kg,d1,4,8,11,Q21d。GC组患者疾病进展后可交叉至GCI组继续治疗。结果显示,两组OS及PFS均未达到预期的显著差异。GC组和GCI组中位OS分别为11.1个月和11.8个月(HR=0.876,P=0.284),中位PFS分别为5.1个月和4.1个月(HR=0.794,P=0.027),GC组152例/258例(59%)疾病进展后交叉至GCI组继续治疗。该项Ⅲ期临床试验观察到的毒副反应与Ⅱ期临床试验相似,但未能对疗效加以验证。
贝伐珠单抗待证实
三阴性乳腺癌缺乏有效的治疗靶点,因此近年的研究重点主要集中在新药的研发和抗血管生成的靶向治疗。基于E2100研究结果,美国FDA于2008年2月通过快速审批通道批准了贝伐珠单抗+紫杉醇作为转移性HER阴性乳腺癌患者一线治疗方案,但2010年12月16日,FDA建议撤消贝伐珠单抗治疗乳腺癌适应证,其原因基于四项试验(E2100、AVADO、RIBBON-1和RIBBON-2试验)的临床研究数据显示,该药并没有延长乳腺癌患者的OS,也没有为患者带来能够抵消用药风险的足够临床获益。因此对于贝伐珠单抗在转移性乳腺癌中的应用,正在积极开展新的研究,以鉴别出哪些适合应用该药的人群。
本届ASCO年会公布了RIBBON-2试验(贝伐珠单抗联合不同化疗方案二线治疗HER2阴性转移性乳腺癌的Ⅲ期临床试验)三阴性亚组的分析结果。 684例入组患者中,159例(23%)为三阴性乳腺癌。亚组分析显示,贝伐珠单抗联合化疗组(112例)中位PFS较安慰剂联合化疗组(47例)显著延长(6.0个月 vs. 2.7个月,P=0.0006);中位OS有延长的趋势(17.9个月 vs. 12.6个月,P=0.0534)。但该研究的三阴性亚组样本量较小,更大规模的贝伐珠单抗治疗三阴性乳腺癌的随机前瞻试验正在进行中。
索拉非尼疗效初显
其他针对肿瘤血管的靶向药物中,索拉非尼是针对肿瘤细胞和肿瘤血管的多靶点的酪氨酸激酶抑制剂。已有四项临床试验证实在既往未使用过贝伐珠单抗的HER2 阴性转移性乳腺癌中,索拉非尼联合化疗有较好的疗效。对酪氨酸激酶受体的抑制可能克服贝伐珠单抗的耐药,因此目前开展了研究索拉非尼治疗贝伐珠单抗治疗进展的HER2阴性局部晚期和转移性乳腺癌的Ⅱb期随机临床试验。患者随机分为化疗联合索拉非尼组(81例)和化疗联合安慰剂组(79例)。化疗方案为吉西他滨或卡培他滨。结果显示,索拉非尼联合化疗可显著延长PFS(3.4个月 vs. 2.7个月,P=0.001)和TTP(3.6个月 vs. 2.7个月,P=0.0009)。化疗联合索拉非尼组最常见的3~4级毒副反应是手足综合征。但该研究结果尚需Ⅲ期临床试验进一步证实。
小提示:本篇资讯需要登录阅读,点击跳转登录
版权声明:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#阴性乳腺癌#
57
#循证#
86
#三阴性#
65