JCO社论:弥漫大B细胞淋巴瘤的治疗,是否越来越智能?
2022-09-19 聊聊血液 网络
8月初,《Journal of Clinical Oncology》报道了一项研究者发起的单臂、II期Smart Start研究,其中探索了初治弥漫大B细胞淋巴瘤一个新的联合方案,即利妥昔单抗、来那度
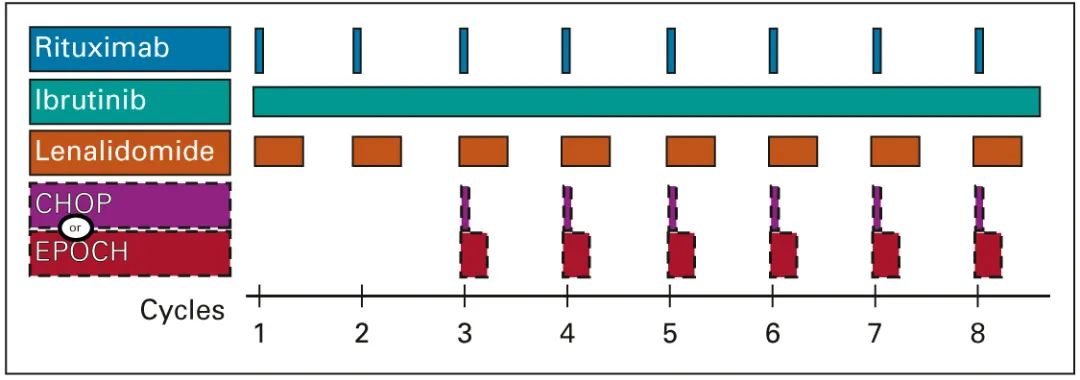
8月初,《Journal of Clinical Oncology》报道了一项研究者发起的单臂、II期Smart Start研究,其中探索了初治弥漫大B细胞淋巴瘤一个新的联合方案,即利妥昔单抗、来那度胺、伊布替尼方案(RLI)。研究共入组60例患者,给予患者利妥昔单抗 375 mg/m2(D1静脉给药)、来那度胺25 mg(每日一次口服,D1-10)和伊布替尼560 mg(每日一次口服,连续给药,21天为一个周期);治疗2个周期后,在 RLI 基础上加用标准化疗(CHOP或EPOCH)再治疗6个周期。
患者中42%为R-IPI高危,62%为双表达。RLI治疗2个周期后的 ORR 为86.2%,RLI+化疗治疗结束时的CR率为94.5%(ORR 100%),EPOCH或CHOP化疗的缓解率无差异。中位随访31个月,2年PFS和OS率分别为91.3%和96.6%。
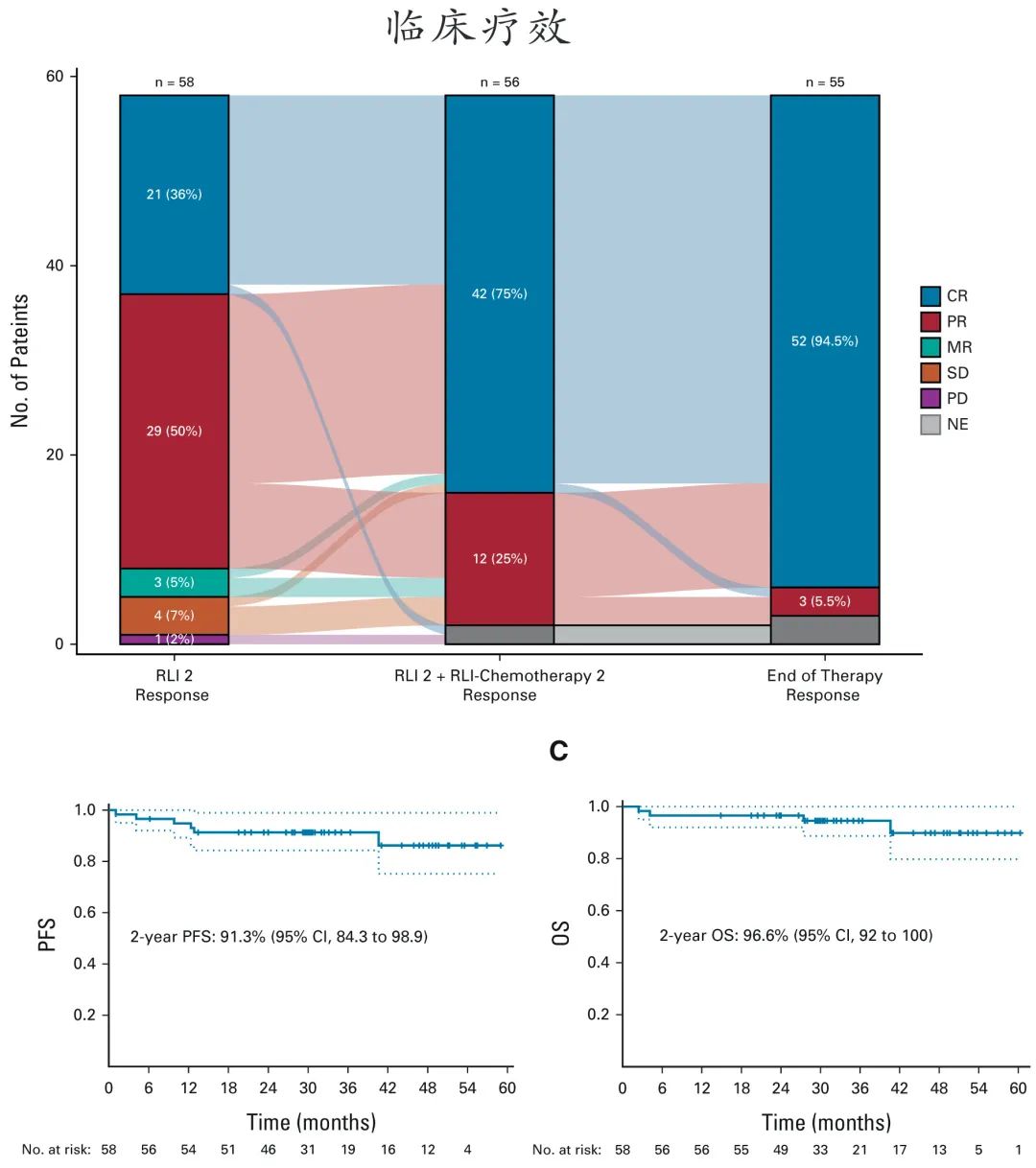
Smart Start研究是第一项在化疗前使用靶向联合方案治疗新诊断 DLBCL 的研究,证实RLI可带来较高的ORR,且联合化疗产生了持久缓解,从而确立了开发生物学驱动和非细胞毒性DLBCL一线治疗的潜力。
近日JCO杂志发表了Brad S Kahl教授的社论文章“Management of Diffuse Large B-Cell Lymphoma: Are We Getting Smarter? “,现摘取主要内容如下。
R-CHOP方案可以治愈85%的局限期患者,而老年/虚弱患者可能需要减量方案(如R-miniCHOP),基线心脏功能较差的患者可能需要用依托泊苷替代多柔比星(R-CEOP)。DLBCL 生物变体的患者,例如双打击 DLBCL 或原发纵隔DLBCL,可以更好地接受更强化的方(例如EPOCH-R)。此外CNS 复发高危患者一般接受某种形式的 CNS 预防,但最近的数据质疑了这一策略。
改善 DLBCL疗效的策略通常分为三类:强化细胞毒药物、添加或替代新的单抗或所谓的 R-CHOP 加 X。强化治疗包括结合一线自体干细胞移植、剂量密集的 R-CHOP 或动态调整输注给药 (EPOCH-R),但它们均无法改善结局;而加入较新的单克隆抗体(如obinutuzumab)也并不优于标准治疗;此外一系列 R-CHOP 加 X 的研究,即使在 DLBCL 生物学的基础上选择合适药物,结果也是阴性。
已知 DLBCL 是一种生物学异质性疾病,由处于不同成熟阶段的成熟 B 细胞引起,在起源细胞的基础上产生两种不同的亚型(生发中心 B 细胞 [GCB] 和活化 B 细胞 [ABC])。部分靶向药物(如硼替佐米、来那度胺和伊布替尼)在 ABC 亚型 DLBCL 中的活性更高,并且这种活性差异具有高度合理的生物学解释。但3项独立的随机临床研究(富集了 ABC DLBCL 患者,评估 R-CHOP +硼替佐米、伊布替尼或来那度胺)均未能显示结局改善。这些负面的研究极度令人失望,因为它们意味着将生物发现转化为治疗的尝试失败了。
最近发表的一项研究可能改变晚期、IPI 2-5分DLBCL患者的标准治疗。在这项全球 III 期随机临床研究中,抗体药物偶联物 polatuzumab vedotin 取代了 R-CHOP 方案中的长春新碱,并显示2年PFS改善。如果R-CHP-Pola(利妥昔单抗、环磷酰胺、阿霉素、泼尼松和polatuzumab vedotin)的新方案获得监管机构批准,它可能成为合格患者的新标准治疗。,然而即使 R-CHP-Pola 取得了突破性进展,但 DLBCL 仍未实现基于疾病生物学的个性化治疗,即使已经对其生物学有了相对好的认知。
MD 安德森癌症中心的研究者试图将这种个性化治疗的差距与使用基于细胞起源检测(Smart Start) 选择的新型药物的试验联系起来。研究者进行了一项具有窗口设计要素(window design element)的 II 期研究,他们选择非 GCB DLBCL 患者(意味着富集ABC),先给予两个周期的利妥昔单抗、来那度胺和伊布替尼 (RLI) 治疗,直至周期3才加用常规化疗。两个周期 RLI治疗的总缓解率为86%,完全缓解率为36%,这似乎令人印象深刻。然后患者完成6个额外周期的常规治疗(EPOCH或CHOP)联合RLI。尽管在本试验中未尝试调整 EPOCH 剂量,但 RLI 似乎不影响化疗的可及性。整个治疗后的总缓解率为100%,2年PFS率为91%,这一结局肯定优于大多数研究。
在化疗中添加 RLI 是否改善了非 GCB DLBLC 的可治愈性?作者通过将Smart Start研究结果与最近发表的晚期 DLBCL III 期研究进行比较,认为答案是肯定的,其中约70%的患者在3年时无进展。但Brad S Kahl教授担心这一比较是无效的,因为Smart Start研究中37%的患者为局限期,明显比晚期患者更容易治愈。此外这种类型的试验设计也存在固有的选择偏倚,入组医生可能不倾向于入组病情最严重、大多数有症状的患者,毕竟该研究中直至周期3才给予经证实的治疗。此外,能够飞到三级医疗中心进行第二评估和治疗的患者与紧急就诊的患者有着根本的不同。当然并不是说结果是无效的,但它们可能不会转化到更广泛的人口。
尽管Smart Start研究的总体结果很难解释,但该研究的优势在于其窗口要素(window element),它证明了新型药物的高活性,而不会损害结局。窗口设计为未来的努力提供了路线图,人们可以在增加标准治疗之前,以类似的方式测试其他新型药物。在窗口部分前/后进行配对活检可以提供关键的生物学见解,特别是提高对无应答者耐药机制的理解。
那么后文如何?有学者使用利用对这些靶向药物的反应以减少患者接受的细胞毒性化疗量(Smart Stop, NCT04978584),其他工作组也在探索对DLBCL生物学的认知纳入个性化治疗方法中;现在很明显的是,简单的 ABC 与 GCB 区分对于精准医疗来说并不够精确,而利用突变谱分析和基因组结构改变的特征,至少可以确定5种不同的 DLBCL 分子亚型。在此框架内,ABC DLBCL可分为两个不同亚组,GCB DLBCL也可分为两个不同亚组,且每个亚组均具有非常差异化的分子学基础和结局。可以认为,既往R-CHOP + X试验失败的真正原因不是由于选择的药物无活性,而是患者人群对于正在研究的靶向药物不够精确。利用这一理论,National Clinical Trials Network计划在 DLBCL 中开展一系列精准医学试验(称为Lymphomatch),在 R-CHOP 化疗中添加通路特异性药物,但该策略只应用于已准确表征为属于5种分子亚型之一的患者。通过这些努力,DLBLCL的治疗会更智能、个性化并改善结局。
参考文献
1. Jason Westin ,et al. Smart Start: Rituximab, Lenalidomide, and Ibrutinib in Patients With Newly Diagnosed Large B-Cell Lymphoma. J Clin Oncol . 2022 Aug 11;JCO2200597. doi: 10.1200/JCO.22.00597.
2.Brad S Kahl. Management of Diffuse Large B-Cell Lymphoma: Are We Getting Smarter?J Clin Oncol . 2022 Sep 1;JCO2201501. doi: 10.1200/JCO.22.01501.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言