2023专家共识:脊柱关节炎生物制剂靶向药物治疗专家共识
2023-06-11 生物制剂Biotech 生物制剂Biotech 发表于上海
本共识旨在为临床医师安全有效地使用靶向药物提供指引,提高我国SpA的规范治疗水平,本共识提出了13条推荐意见,仅供参考。
编者按
如何针对脊柱关节炎SpA患者的疾病特点,精准且规范地选择与使用靶向药物,在合理选择的同时兼顾其安全性,使更多SpA患者获益是临床亟待规范的问题。为此,由国家皮肤与免疫疾病临床医学研究中心(北京协和医院)联合中国医师协会风湿免疫专科医师分会、中国康复医学会风湿免疫专业委员会及中国研究型医院学会风湿免疫专业委员会,依据循证医学证据及共识制定的国际规范制定了本共识,旨在为临床医师安全有效地使用靶向药物提供指引,提高我国SpA的规范治疗水平,本共识提出了13条推荐意见,仅供参考。
推荐意见1
先后经至少两种非甾体抗炎药(NSAIDs)治疗效果不佳的中轴型SpA,或经一种传统改善病情抗风湿药物(DMARDs)治疗外周关节病变控制不佳的SpA,或皮肤损害严重的PsA,建议使用靶向药物治疗。
先后经至少两种NSAIDs最大剂量治疗超过4周,或先后使用过两种NSAIDs治疗2个月病情仍活动或对NSAIDs不耐受的中轴型SpA患者,建议使用靶向药物治疗;经一种传统DMARDs治疗但外周关节炎控制不佳,或经一种NSAIDs治疗但附着点炎和中轴症状仍活动的SpA患者,建议使用靶向药物治疗。SpA疾病活动定义为基于C反应蛋白计算的AS疾病活动度评分(ASDAS-CRP)≥2.1或Bath AS活动性指数(Bath ankylosing spondylitis disease activity index,BASDAI)≥4。对皮肤损害严重的PsA患者,亦建议使用靶向药物治疗。
针对中轴型SpA患者治疗的随机对照试验显示,TNFα抑制剂、IL-17A抑制剂、JAK抑制剂均能降低NSAIDs充分治疗失败的中轴型SpA患者的疾病活动度。
针对AS患者治疗的研究显示,AS患者需使用NSAIDs的最大剂量才能获得最佳疗效,且NSAIDs通常需在治疗2周后方能达到最大疗效,2周后疗效增加不显著。国外关于AS治疗的指南均对AS患者开始使用靶向药物治疗的时机给出了大致相同的推荐意见。
推荐意见2
建议在开始使用靶向药物治疗前,对SpA患者的病情进行全面评估,包括疾病活动度、结构损伤进展情况、关节受累部位和程度、关节外表现、功能状态及合并疾病等。
在开始靶向药物治疗前,应对SpA患者的病情进行全面评估。疾病活动度是决定是否开始使用靶向药物治疗的关键。中轴型SpA常用的评估工具包括AS疾病活动评分(ankylosing spondylitis disease activity score,ASDAS)或BASDAI。PsA的评估工具包括PsA疾病活动指数(disease activity index for PsA,DAPSA)和最低疾病活动度(minimum disease activity,MDA)等。附着点炎是SpA的特征性病变和结构进展的基础,可导致不可逆的骨损伤。髋关节是中轴型SpA患者常见的受累关节,病变进展可引起关节结构损伤,导致机体功能受限和残疾。远端指间关节是PsA最常累及的部位,随着疾病进展,可由单或寡关节炎向多关节炎发展,最终引起残疾。因此,对出现附着点炎和髋关节受累的SpA患者,以及出现远端指间关节炎的PsA患者,应尽早开始靶向药物治疗。
推荐意见3
开始靶向药物治疗前,应进行慢性肝炎病毒感染和结核感染筛查。
在开始靶向药物治疗前,应对是否存在乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)和结核感染进行筛查。
TNF-α是参与抑制HBV病毒复制的重要细胞因子。5%既往感染HBV的炎症性肠病、AS、PsA患者接受TNF抑制剂治疗可能导致HBV再激活,引起乙型肝炎复发,重者可致肝衰竭甚至死亡。HBsAg阳性患者肝炎病毒再激活的风险可高达27%~39%,JAK抑制剂亦会增加HBV病毒复制的风险。IL-17A抑制剂在SpA患者中进行的几项临床研究中未见HBV再激活的报道。慢性HCV感染患者使用靶向药物治疗导致HCV再激活的风险相对较小。但由于长期使用IL-17A抑制剂治疗的安全性尚不明确,因此推荐所有SpA患者在开始靶向药物治疗前均应常规筛查HBV和HCV感染情况。
推荐意见4
建议选择TNF抑制剂或IL-17A抑制剂作为中轴型SpA患者的初始靶向治疗药物;PsA患者可根据不同临床表现选择不同的靶向治疗药物。
多项AS患者治疗的随机对照试验证实,TNF抑制剂可有效改善活动性AS患者的临床与影像学表现,包括复合疗效指标、患者自述疗效及影像学改变等;IL-17A抑制剂亦能有效控制AS的炎症,改善临床症状与影像学改变。目前尚无TNF抑制剂和IL-17A抑制剂治疗AS的“头对头”对比研究,但国内外SpA诊治指南或诊疗规范均推荐,将TNF抑制剂和IL-17A抑制剂作为NSAIDs治疗SpA无效后可选择的生物制剂,两者并无优先顺序。美国食品药品监督管理局已批准TNF抑制剂和IL-17A抑制剂用于治疗nr-axSpA,但目前我国尚无药物获批用于治疗nr-axSpA。
PsA患者外周关节炎、附着点炎、指(趾)炎、皮肤损害、指(趾)甲损害常见,应根据主要受累部位和程度选择靶向药物。目前,多项PsA患者治疗的Ⅲ期临床研究显示,TNF抑制剂、IL-17A抑制剂、IL-12/IL-23抑制剂、JAK抑制剂、PDE4抑制剂、选择性T细胞共刺激调节剂等均可有效改善PsA患者的外周关节炎,亦均可有效治疗PsA患者的皮肤病变。
推荐意见5
对合并复发性葡萄膜炎或炎症性肠病的SpA患者,建议优先使用单克隆抗体类TNF抑制剂。
23%的AS患者、15.9%的nr-axSpA患者、3%的PsA患者出现前葡萄膜炎,合并炎症性肠病的比例分别为6.4%、4.1%、3%,AS和nr-axSpA合并银屑病的比例分别为10.2%、10.9%。SpA患者治疗的临床研究和Meta分析显示,与依那西普比,阿达木单抗、英夫利昔单抗可降低AS患者葡萄膜炎的发生率。少数在SpA患者中进行的开放标签和非对照研究亦证实,培塞利珠单抗或戈利木单抗对SpA相关前葡萄膜炎有一定的疗效。因此,TNF-α单克隆抗体在预防新发葡萄膜炎方面优于TNF-α融合蛋白依那西普。IL-17A抑制剂在前葡萄膜炎的预防与减少复发方面的作用尚不明确。由于有使用IL-17A抑制剂诱发或加重炎症性肠病的报道,因此,对合并活动性炎症性肠病的SpA患者应慎用IL-17A抑制剂。
推荐意见6
对TNF抑制剂或IL-17A抑制剂疗效不佳或不耐受的AS患者,可选择JAK抑制剂。
JAK抑制剂通过抑制细胞内JAK通路的信号传导,缓解附着点炎和指(趾)炎,在AS的临床研究中显示出较好的疗效。目前有治疗SpA疗效和安全性证据的JAK抑制剂有托法替布和乌帕替尼,可作为其他靶向药物治疗SpA不耐受或疗效不佳的选择。
推荐意见7
不推荐生物制剂联合甲氨蝶呤治疗中轴型SpA
既往研究表明,甲氨蝶呤、柳氮磺吡啶、来氟米特等对SpA患者的中轴症状无效,仅在外周关节受累、关节外表现及由于副作用、禁忌证或无其他药物选择的情况下使用。使用生物制剂治疗的中轴型SpA患者联用甲氨蝶呤或柳氮磺吡啶并不能提高疗效或延长药物的使用时间。中轴型SpA 患者治疗的随机对照研究显示,与英夫利昔单抗单药治疗比,英夫利昔单抗联合甲氨蝶呤治疗并不增加中轴型SpA患者达到ASAS20、ASAS40的比例及BASDAI改善率。此外药代动力学研究显示,中轴型SpA患者使用英夫利昔单抗联合甲氨蝶呤治疗时,并不能升高英夫利昔单抗的血药浓度。
推荐意见8
使用靶向药物治疗期间,建议定期行治疗反应评估及不良反应监测
SpA的主要治疗目标是通过控制炎症及预防、延缓结构损伤,最大限度地保存或改善患者的整体功能状态和生活质量,避免或减少残疾,同时避免药物的副作用。靶向药物治疗期间,对未达到治疗目标的患者,建议每1~3个月进行治疗反应评估,直至达到治疗目标;对已达到治疗目标的患者,建议每3~6个月进行一次疾病活动度评估。推荐使用ASDAS或BASDAI评估和监测中轴型SpA患者的疾病活动度,ASDAS与临床疗效、炎症生物标志物及根据MRI进行的炎症评分有良好的相关性,可用于评估靶向药物的疗效。此外,治疗期间应定期评估患者的整体功能状态和关节外表现。推荐使用PsA疾病活动指数或最低疾病活动度评估和监测PsA患者的疾病活动度。
应用靶向药物治疗期间应密切监测药物相关不良反应。TNF抑制剂常见的不良反应包括上呼吸道感染、血细胞减少、肝酶升高等,充血性心力衰竭和脱髓鞘疾病等罕见。IL-17A抑制剂的常见不良反应包括上呼吸道感染、鼻咽炎、头痛等,部分患者出现念珠菌感染,出现炎症性肠病等亦有报道。JAK抑制剂亦增加上呼吸道感染的发生风险,其带状疱疹病毒感染的发生率高于TNF抑制剂;存在心脑血管疾病发病危险因素的患者,有增加重要心血管事件和血栓的发生风险,应用时需注意。
推荐意见9
经靶向药物治疗病情稳定至少6个月的SpA患者,方可考虑减量;推荐的减量方案为减少单次用药剂量或延长用药间隔。在减量过程中应定期评估SpA疾病活动度,如出现复发,则应恢复原剂量。
2017年SpA国际工作组推荐,SpA的治疗目标为肌肉骨骼症状和关节外表现缓解,即无疾病活动状态,但低/极低疾病活动度亦是可以接受的治疗目标。中轴型SpA患者治疗后ASDAS-CRP<1.3或BASDAI≤2为疾病缓解,ASDAS-CRP<2.1或BASDAI<4为低疾病活动度。尽管目前对SpA达标治疗的理念仍有争议,但目前进行的大多数SpA患者靶向药物减量的研究中,减量均是在SpA处于低疾病活动度或疾病缓解后才开始的。目前有关SpA患者减停靶向药物的研究很少。但在PsA和中轴型SpA中的研究显示,在靶向药物减量前,较低的疾病活动度与靶向药物减量后仍能维持缓解的可能呈正相关。因此推荐,SpA患者在维持低疾病活动度或疾病缓解半年以上方可考虑减少靶向药物。除了疾病活动度外,亦要结合SpA患者关节外表现的缓解程度以决定是否开始靶向药物减量。靶向药物的减量方案包括减少单次用药剂量或延长用药间隔。
推荐意见10
建议根据患者的合并疾病,采用个体化、分层管理的原则,决定靶向药物治疗的时机与种类。
由于SpA患者的临床异质性强,合并疾病多,因此建议根据患者的临床情况,采用分层管理的原则进行个体化治疗。
1.有活动性结核感染的SpA患者,不推荐使用靶向药物治疗,建议转诊至专科医生进行抗结核治疗。
2.合并HBV感染的SpA患者,应根据感染状态进行分层管理。
3. 对合并充血性心力衰竭的SpA患者,推荐优先选择IL-17A抑制剂。
4.对合并严重活动性感染(需静脉注射抗生素或住院治疗)的SpA患者,不推荐应用靶向药物治疗。
5.有恶性肿瘤病史的SpA患者,需综合判断其肿瘤复发风险,谨慎使用靶向药物。
推荐意见11
SpA患者在使用靶向药物治疗前或使用期间可接种灭活疫苗
由于疾病本身及药物的影响,SpA患者发生流行性感冒和肺炎等感染性疾病的风险高于健康人群。大多数接受免疫抑制治疗的风湿病患者接种疫苗是有益的。目前风湿病患者使用靶向药物治疗的临床研究已证实,在靶向药物(阿巴西普、利妥昔单抗除外)治疗期间,接种流行性感冒和灭活肺炎球菌疫苗是安全有效的,因此推荐SpA患者在开始靶向药物治疗前或使用期间接种肺炎球菌和流行性感冒疫苗。由于接种减毒活疫苗尚缺乏足够的安全性证据,因此不推荐SpA患者接种减毒活疫苗。
TNF抑制剂与JAK抑制剂治疗均显著增加带状疱疹病毒再激活的发生率。使用JAK抑制剂后带状疱疹再激活的发生率为3~4例/100患者年,使用TNF抑制剂治疗的患者带状疱疹病毒再激活率为2~3例/100患者年,因此推荐在开始使用TNF抑制剂和JAK抑制剂前4周接种带状疱疹疫苗,但不推荐在使用TNF抑制剂和JAK抑制剂治疗期间接种。如果在TNF抑制剂和JAK抑制剂治疗期间发生带状疱疹,应暂时中断治疗,直至病毒感染消失。对反复出现带状疱疹病毒感染的SpA患者,可考虑预防性抗病毒治疗。
推荐意见12
拟行手术治疗的SpA患者,手术前应停用靶向治疗药物。手术后至少14 d且无感染时,可恢复使用。
TNF-α在组织修复所需的炎症细胞募集中起关键作用,TNF抑制剂的应用可能导致患者发生感染的风险增加,且与伤口愈合受损或延迟有关,因此建议术前停用;为尽可能降低手术感染的风险,建议停用一个正常用药周期后再行手术;IL-17A抑制剂、乌司奴单抗和古塞奇尤单抗尚无在围手术期使用的数据,但因存在与其他生物制剂相似的感染风险及伤口愈合不良之忧,建议术前停用。建议在术前3 d停用托法替布。对既往有使用托法替布造成假体关节感染史的SpA患者,建议不再使用JAK抑制剂。
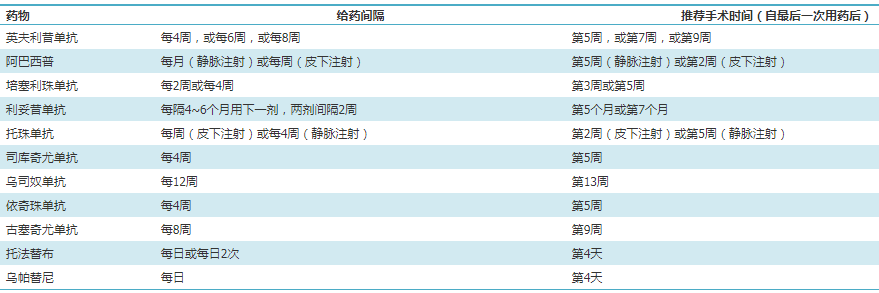
术前停用靶向药物的SpA患者,若术后伤口表现出愈合的征象(通常在14 d左右)、已拆除所有缝线/皮钉,且手术伤口无明显水肿、红斑、渗出物,无非手术部位感染的临床证据时,即可重新开始靶向药物治疗。靶向药物围手术期使用的建议见表1。
表1脊柱关节炎患者围手术期使用靶向药物的建议
推荐意见13
妊娠期和哺乳期SpA患者如需使用靶向药物治疗,推荐优先使用不含Fc段的生物制剂。男性SpA患者在备孕期间,可继续使用TNF抑制剂类药物。
含有Fc段的生物制剂能与胎盘表达的Fc段受体结合,将生物制剂从胎盘的母体侧转运至胎儿侧,进入胎儿循环,可能对胎儿产生一定的影响,因此不含Fc段的生物制剂如培塞利珠单抗,可以不通过胎盘转运,在妊娠全程使用是安全的。基于生物制剂的分子结构和半衰期以及胎盘转运差异,推荐在妊娠20周前停用英夫利昔单抗和阿达木单抗,推荐妊娠30~32周时停用依那西普;戈利木单抗因缺乏胎儿的安全性证据,因此建议在妊娠时停用。小样本类风湿关节炎患者的研究显示,使用生物制剂的患者乳汁中的血药浓度极低甚至检测不到,因此哺乳期的患者仍可考虑使用TNF抑制剂。其他靶向药物,如IL-17A、IL-12/IL-23抑制剂、JAK抑制剂因缺乏足够的安全性证据,因此不推荐用于妊娠和哺乳期患者。
表2 不同妊娠阶段和哺乳期的脊柱关节炎患者靶向药物的选择

根据现有数据,备孕期的男性SpA患者可继续使用TNF抑制剂类药物(包括英夫利昔单抗、依那西普、阿达木单抗和戈利木单抗)。由于有关其他靶向药物对男性生殖的安全性数据有限,因此不建议备孕期男性SpA患者使用除TNF抑制剂以外的靶向药物。
参考文献
[1] 国家皮肤与免疫疾病临床医学研究中心(北京协和医院), 中国医师协会风湿免疫专科医师分会, 中国康复医学会风湿免疫专业委员会, 等. 脊柱关节炎靶向药物治疗专家共识 [J] . 中华内科杂志, 2023, 62(6) : 606-618. DOI: 10.3760/cma.j.cn112138-20221031-00806.
[2] NikiphorouE, RamiroS. Work disability in axial spondyloarthritis[J]. Curr Rheumatol Rep, 2020, 22(9):55. DOI: 10.1007/s11926-020-00932-5.
[3] NgSC, LiaoZ, YuDT, et al. Epidemiology of spondyloarthritis in the People′s Republic of China:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言