探案:发热咳嗽引出的头等大事
2019-01-20 黄英男,马玉燕,金文婷 SIFIC感染官微
患者9天前开始出现发热,多在午后,Tmax 38.8℃,伴咳黄白痰。2018-08-05当地WBC 15.4*10^9/L;CRP 16.15mg/L,PCT 0.05ng/ml,Alb 20g/L,Cr 50μmol/L。尿蛋白++;胸部CT:左上肺团块影,考虑球形肺炎;G试验 >600,GM试验 0.34,血隐球菌乳胶凝集试验阴性,痰找抗酸杆菌阴性;予阿莫西林/克拉维酸+左氧氟沙星治疗1天,后
一、病史简介
男性,61岁,安徽人,2018-08-14入中山医院感染病科
主诉:发热伴咳嗽咳痰9天
现病史:
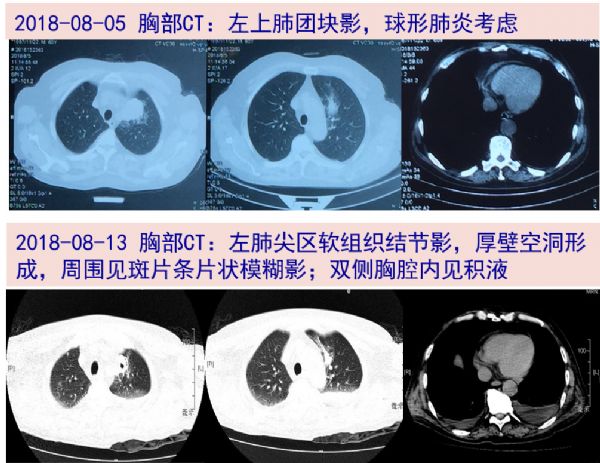
患者9天前开始出现发热,多在午后,Tmax 38.8℃,伴咳黄白痰。2018-08-05当地WBC 15.4*10^9/L;CRP 16.15mg/L,PCT 0.05ng/ml,Alb 20g/L,Cr 50μmol/L。尿蛋白++;胸部CT:左上肺团块影,考虑球形肺炎;G试验 >600,GM试验 0.34,血隐球菌乳胶凝集试验阴性,痰找抗酸杆菌阴性;予阿莫西林/克拉维酸+左氧氟沙星治疗1天,后改比阿培南+氟康唑治疗2天,体温高峰无下降;08-09调整为头孢哌酮/舒巴坦+莫西沙星;08-11改为亚胺培南;仍发热,Tmax 41℃,伴咳痰。
2018-08-13至我院急诊,复血常规:WBC 15.6*10^9/L,N 92.6%,CRP 17.3mg/L,PCT 0.23ng/ml;Alb 16g/L,Cr 60μmol/L,G试验 2478.80;T-spot 0/0;肺支原体抗体、呼九联、隐球菌荚膜抗原、自身抗体均阴性;胸部CT示“左上肺结节,炎性可能大,双侧胸腔积液伴双下肺少许膨胀不全,心包少量积液”。腹部CT为“胆囊炎可能;胰头可疑占位,合并胰腺炎待排;腹盆腔积液伴系膜及腹膜增厚”。予头孢吡肟2g qd+莫西沙星0.4g qd+氟康唑 0.2g qd+甲泼尼龙40mg qd治疗,体温降至正常。
2018-08-14早晨出现腹泻,黄色稀水样便,共4次,无恶心呕吐腹痛等,为进一步诊治收住中山医院感染病科。
既往史: 2018-01出现下肢水肿,2018-05当地肾穿病理:符合II期膜性肾病,抗M型磷脂酶2受体(PLA2R):+/-,予甲泼尼龙+环磷酰胺冲击治疗,后甲泼尼龙逐渐减量,环磷酰胺每月一次静滴;2018-08-06甲泼尼龙调整为40mg qd po,08-12因口腔白斑调整为24mg qd;末次环磷酰胺治疗日期为2018-07-25,累积剂量2.0g。2018-01发现高血压,口服氨氯地平+氯沙坦,血压控制可。否认糖尿病、冠心病等。
二、入院检查(2018-08-14入院)
【体格检查】
T 36℃,P 110bpm,R 20bpm,BP 151/107mmHg
神清,精神可,双肺未及干湿啰音。
【实验室检查】
血常规:WBC 13.64X10^9/L,N 93.9%,Hb 115g/L,PLT 288X10^9/L
尿常规:RBC 41/μL,WBC 44μL,蛋白 +++,亚硝酸盐-
炎症标志物:ESR 64mm/H,hs-CRP<5mg/L,PCT 0.13ng/mL;SF 1979ng/ml;
血气分析:PH 7.47,PaO2 128mmHg(吸氧3L/min),SpO2 99%;
生化:K 3.4mmol/L,ALT/AST 24/15U/L,Alb 18g/L,Scr 85umol/l, 余基本正常;
肿瘤标志物:CEA 6.4ng/ml,余均阴性
病毒抗体:CMV抗体IgM-、IgG+;EBV抗体IgG-、 IgA+;单个核细胞EBV-DNA 1.90×10^4/ml,血浆EBV-DNA阴性
细胞因子:IL-2受体 1371U/mL,IL-6 3.8 pg/mL,TNF 13.3pg/mL,余正常;
细胞免疫:Th淋巴细胞 CD4:30.2%;Ts淋巴细胞 CD8: 37.8%;CD4/CD8: 0.8;
血培养(-),痰细菌培养(-);
GM试验(-)
三、临床分析
病史特点:患者老年男性,有免疫抑制基础,主要表现为发热伴咳嗽咳痰,血常规白细胞及中性粒升高,CRP轻度升高,多种抗感染药物治疗均无好转,肺内病灶出现空洞和胸腔积液。疾病诊断考虑如下:
1、感染性疾病:
肺曲霉菌病:临床表现和胸部影像学可因患者免疫功能状态表现为多态性,胸部影像学典型可表现为结节、空洞、晕轮征、新月征等。本患者为免疫抑制状态,长期使用激素及免疫抑制剂,外院G试验阳性,胸部CT示短时间内病灶出现空洞,需警惕曲霉感染。可行肺活检和抽取胸腔积液做病理学和微生物学检查以明确诊断。
隐球菌感染:全身症状轻重不一,可有发热、干咳,偶有少量咯血、乏力、体重减轻,影像学表现多样,较为特征的为单发或多发结节,可伴有小空洞形成,多位于周围肺野。本患者隐球菌荚膜乳胶试验阴性不支持本病,但隐球菌病患者约有30%概率为该试验阴性,确诊同样有赖于组织病理学或微生物学的培养技术等。
其他特殊病原体感染:如结核、非结核分枝杆菌(NTM)、诺卡菌、放线菌等病原体引起的感染。本例患者喹诺酮类抗感染效果不佳,T-spot不高,病变发展速度似乎也不太符合结核的特点。放线菌感染,通常表现为慢性化脓性感染,以口腔菌群吸入为其主要发病机制,患者肺部病灶部位,似乎也不太符合。本例的免疫抑制基础,抗感染治疗效果不佳,需要考虑NTM或诺卡菌感染,但这些菌常规实验室检测困难,容易漏检,可以与实验室联系,加做弱抗酸染色,以及延长培养时间并关注这些细菌生长情况,同时送标本行病原体基因检测(mNGS)提高病原体检出率。
合并其他部位感染:患者有反复发热,虽然有肺部病灶解释,但患者腹部CT提示胆囊炎可能;胰头可疑占位,合并胰腺炎待排;腹盆腔积液伴系膜及腹膜增厚。需进一步排除合并肺外感染的可能性。
2、非感染性疾病:
肿瘤:患者中年男性,CEA稍高,结合腹部影像学,不排除合并肿瘤,甚至肿瘤引起的发热可能性。且患者伴有膜性肾病,可能与肿瘤相关。可进一步行相关检查,包括PET/CT和组织活检等。
风湿性疾病累及肺:风湿性疾病累及肺主要变现为肺间质纤维化,也可有发热症状,但患者无皮疹、关节酸痛、雷诺现象等表现,自身抗体阴性,目前风湿性疾病依据不足。
四、进一步检查、诊治过程和治疗反应
2018-08-14 起予亚胺培南(因恶心纳差明显,08-18调整为美罗培南1g q12h)+伏立康唑+SMZ-Co抗感染,同时予甲强龙 20mg qd治疗膜性肾病。
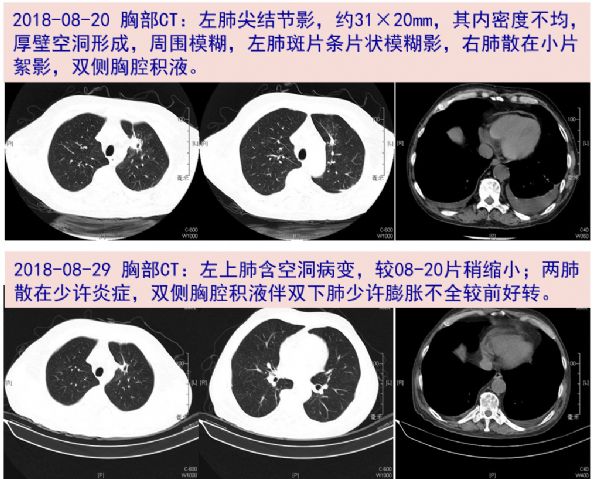
08-20 复查血常规及炎症标志物转为正常。胸部CT:左上肺结节,较08-12片略有缩小,两肺散在少许炎症,胸腔积液较前稍减少。
08-21 PET/CT:左肺上叶炎性结节可能,合并MT不除外
08-24 体温平;美罗培南降级为哌拉西林他唑巴坦 4.5g q8h
08-29 复查血常规及炎症标记物均正常范围,胸部CT示右上肺病灶较08-20有所吸收。予出院,出院后伏立康唑单药口服。出院后继续予甲强龙20mg qd治疗膜性肾病,肾内科会诊建议暂不调整激素剂量,暂缓免疫抑制剂使用。
第2次住院
2018-09-03 出院后5天,患者再次畏寒发热,Tmax 39℃,伴咳嗽,门诊予左氧氟沙星0.5g qd,体温仍波动于38.5-39.5℃;
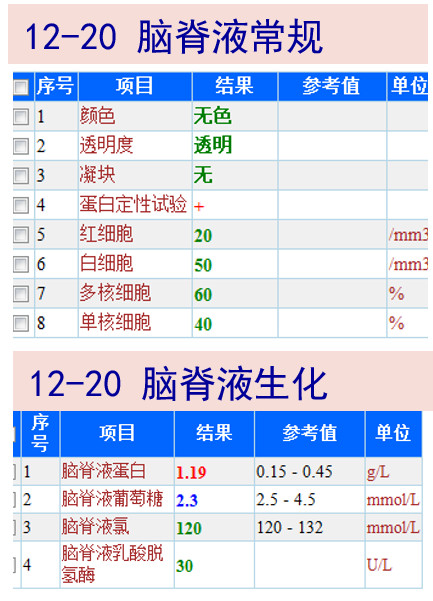
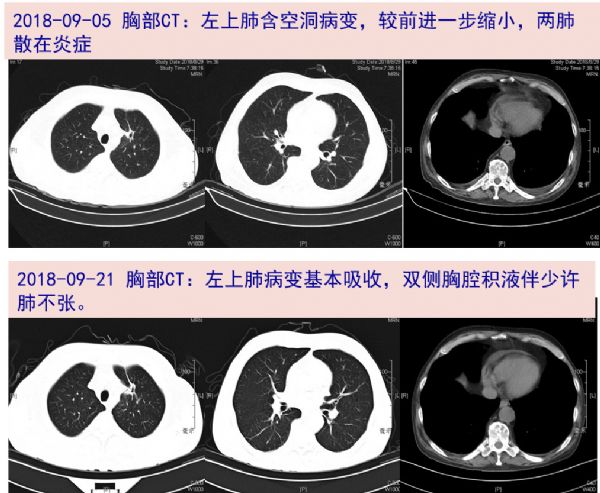
09-04 再次收治中山感染病科。查血常规:WBC 12.03*10^9/L,N 79.2%;ESR 14mm/H,CRP 3.0mg/L,PCT 0.05ng/ml;肝肾功能基本正常;血培养(需氧+厌氧)阴性。胸部CT:左上肺含空洞病变,两肺散在少许炎症,双侧胸膜稍厚,整体较前08-29片好转。
09-04 考虑抗真菌治疗病灶有吸收,不排除合并其他感染可能,予伏立康唑+氟胞嘧啶抗真菌治疗,并加用哌拉西林/他唑巴坦抗细菌。
09-06 因发热、外周血单个核EBV-DNA两次阳性,考虑EBV感染不除外,使用伐昔洛韦抗病毒7天。同时继续甲泼尼龙20mg qd治疗膜性肾病,并遵肾内科建议予丙种球蛋白 10g*3d。
09-10 仍高热,Tmax 40℃,行头颅增强MRI:脑内少许腔隙缺血灶,鼻窦轻度炎症。
09-12 骨穿+活检:未见明确血液系统疾病依据。
09-18 甲泼尼龙加量至40mg qd;
09-21 复查胸部CT基本吸收,停抗细菌药物,考虑肺部病灶吸收快,曲霉感染可能小,停用伏立康唑,但患者仍有发热,不除外特殊病原体感染,改米诺环素单药治疗。
09-26 起头痛明显。09-28 头颅CT:脑内散在腔梗缺血灶;
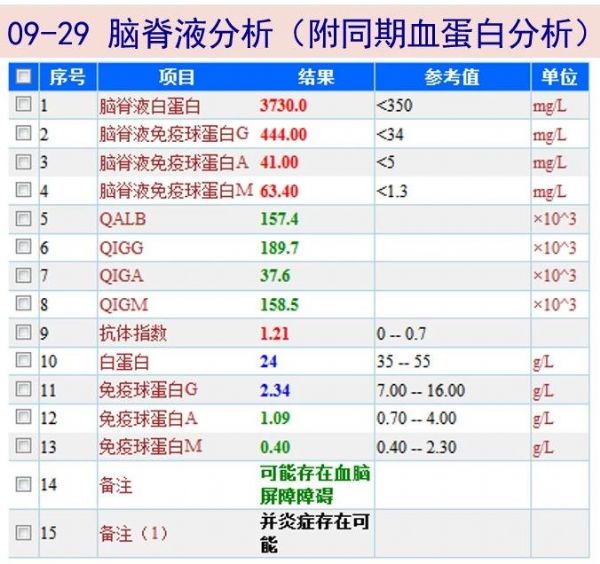
09-29 行腰穿,提示颅压增高,测初压为190 mmH2O;脑脊液常规提示WBC升高中性为主,生化示低糖低氯明显,蛋白升高明显。考虑中枢感染,予美罗培南+莫西沙星+SMZ-Co+更昔洛韦抗感染,并予甘露醇降颅压;后脑脊液ADA、细菌及真菌涂片+培养、隐球菌抗原回报均阴性;
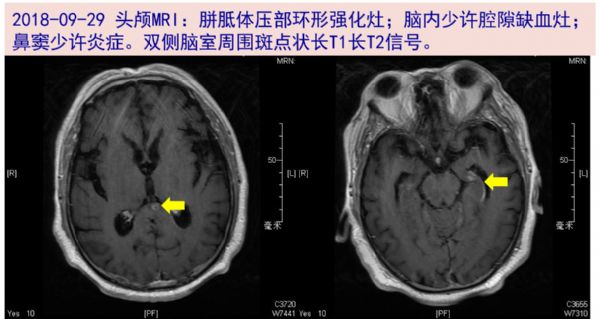
09-29 头颅增强MRI:胼胝体压部环形强化灶;双侧脑室周围斑点状长T1长T2信号。脑内少许腔隙缺血灶;鼻窦少许炎症。
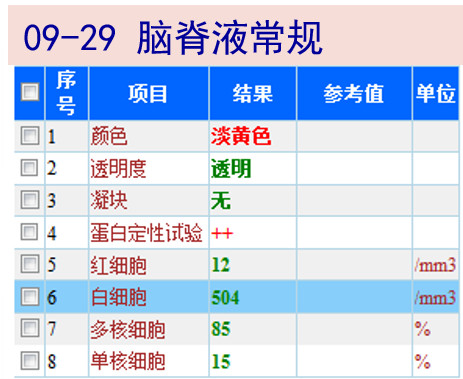

09-29 神经科会诊:考虑脑室炎,调整抗感染方案为美罗培南+莫西沙星+伐昔洛韦,继续甲强龙抗炎以及对症支持治疗。
09-29 寄生虫抗体回报:阴性(09-25送检)
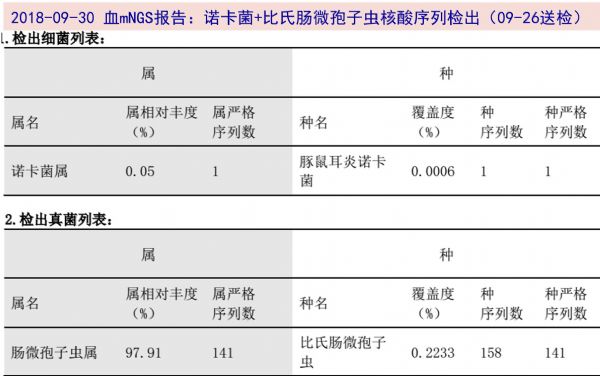
09-30血mNGS回报:诺卡菌属(豚鼠耳炎诺卡菌)序列数1条,比氏肠微孢子虫序列数141条。患者仍有发热,考虑寄生虫感染不除外,予以加用阿苯达唑抗肠微孢子虫治疗2周。
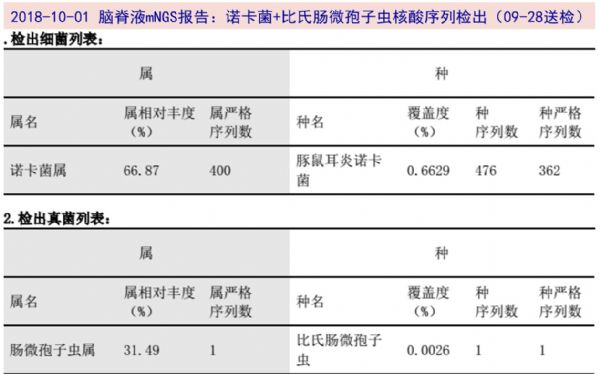
10-01 脑脊液mNGS回报:诺卡菌属(豚鼠耳炎诺卡菌)检出序列数362条,比氏肠微孢子虫序列数1条;电联微生物室脑脊液细菌培养延长至2周,后回报阴性。
10-01 考虑患者为中枢神经系统豚鼠耳炎诺卡菌感染,调整抗感染方案:继续予以美罗培南+莫西沙星治疗。
10-11起患者体温逐渐转平,头痛、恶心、呕吐好转;10-19起患者体温平
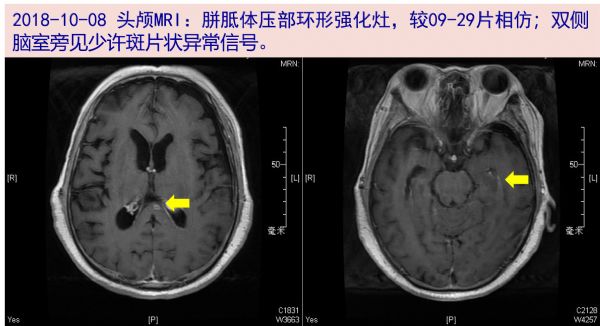
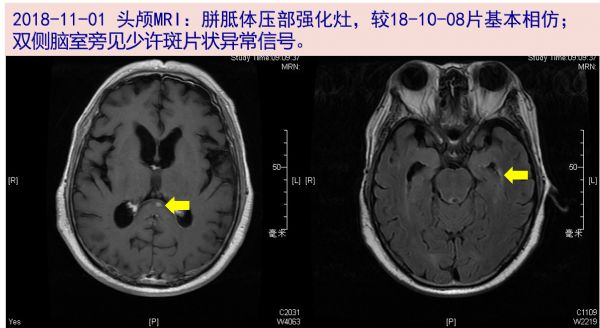
10-08 头颅增强MRI:胼胝体压部环形强化灶,较09-29片相仿;双侧脑室旁见少许斑片状异常信号。
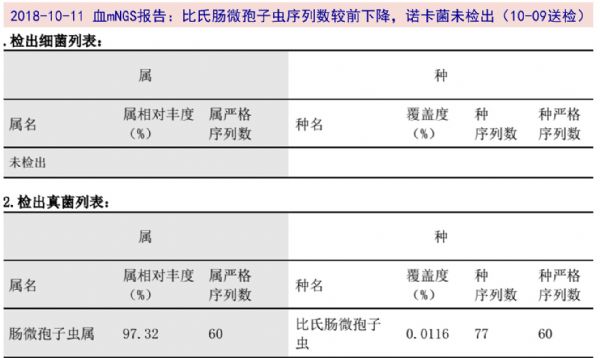
10-11 血mNGS复查回报:比氏肠微孢子虫序列数60条,较前下降,诺卡菌序列未检出。
10-16 复查腰穿,脑脊液压力下降至正常(初压135mmH2O);WBC较前下降,生化较前好转;后陆续回报:脑脊液隐球菌抗原阴性;脑脊液涂片找细菌、真菌、抗酸杆菌及隐球菌均阴性。
10-18 脑脊液mNGS:诺卡菌检出序列数22条,较前明显下降,肠微孢子虫序列未检出。
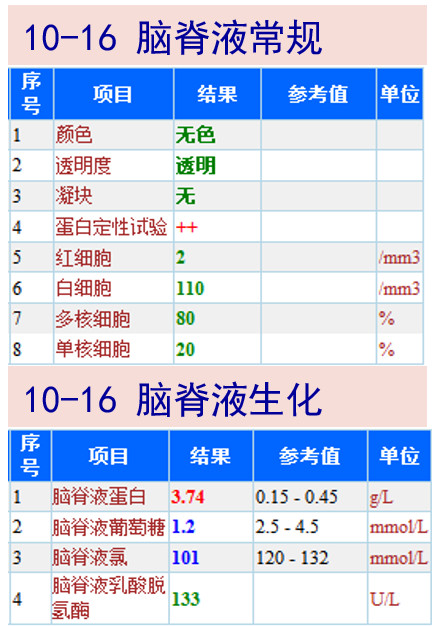
患者头痛、发热症状明显好转;随访炎症标记物较前下降,后因恶心呕吐停莫西沙星,继续予美罗培南+SMZ-Co抗感染,以及其他对症支持治疗(SMZCo使用后消化道副作用明显,于10-22停用)
神经内科专家会诊,自阅片考虑胼胝体环形强化及左侧脑室后角强化,考虑中枢神经系统感染:诺卡菌感染可能较大,脑脊液蛋白较高,10-18起激素调整为地塞米松20mg预防脑室粘连,并逐渐减量;10-29地塞米松减至5mg qd,患者再次出现体温升高,再次加用莫西沙星0.4g qd 抗感染。
治疗期间,10月中旬出现幻视,被害妄想,神经内科考虑幻视与颅内病变相关,心理科会诊考虑幻觉妄想状态,予以利培酮0.25ml qn po好转后停用,后未再出现幻视。
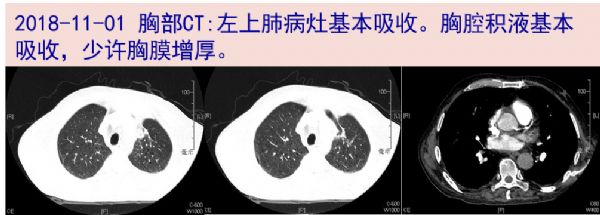
11-01胸部CT:左上肺病灶基本吸收。双侧胸腔积液基本吸收,少许胸膜增厚。头颅MRI:胼胝体压部强化灶,较18-10-08片基本相仿;双侧脑室旁见少许斑片状异常信号;脑内少许腔隙性缺血灶,老年脑。建议患者复查脑脊液以评估病情,患者及家属表示拒绝。
出院后随访
11-13 出院至当地继续美罗培南+莫西沙星抗感染治疗
12-19 为随访病情,再次入院。
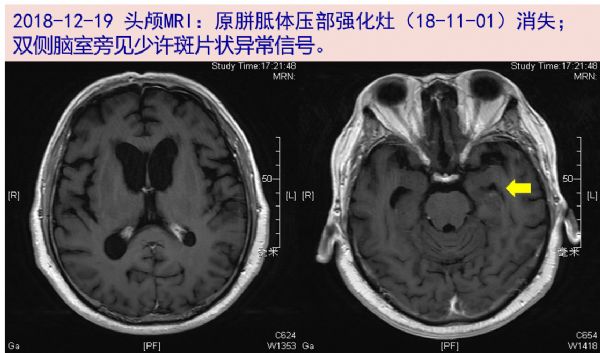
12-19复查增强头颅MRI:原胼胝体压部强化灶(11-01)消失; 双侧脑室旁见少许斑片状异常信号;脑内少许腔隙性缺血灶;老年脑。
12-20复查腰穿提示常规、生化均明显好转。
五、最后诊断与诊断依据
最后诊断:
豚鼠耳炎诺卡菌感染(肺,脑)
膜性肾病
诊断依据:
患者老年男性,有免疫抑制基础,主要表现为发热伴咳嗽咳痰,血常规白细胞及中性粒升高,CRP轻度升高,胸部CT提示左上肺病灶伴空洞,抗细菌治疗有效;但反复高热、后出现头痛,腰穿示脑脊液压力升高,常规及生化提示化脑表现,头颅增强MRI提示胼胝体炎性病灶,脑室旁斑片状异常信号,血及脑脊液NGS测序提示豚鼠耳炎诺卡菌;抗诺卡菌治疗后,患者头痛发热症状明显好转,脑脊液常规、生化好转,随访NGS监测脑脊液诺卡菌序列明显下降;头颅MRI提示胼胝体病灶吸收,故考虑诺卡菌颅内感染诊断成立,回顾肺部病灶治疗过程,抗细菌+曲霉治疗后迅速吸收,后停抗曲霉后病灶进一步吸收,曲霉感染证据不足,考虑肺内病灶亦为诺卡菌感染。此外,虽然血液检测到较多的肠微孢子虫核酸序列,临床意义不明,可能为环境污染微生物,综合分析疾病过程,肺部和颅内感染应该与肠微孢子虫无关。
六、经验与体会
本例患者以肺部起病,外院多种抗细菌治疗无效,入院后改用同时覆盖细菌和真菌的抗感染治疗后病情明显好转,考虑肺部真菌感染,但微生物学检查未获明确结果。后因再次发热,并出现明显头痛等脑部症状,进而对累及颅内引起关注。然而复查头颅MRI虽然发现病灶,被判断为“脑内少许腔隙缺血灶”。后进行腰穿并送脑脊液mNGS测序,终于获得诺卡菌感染的诊断。此案例也再次验证,临床上无明显脑膜刺激征的中枢神经系统感染非常隐匿,可仅表现为发热,炎症标志物升高不明显,临床诊断困难,容易漏诊、误诊。
诺卡菌属生长缓慢,容易实验室漏诊,对于此类生长缓慢、或者需要特殊培养基的病原体、或者经过抗菌药物治疗后,传统培养常无阳性发现,mNGS可成为诊断的有力补充,亦可成为监测病原载量的重要工具。
诺卡菌其广泛存在于世界各地的土壤、腐烂蔬菜和水生环境中,一般认为吸入是最常见的感染途径,引起肺诺卡菌病,也可经被污染的食物通过胃肠道致病、外伤导致皮肤感染,以及院内传播。诺卡菌不属于人体正常菌群,其感染通常认为是一种机会性感染,免疫抑制患者患病率较高,且容易播散至其他器官尤其是中枢神经系统。该患者长期使用激素及免疫抑制剂,存在免疫抑制状态,以发热、肺部感染起病,后出现头痛,腰穿提示化脑性表现,符合诺卡菌感染的特点。
诺卡菌通常引起播散性感染,形成脓肿如皮肤脓肿、脑脓肿常见,所有免疫功能受损患者和所有肺部诺卡菌病患者均需考虑是否有颅内累及、行脑部影像学检查或腰穿排除。本患者脑脊液压力高,常规+生化提示化脑性改变,但MRI未见明显脑脓肿占位,可见胼胝体病灶、左侧脑室旁异常信号,故考虑脑室炎可能,诺卡菌感染引起的脑室炎实属罕见。
具有抗诺卡菌活性的药物包括SMZCo、阿米卡星、亚胺培南、美罗培南、三代头孢菌素类(头孢曲松和头孢噻肟)、米诺环素、超广谱氟喹诺酮类药物(如莫西沙星)、利奈唑胺、替加环素和氨苯砜。不同分离株对抗菌药物的敏感性不同。重症患者如播散性或CNS感染,以及免疫抑制者超过1个部位受累,需要联合用药。该患者免疫抑制状态,mNGS证实为豚鼠耳炎诺卡菌感染,累及肺、中枢,病程严重,故予碳青霉烯类+复方磺胺联合抗感染治疗,收到了良好的效果。
诺卡菌感染推荐长疗程治疗,疗程不足,容易复发。免疫正常的单纯皮肤感染者通常治疗3-6个月,若有免疫受损则为6-12个月,严重肺部感染需治疗6-12个月或更长。所有免疫功能受损的患者(单纯性皮肤感染者除外)以及CNS受累者应至少治疗1年。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









好 学习了 不断探求病因
100