Blood Adv:BCMA CAR-T治疗RRMM后的淋巴细胞绝对值可预测缓解
2024-05-27 聊聊血液 聊聊血液 发表于上海
该研究是首次报道BCMA CAR-T输注后ALC与临床结局的关联及其在预测RRMM患者缓解方面的应用。
CAR-T后的淋巴细胞绝对值
靶向BCMA CAR-T细胞是复发/难治性多发性骨髓瘤(RRMM)的有效治疗手段,但缓解治疗后的缓解持续时间(DoR)差异较大。CAR-T细胞输注后的扩增及持续时间可预测缓解深度和持续时间,但检测CAR-T细胞扩增的技术仍处于研究阶段,尚缺乏预测缓解的预后因素。
R/R B-ALL的研究证实,CD19 CAR-T输注后两周内淋巴细胞绝对值(ALC)增加,且+10天时的ALC峰值与持续缓解存在相关性。但该现象尚未在其他血液肿瘤中予以证实。因此美国3家中心的学者开展研究,描述了RRMM患者在BCMA CAR-T治疗后的ALC动力学,以及该动力学与免疫介导毒性和临床结局的关联。该研究是首次报道BCMA CAR-T输注后ALC与临床结局的关联及其在预测RRMM患者缓解方面的应用,近日发表于《Blood Advances》。

重点
1、BCMA CAR-T细胞输注后前15天的最大ALC (ALCmax)与更深缓解及CRS和ICANS的发生相关。
2、ALCmax≤0.5 x103/uL是无缓解的预测指标,而>1.0是持续缓解的独立预后生物标志物。
研究结果
该研究纳入美国3家中心(威尔康奈尔医学中心,哥伦比亚大学欧文医学中心,西奈山医院)接受cilta-cel或ide-cel治疗的RRMM患者。监测并分析ALC的动力学。
患者特征
研究共纳入156例患者,基线特征见表1。接受cilta-cel和ide-cel治疗的患者基线特征平衡,且CRS/ICANS无差异(CRS:88% vs 86%,p=0.75;ICANS:13% vs 11%,p=0.65)。多数CRS为1级(cilta-cel和ide-cel分别为73%和76%)。所有患者中位随访17.5个月,cilta-cel和ide-cel分别为9.4个月和33.2个月。
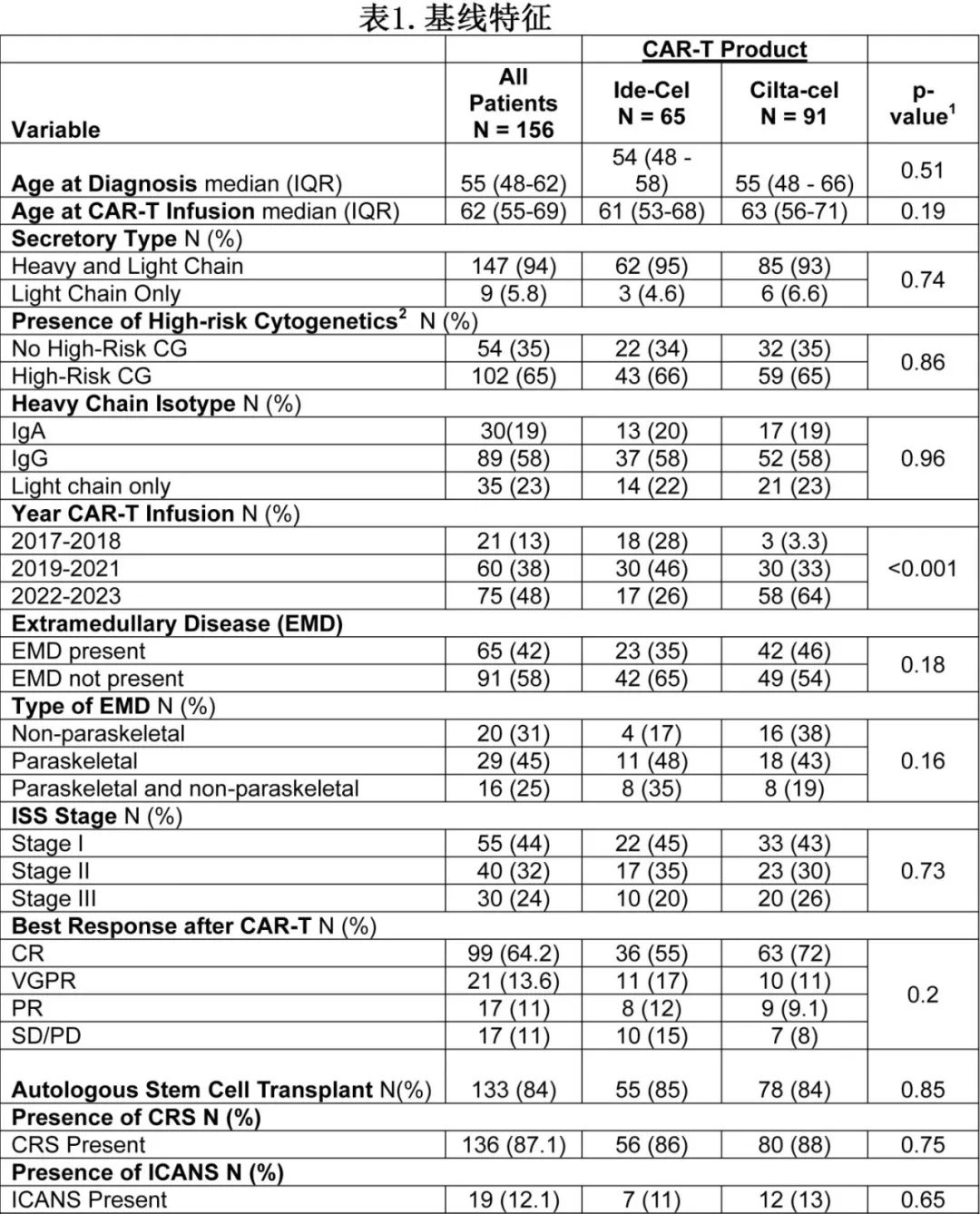
整个队列的总缓解率(ORR)为89%,完全缓解率(CR)为65%,MRD阴性率为46%。
BCMA CAR-T后的ALC动力学
研究中监测-5到+15天的ALC。两个产品+6到+7天的ALC均增加,且ALCmax(0天到+15天的ALC最高值)和至ALCmax时间存在显著差异。cilta-cel和ide-cel组预处理前的ALC分别为0.83 x103/uL和1.0 x103/uL (p=0.6);所有患者的ALCmax为1.28 x103/uL,且cilta-cel高于ide-cel (2 x103/uL vs 0.8 x103/uL,p<0.001)。所有患者ALC的绝对变化值(ALCmax与0天时的差异)为1.28 x103/uL,且cilta-cel高于ide-cel (2.1 x103/uL vs 0.77 x103/uL,p<0.001)。使用3.75 x103/uL作为ALC的正常值上限,cilta-cel组32%发生淋巴细胞增多,而ide-cel组为0;与之类似,cilta-cel和ide-cel组ALCmax >1.0 x103/uL的比例分别为74%和29% (p<0.001)。ide-cel组的至ALCmax时间短于cilta-ce组(+11天vs +12天,p=0.002)。
ICANS和CRS与ALC的关联
细胞因子释放综合(CRS)与较高的ALCmax相关,包括所有患者中(优势比[OR]=5.16,P=0.018)和cilta-cel组(OR=12.6,P=0.013),ide-cel组有相关趋势但不显著(OR=1.38,P=0.1)。免疫效应细胞相关神经毒性综合征(ICANS)与较高的ALCmax相关,包括所有患者中(OR=6.6,p=0.005) 和cilta-cel组(OR=13,P=0.009)、ide-cel组(OR=1.57,p=0.03)。此外有趣的是,发生神经毒性的患者ALCmax高于未发生神经毒性的患者(4.3 vs 1.1 x103/uL,p=0.02)
此外,较高级别的CRS与较高的ALCmax相关,包括所有患者和两组都是如此(表2)。ide-cel组的至CRS时间早于cilta-cel组(1天vs 7天,P<0.001)。cilta-cel组发生CRS的患者的ALCmax高于未发生CRS患者(2.5 x103/uL vs 0.46 x103/uL,P=0.001),但ide-cel组无差异。
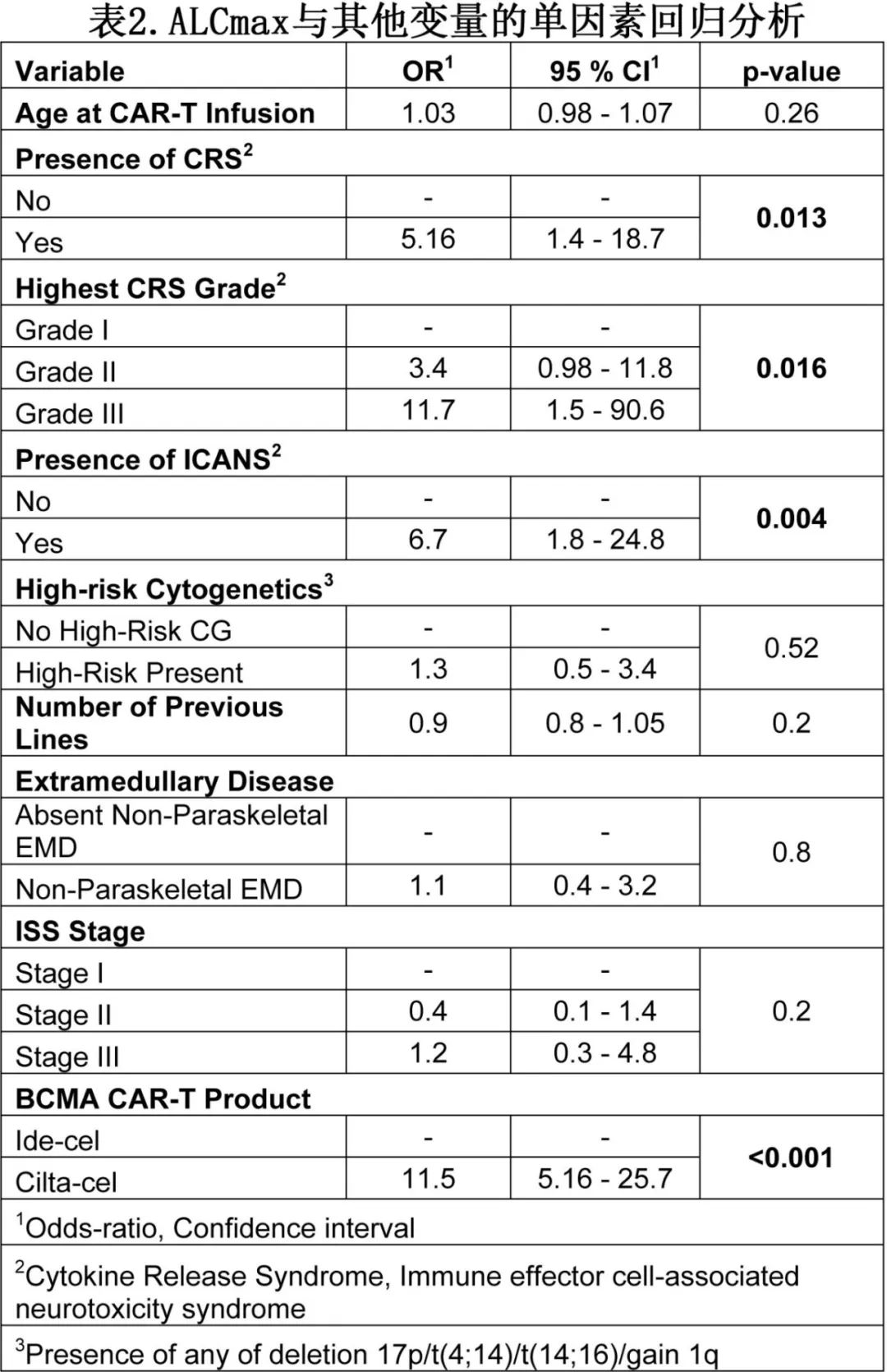
ALC与CAR-T后的结局
PFS和DOR
cilta-cel和ide-cel组的91和65例患者中,分别有70和25例发生进展和死亡事件。单因素分析中,ALCmax >1.0 x103/uL、ALCmax>队列中位值、ALCmax处于第二/第三分数与较长PFS相关,非骨旁EMD和CAR-T产品与较差的PFS相关;两个产品的单独分析也是如此。ALCmax >1.0 x103/uL患者的PFS优于≤1.0 x103/uL患者(30.5个月 vs 6.01个月,HR=0.34,P<0.001;图1A)。
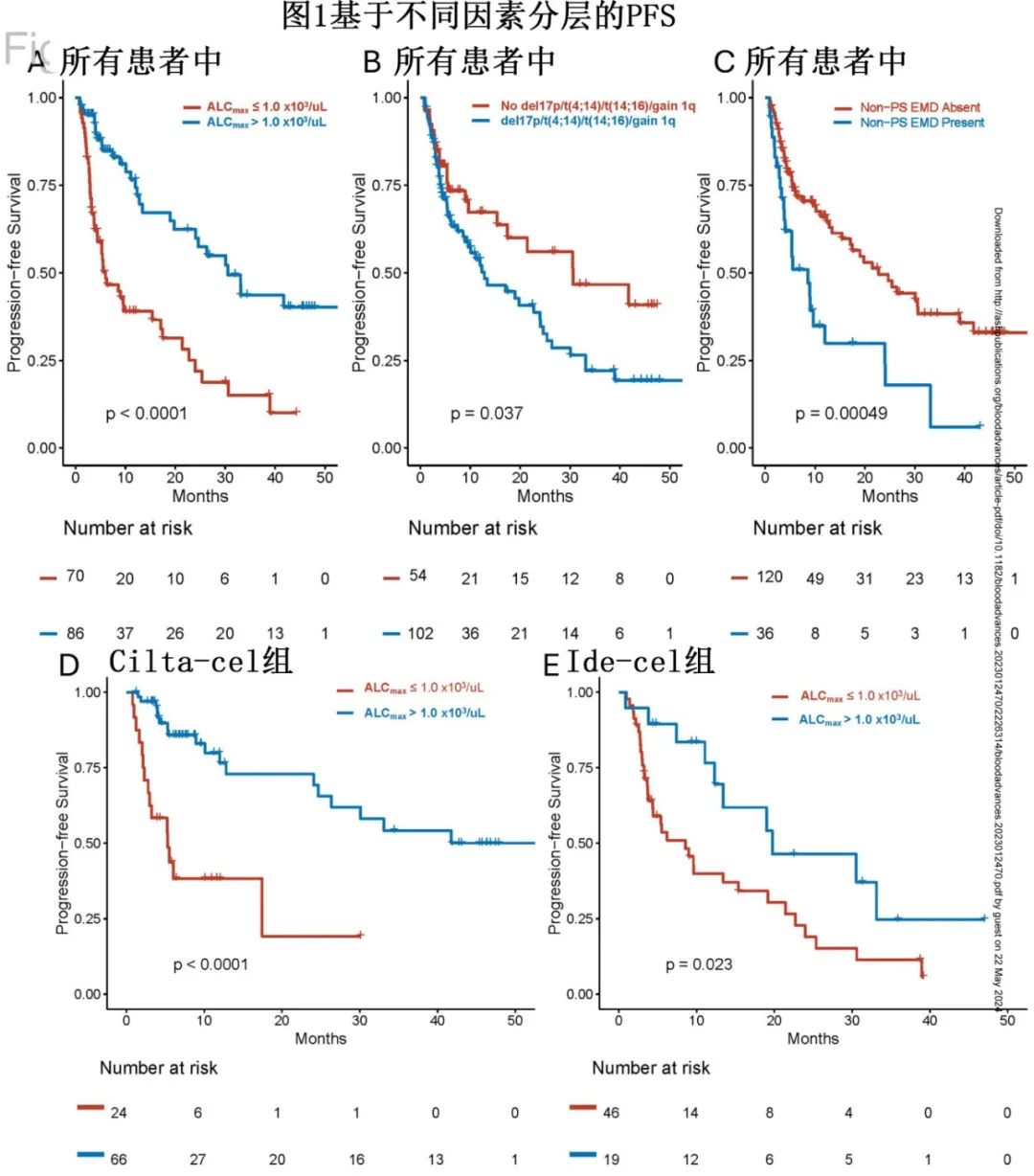
多因素分析校正非骨旁EMD、高危细胞遗传学、既往治疗线数和CAR-T产品后,仅ALCmax >1.0 x103/uL (HR=0.37,p<0.001)存在非骨旁EMD(HR=2.15,p=0.003)仍与PFS显著相关(表3)。ALCmax >1.0 x103/uL与改善PFS的关联还存在于高危细胞遗传学((19.8 vs 5.3个月,p<0.001)和非骨旁EMD(12 vs 4.5个月,p=0.008)患者中。
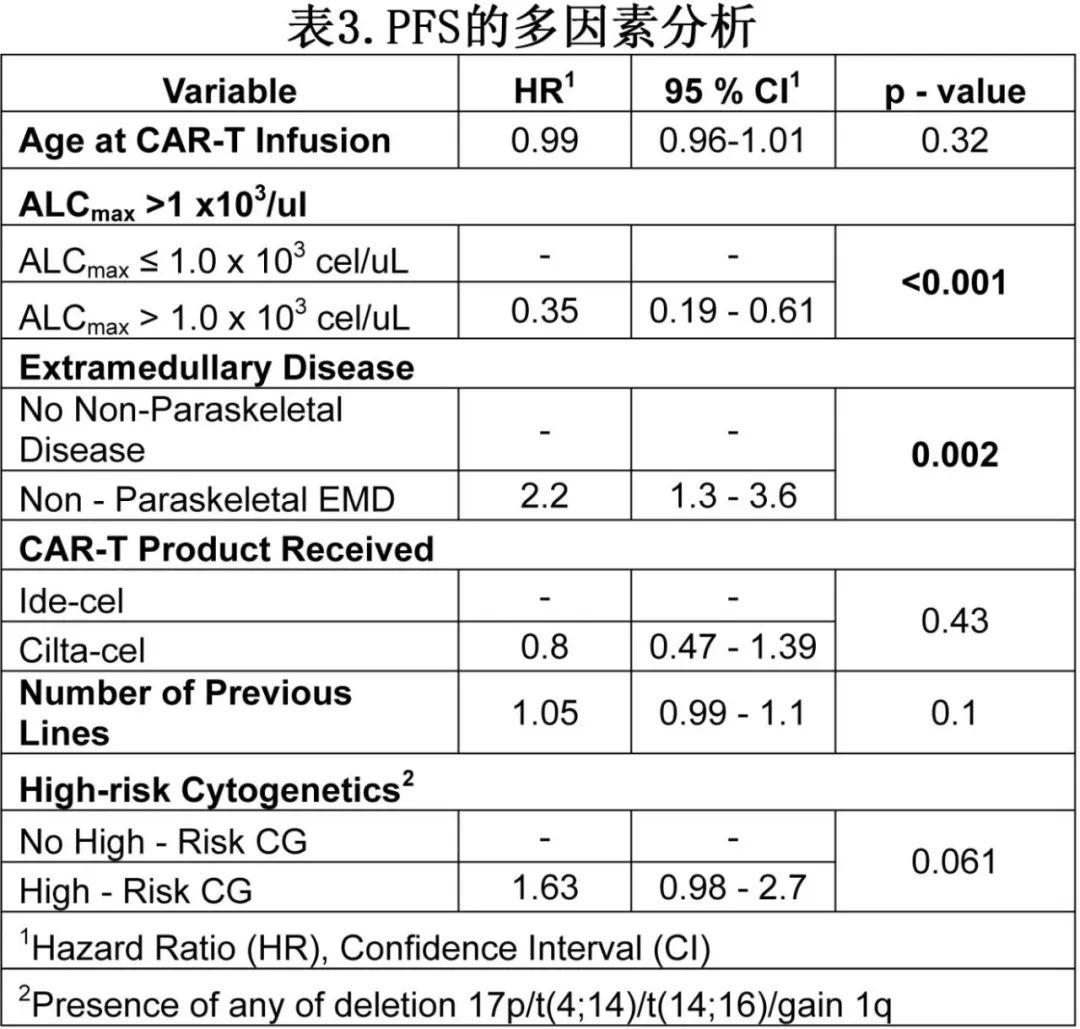
对于DOR,137例(82例cilta-cel和55例ide-cel)患者中结果类似。多因素分析控制相关变量后,ALCmax >1.0 x103/uL与DOR改善(HR=0.46,p=0.025)相关。
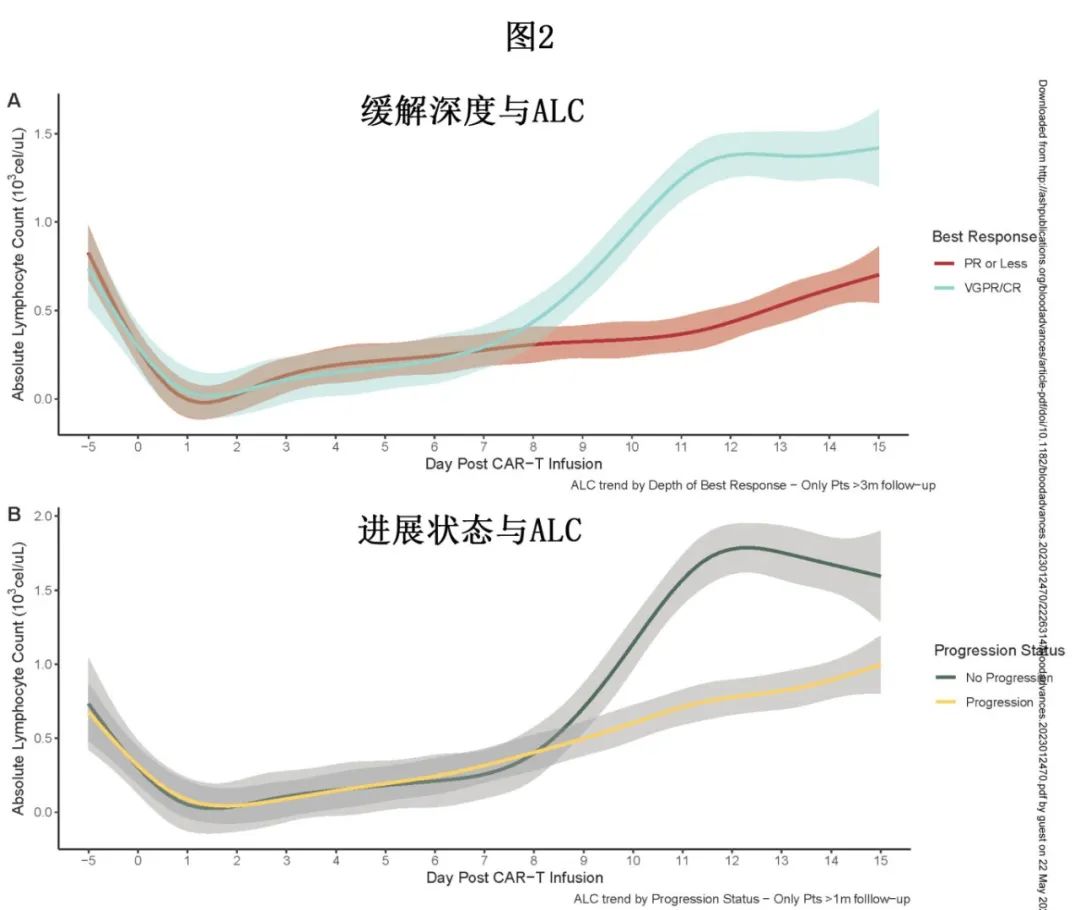
缓解深度和进展状态
VGPR/CR患者的ALCmax高于最佳缓解为PR和SD/PD的患者(表4)。
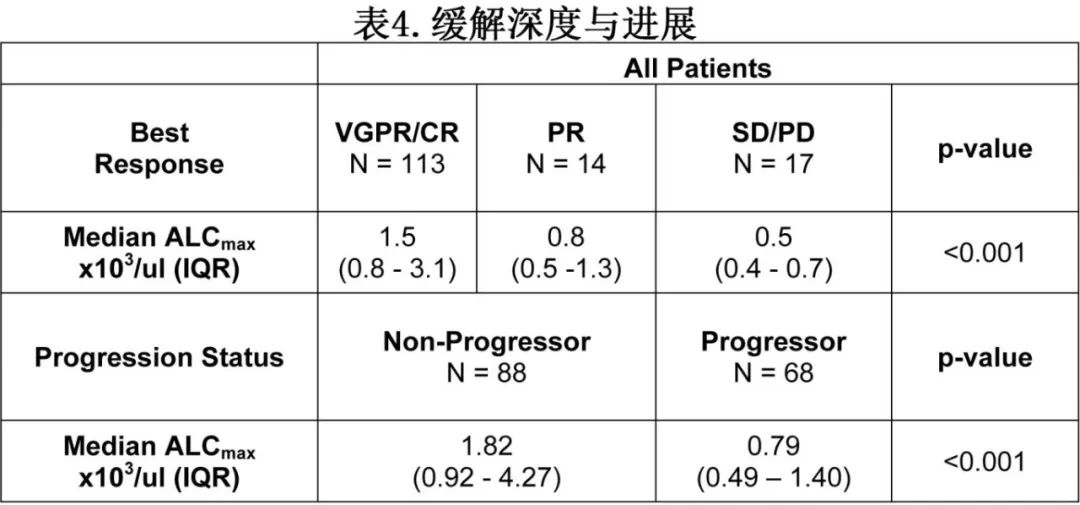
多因素分析中,ALCmax、ALC绝对值变化和ALCmax >1.0 x103/uL与达到≥VGPR相关,ALCmax >1.0 x103/uL还与进展风险较低相关。重要的是,预处理前ALC和基线ALC不影响缓解深度,ALCmax不影响至初始或最佳缓解时间。此外,未进展患者的ALCmax高于进展患者(1.86 vs 0.79 x103/uL,p<0.001),≥VGPR 患者的ALCmax也更高(1.67 x103/uL vs 0.5 x103/uL, p<0.001)。
ALCmax作为预后工具的不同临界值
本部分旨在探索不同的ALCmax临界值是否可以预测更深缓解、更长PFS或早期进展。
ALCmax ≤0.5 x103/uL可预测缺乏缓解和较短PFS:ALCmax ≤0.5 x103/uL患者的中位PFS短于>0.5 x103/uL患者(3.7 vs 24.1个月,P<0.001)。
ALCmax >1.0 x103/uL可预测较长PFS:ALCmax >1.0 x103/uL患者的中位PFS较长(33.1 vs 6个月,P<0.001);ide-cel组(19.8 vs 8.5个月,p=0.023)和cilta-cel组(未达到vs 5.3个月,p<0.0001)也是如此(图1D、E)。
CAR-T输注后的淋巴细胞增多主要是由BCMA CAR-T淋巴细胞驱动
通过流式细胞术分析四例患者的外周血样本,观察到ALC与BCMA+ T细胞比例之间存在显著的强相关性(Spearman r=0.93, p<0.0001),表明ALC是CAR-T扩增的良好指标。
BCMA CAR-T ALC的动力学与CD19 CAR-T治疗NHL不同
作者纳入威尔康奈尔医学中心接受axicabtagene ciloleucel (axis-cell)、lisocabtagene maraleucel (liso-cell)、tisagenlecuucel (tisa-cell)或brexucabtagene autooleucel (brexue-cell) CD19 CAR-T治疗NHL的105例患者作为NHL队列,分析第-5天到第+15天的ALC。
当比较BCMA与CD19 CAR-T时,ALC动力学存在差异。BCMA CAR-T的中位ALCmax为1.3 x103/uL,至ALCmax的中位时间为12天,而CD19 CAR-T的中位ALCmax为0.47 x103/uL,至ALCmax的中位时间为10天,两者差异有统计学意义(p<0.001)(图3)。
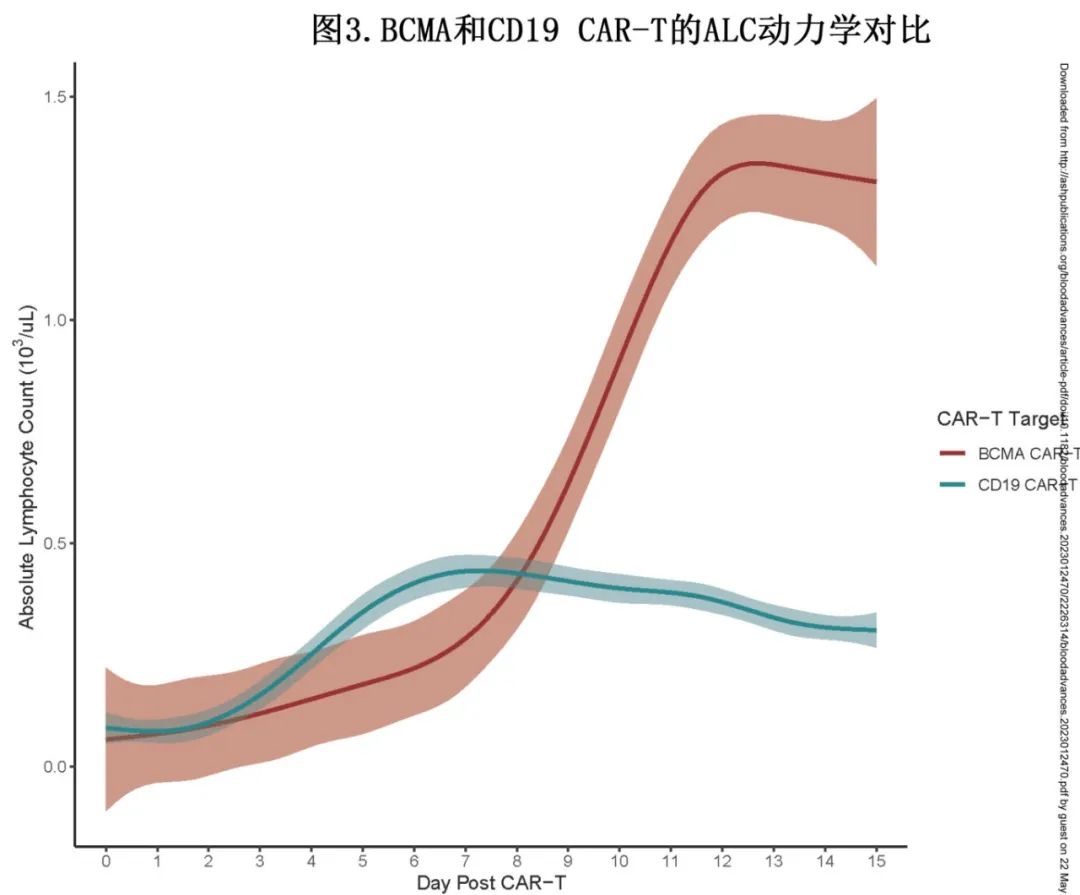
总结
该多中心研究描述了156例接受BCMA CAR-T(cilta-cell和ide-cell)治疗的RRMM患者输注后15天内ALC的动力学和预后影响。最大ALC (ALCmax)较高的患者具有更好的缓解深度、无进展生存期和缓解持续时间。ALCmax >1.0 x103/uL的患者的PFS优于≤1.0x103/uL的患者(30.5 vs 6个月,p<0.001),而ALCmax ≤0.5 x103/uL的患者是疾病早期进展和PFS较短的高危组(HR=3.4,p<0.001)。在多因素分析中,考虑ISS分期、年龄、CAR-T产品、高危细胞遗传学和既往治疗线数后,ALCmax >1.0 x103/uL和非骨旁EMD是PFS和DOR的唯一独立预测因子。此外,流式细胞术数据表明,ALC是BCMA CAR-T扩增的替代物,可以作为一种可获得的预后标志物。
该研究首次报道了BCMA CAR-T输注后ALC与临床结局的关联及其在预测RRMM患者缓解方面的应用,将输注后15天内的ALC作为一种新的、广泛可用的生物标志物,用于预测RRMM患者对BCMA CAR-T治疗的反应。ALCmax≤0.5 x103/uL是与缓解不佳和较短PFS相关的负面预后因素,而ALCmax >1.0 x103/uL是预示着BCMA CAR-T缓解更深和更持久的阳性预后因素。该研究结果也为进一步了解高ALC患者和低ALC患者在免疫微环境、CAR-T特征和T细胞特征方面的表型差异开启新的世界。
参考文献
Saldarriaga MM,et al.Absolute Lymphocyte Count after BCMA CAR-T Therapy is a Predictor of Response and Outcomes in Relapsed Multiple Myeloma.Blood Adv . 2024 May 22:bloodadvances.2023012470. doi: 10.1182/bloodadvances.2023012470.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#多发性骨髓瘤# #CAR-T治疗# #BCMA# #淋巴细胞绝对值#
84